
- •1. Материя и ее движение
- •2 Вещества и их изменение. Предмет неорганической химии
- •3. Закон сохранения массы. Основное содержание атомно-молекулярного учения
- •4. Эквивалент. Закон эквивалентности. Важнейшие классы и номенклатура неорганических веществ
- •5. Периодическая система элементов д.И. Менделеева
- •6. Теория химического строения
- •7. Общая характеристика p-, s-, d-элементов
- •8. Ковалентная связь. Метод валентных связей
- •9. Неполярная и полярная ковалентные связи
- •10. Многоцентровые связи
- •11. Ионная связь
- •12. Водородная связь
- •13. Превращение энергии при химических реакциях
- •14. Цепные реакции
- •15. Общие свойства неметаллов
- •16. Водород
- •17. Вода
- •18. Перекись водорода
- •19. Общая характеристика подгруппы галогенов
- •20. Хлор. Хлороводород и соляная кислота
- •21. Краткие сведения о фторе, броме и йоде
- •22. Общая характеристика подгруппы кислорода
- •23. Кислород и его свойства
- •24. Озон и его свойства
- •25. Сера и ее свойства
- •26. Сероводород и сульфиды
- •27. Свойства серной кислоты и ее практическое значение
- •28. Азот. Сигма– и пи-связи
- •29. Общая характеристика подгруппы азота
- •30. Аммиак
- •31. Соли аммония
- •32. Оксиды азота
- •33. Азотная кислота
- •34. Фосфор
- •35. Аллотропные модификации фосфора
- •36. Оксиды фосфора и фосфорные кислоты
- •37. Минеральные удобрения
- •38. Углерод и его свойства
- •39. Аллотропные модификации углерода
- •40. Оксиды углерода. Угольная кислота
- •41. Кремний и его свойства
- •42. Понятие коллоидных растворов
- •43. Соли кремниевой кислоты
- •44. Получение цемента и керамики
- •45. Физические свойства металлов
- •46. Химические свойства металлов
- •47. Металлы и сплавы в технике
- •48. Основные способы получения металлов
- •49. Коррозия металлов
- •50. Защита металлов от коррозии
- •51. Общая характеристика подгруппы лития
- •52. Натрий и калий
- •53. Едкие щелочи
- •54. Соли натрия и калия
- •55. Общая характеристика подгруппы бериллия
- •56. Кальций
- •57. Оксид и гидроксид кальция
- •58. Жесткость воды и способы ее устранения
- •59. Общая характеристика подгруппы бора
- •60. Алюминий. Применение алюминия и его сплавов
- •61. Оксид и гидроксид алюминия
- •62. Общая характеристика подгруппы хрома
- •63. Хром
- •64. Оксиды и гидроксиды хрома
- •65. Хроматы и дихроматы
- •66. Общая характеристика семейства железа
- •67. Железо
- •68. Соединения железа
- •69. Доменный процесс
- •70. Чугун и стали
- •71. Тяжелая вода
- •72. Соли соляной кислоты
53. Едкие щелочи
Щелочи образуют гидроксиды щелочных металлов 1 группы главной подгруппы при растворении их в воде.
Физические свойства: растворы щелочей в воде мылкие на ощупь, они разъедают кожу, ткани, бумагу – едкие щелочи (едкий натр NaOH, едкий калий КОН). На коже они вызывают долго незаживающие раны. Очень гигроскопичны.
Химические свойства LiOH, NaOH, КОН, RbOH, CsOH. В этом ряду сила и растворимость щелочей возрастает, что связано с увеличением размеров ионов щелочных металлов (катионов) и ослаблением электростатического притяжения с гидроксидной группой (анионом). К щелочам относится гидроксид щелочно-земельного металла бария – Ва(ОН)2.
Щелочи – сильные основания, химически очень активные вещества. При растворении их в воде выделяется большое количество теплоты.
В водном растворе идет диссоциация щелочей:
![]()
Химические свойства щелочей:
1) щелочи вступают в реакцию нейтрализации с кислотами, образуя соль и воду:
![]()
2) взаимодействуют с кислотными оксидами, образуя как средние, так и кислые соли:
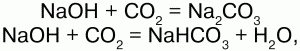
в ионной форме:
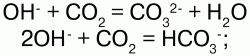
3) вступают со средними солями в реакцию обмена: CuSO4 + KOH = Cu(OH)2 + K2SO4, с кислыми солями: NaНSO4 + KOH = Na2SO4 + К2SO3 + H2O (окислительно-восстановительная);
4) растворы щелочей вступают в реакцию с амфотерными оксидами – образуются комплексные соли: Al2O3 + NaOH + 7Н2О = 2Na[Al(ОН)4(Н2О)2];
5) при сплавлении твердых щелочей с оксидами амфотерных металлов образуются двойные безводные соли: Al2O3 + 2NaOH = 2NaAlO2 (метаалюминат натрия);
6) взаимодействуют с галогенами в зависимости от температурных условий – на холоде: Cl2 + 2NaOH = NaClO + NaCl + H2O, при нагревании: 3Cl2 + 6NaOH = NaClO3 + 5NaCl + 3H2O;
7) взаимодействуют с некоторыми органическими веществами: С2Н5ОН + NaOH = С2Н5ОNa + Н2О;
8) растворы и расплавы щелочей подвергаются электролизу

Получение:
1) реакция металлов с водой: 2К + 2H2O = 2KOH + H2;
2) реакция оксидов металлов с водой: 2К2О + 2H2O = 2KOH.
Применение: NaOH и KOH используют в производстве мыла, бумаги, в текстильной промышленности и др.
54. Соли натрия и калия
Натрий и калий образуют соли со всеми кислотами. Соли натрия и калия очень похожи по химическим свойствам. Характерная особенность этих солей – хорошая растворимость в воде, поэтому доступных качественных реакций на ионы этих элементов нет. Наличие в соединении даже ничтожно малого количества ионов натрия или калия определяют путем внесения этого соединения в бесцветное пламя: в случае натрия пламя окрашивается в желтый цвет, а в случае калия – в розово-фиолетовый. Натрий и калий образует средние, кислые, двойные и комплексные соли. Большинство средних солей натрия и калия – термически устойчивые вещества и разлагаются только при очень высоких температурах. При умеренном нагревании разлагаются только соли галогенсодержащих оксокислот, нитраты и некоторые другие соединения:
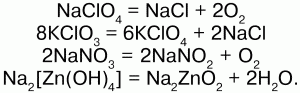
Кислые соли менее устойчивы, при нагревании все они разлагаются:
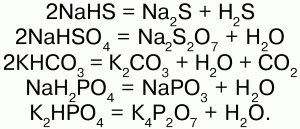
Основных солей эти элементы не образуют.
Из солей наибольшее значение имеет хлорид натрия – NaCl – поваренная соль. Это необходимая составная часть пищи, консервант, сырье для химической промышленности. Из него получают гидроксид натрия, питьевую соду (NaHCO3), соду (Na2CO3) и многие другие соединения натрия. Многие соли натрия образуют кристаллогидраты. Na2S2O3?Н2О – тиосульфат натрия, соответствующий тиосерной кислоте Н2S2O3, применяется в фотографии, для фиксации проявленных бумаг. Na2SO4?10H2O – десятиводный сульфат натрия, глауберова соль, используется в сульфатном способе получения соды и в производстве стекла. Na2CO3?10H2O – карбонат натрия или кальцинированная сода применяется в стекольной, мыловаренной, целлюлозно-бумажной, текстильной, нефтяной, химической промышленностях, а также в быту. NaNO3 – нитрат натрия, натриевая или чилийская селитра – используется как минеральное удобрение. Соли калия – необходимые минеральные удобрения. Na2SiO3 – силикат натрия – используется в производстве стекла. Соли калия выделяются из раствора в основном без кристаллизационной воды. К2CO3 – карбонат калия или поташ – используется в производстве мыла, в производстве тугоплавкого стекла, в фотографии. КNO3 – карбонат калия или калиевая селитра – применяется при изготовлении черного пороха. КCl – хлорид калия – применяется в качестве удобрения. Многие соли калия встречаются в природе: КCl?MgCl?6Н2О – карналлит; КCl?NaCl – сильвинит. Соли К содержатся в квасцах.
