
- •1. Материя и ее движение
- •2 Вещества и их изменение. Предмет неорганической химии
- •3. Закон сохранения массы. Основное содержание атомно-молекулярного учения
- •4. Эквивалент. Закон эквивалентности. Важнейшие классы и номенклатура неорганических веществ
- •5. Периодическая система элементов д.И. Менделеева
- •6. Теория химического строения
- •7. Общая характеристика p-, s-, d-элементов
- •8. Ковалентная связь. Метод валентных связей
- •9. Неполярная и полярная ковалентные связи
- •10. Многоцентровые связи
- •11. Ионная связь
- •12. Водородная связь
- •13. Превращение энергии при химических реакциях
- •14. Цепные реакции
- •15. Общие свойства неметаллов
- •16. Водород
- •17. Вода
- •18. Перекись водорода
- •19. Общая характеристика подгруппы галогенов
- •20. Хлор. Хлороводород и соляная кислота
- •21. Краткие сведения о фторе, броме и йоде
- •22. Общая характеристика подгруппы кислорода
- •23. Кислород и его свойства
- •24. Озон и его свойства
- •25. Сера и ее свойства
- •26. Сероводород и сульфиды
- •27. Свойства серной кислоты и ее практическое значение
- •28. Азот. Сигма– и пи-связи
- •29. Общая характеристика подгруппы азота
- •30. Аммиак
- •31. Соли аммония
- •32. Оксиды азота
- •33. Азотная кислота
- •34. Фосфор
- •35. Аллотропные модификации фосфора
- •36. Оксиды фосфора и фосфорные кислоты
- •37. Минеральные удобрения
- •38. Углерод и его свойства
- •39. Аллотропные модификации углерода
- •40. Оксиды углерода. Угольная кислота
- •41. Кремний и его свойства
- •42. Понятие коллоидных растворов
- •43. Соли кремниевой кислоты
- •44. Получение цемента и керамики
- •45. Физические свойства металлов
- •46. Химические свойства металлов
- •47. Металлы и сплавы в технике
- •48. Основные способы получения металлов
- •49. Коррозия металлов
- •50. Защита металлов от коррозии
- •51. Общая характеристика подгруппы лития
- •52. Натрий и калий
- •53. Едкие щелочи
- •54. Соли натрия и калия
- •55. Общая характеристика подгруппы бериллия
- •56. Кальций
- •57. Оксид и гидроксид кальция
- •58. Жесткость воды и способы ее устранения
- •59. Общая характеристика подгруппы бора
- •60. Алюминий. Применение алюминия и его сплавов
- •61. Оксид и гидроксид алюминия
- •62. Общая характеристика подгруппы хрома
- •63. Хром
- •64. Оксиды и гидроксиды хрома
- •65. Хроматы и дихроматы
- •66. Общая характеристика семейства железа
- •67. Железо
- •68. Соединения железа
- •69. Доменный процесс
- •70. Чугун и стали
- •71. Тяжелая вода
- •72. Соли соляной кислоты
37. Минеральные удобрения
Минеральные удобрения – неорганические вещества, в основном соли, включающие в себя необходимые для растений элементы питания и используемые для повышения плодородия почвы. Бывают простые (азотные, фосфорные, калийные, микроудобрения) и комплексные.
Простые (односторонние) удобрения содержат один главный питательный элемент – азотные удобрения (аммиачная селитра), фосфорные удобрения (простой и двойной суперфосфаты), калийные удобрения (КСl) и др.
Комплексные (многосторонние) удобрения содержат два или три главных питательных элемента и по их числу называются двойными (азотно-фосфорные, фосфорно-калийные и др.) либо тройными или полными (например, азотно-фосфорно-калийные).
Сложными называются комплексные удобрения, полученные в результате взаимодействия исходных неорганических солей, кристаллизацией или сплавлением основных компонентов, смешением простых и сложных удобрений.
В зависимости от агрегатного состояния минеральные удобрения бывают:
1) жидкие;
2) твердые;
3) порошковидные (размер частиц < 1 мм);
4) кристаллические (> 0,5 мм);
5) гранулированные (1–4 мм).
По концентрации действующих веществ минеральные удобрения подразделяются на:
1) низкоконцентрированные (до 25 %);
2) концентрированные (до 60 %);
3) высококонцентрированные (более 60 %).
Производство минеральных удобрений – важная отрасль химической промышленности. Наиболее важными минеральными удобрениями считаются фосфорные (суперфосфат, двойной суперфосфат, преципитат).
Суперфосфат получают из размолотого фосфорита, смешивая его с серной кислотой, и непрерывно перемешивают:
![]()
Суперфосфат легкорастворим в воде.
Двойной суперфосфат получают в результате разложения природного фосфата под воздействием фосфорной кислоты:
![]()
В этом удобрении отсутствует сульфат кальция, упрощая внесение удобрения в почву.
Преципитат – фосфорное удобрение, компонентом которого является гидрофосфат кальция.
Указанные выше минеральные удобрения являются простыми. Сложные минеральные удобрения более перспективны.
Аммофос получается в результате взаимодействия фосфорной кислоты и аммиака – NH4H2PO4 или (NH4)2H2PO4.
Нитрофоска получается при сплавлении гидрофосфата аммония, нитрата аммония и хлорида (сульфата) натрия.
38. Углерод и его свойства
Углерод (С) – типичный неметалл; в периодической системе находится в 2-м периоде IV группе, главной подгруппе. Порядковый номер 6, Ar = 12,011 а.е.м., заряд ядра +6. Физические свойства: углерод образует множество аллотропных модификаций: алмаз – одно из самых твердых веществ, графит, уголь, сажа.
Химические свойства: электронная конфигурация: 1s22s22p2. На электронной оболочке атома – 6 электронов; на внешнем валентном уровне – 4 электрона. Наиболее характерные степени окисления: +4, +2 – в неорганических соединениях, – 4, -2 – в органических. Углерод в любом гибридном состоянии способен использовать все свои валентные электроны и орбитали. У 4-валентного углерода нет неподеленных электронных пар и нет свободных орбиталей – углерод химически относительно устойчив. Характерно несколько типов гибридизации: sp, sp2, sp3. При низких температурах углерод инертен, но при нагревании его активность возрастает. Углерод – хороший восстановитель, но соединяясь с металлами и образуя карбиды, он выступает окислителем:

Углерод (кокс) вступает в реакции с оксидами металлов:
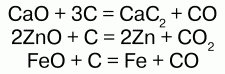

Таким образом выплавляют металл из руды. При очень высоких температурах углерод реагирует со многими неметаллами. Огромное количество органических соединений он образует с водородом – углеводороды. В присутствии никеля (Ni) углерод, реагируя с водородом, образует предельный углеводород – метан: С + Н2 = СН4.
При взаимодействии с серой образует сероуглерод: С + 2S2 = СS2.
При температуре электрической дуги углерод соединяется с азотом, образуя ядовитый газ дициан: 2С + N2 = С2N2?.
В соединении с водородом дициан образует синильную кислоту – НСN. С галогенами углерод реагирует в зависимости от их химической активности, образуя галогениды. На холоде реагирует со фтором: С + 2F2 = СF2.
При 2000 °C в электропечи углерод соединяется с кремнием, образуя карборунд: Si + C = SiC.
Нахождение в природе: свободный углерод встречается в виде алмаза и графита. В виде соединений углерод находится в составе минералов: мела, мрамора, известняка – СаСО3, доломита – MgCO3?CaCO3; гидрокарбонатов – Mg(НCO3)2 и Са(НCO3)2, СО2 входит в состав воздуха; углерод является главной составной частью природных органических соединений – газа, нефти, каменного угля, торфа, входит в состав органических веществ, белков, жиров, углеводов, аминокислот, входящих в состав живых организмов.
