
- •19. Основы сварочного производства
- •19.1. Общие сведения о сварке
- •19.2. Основы ручной дуговой сварки
- •19.3. Устойчивость горения дуги.
- •19.4. Способы регулирования режимов сварки у источников питания.
- •19.5. Источники питания переменного тока.
- •19.6. Источники питания постоянного тока.
- •19.7. Особенности металлургических процессов при сварке.
- •19.8. Основные реакции в зоне сварки.
- •19.10. Электроды и сварочная присадочная проволока
- •19.6. Автоматическая дуговая сварка под флюсом
- •19.7. Электрошлаковая сварка
- •20. Технология сварочного производства
- •20.1. Газовая сварка
- •20.2. Способы сварки давлением
- •20.3. Особенности технологии сварки стали, чугуна и цветных металлов
- •20.5. Дефекты и причины их образования в сварных соединениях
- •21. Основы обработки металлов резанием
- •21.1. Общие сведения о процессе резания металлов
- •21.2. Виды заготовок и припуск на обработку
- •21.3. Рабочие, установочные и вспомогательные движения в металлорежущих станках
- •Конструктивные элементы резца и его геометрические параметры
- •21.4. Точность изготовления деталей машин и качество обработанной поверхности
- •22. Металлорежущие станки и методы обработки заготовок
- •22.1 Классификация металлорежущих станков
- •22.2. Обработка заготовок на станках токарной группы
- •22.3 Обработка заготовок нa сверлильных и расточных станках
- •22.4. Обработка заготовок на фрезерных станках
- •22.6.Физико-химические и электрофизические способы обработки
- •23. Технология производства пластических масс
- •23.1. Пластические массы. Классификация
- •23.2. Технология производства изделий из пластмасс
- •23.3. Технология производства резиновых технических изделий
- •24. Дисперсные системы. Порошковая металлургия
- •24.1. Введение
- •24.2. Свойства малых частиц
- •24.3. Коагуляция частиц
- •24.4. Механические методы получения порошков
- •24.5. Диспергирование расплавов
- •24.6. Физико-химические методы получения порошков
- •24.7. Формирование и спекание порошков
- •24.8. Свойства порошковых материалов
- •25. Контроль качества материалов
- •25.1. Общие положения
- •25.2. Приборы и инструменты для визуального и измерительного контроля
- •25.3. Проведение визуального и измерительного контроля
24.3. Коагуляция частиц
Высокоразвитая поверхность дисперсных коллоидных систем обусловливает большой избыток поверхностной энергии, что делает эти системы термодинамически неустойчивыми и стремящимися к уменьшению межфазной энергии. Это вызывает нарушение агрегатной устойчивости, уменьшение степени дисперсности и объединение частиц под действием молекулярных сил.
Укрупнение частиц может происходить двумя путями:
изотермической перегонкой;
коагуляцией.
Перегонка - перенос вещества от мелких частиц к крупным за счет разности химических потенциалов частиц (µмелк) (µкрупн) - эффект Кельвина.
Коагуляция - слипание частиц. Слияние частиц иногда именуют коалесценцией.
Пептизация - распад коагулянта.
Изотермическая перегонка может происходить практически во всех дисперсных системах за счет разности химических потенциалов, что создает движущую силу переноса вещества:
µ = µмелк - µкрупн.
Этот процесс ведет к постепенному исчезновению мелких частиц.
Различают три стадии перегонки:
- растворение или испарение мелких частиц;
- перенос вещества от мелких к крупным частицам;
- рост крупных частиц;
Скорость перегонки лимитируется скоростью массопереноса в дисперсионной среде, которая согласно закону Фика, зависит от градиента концентраций или давлений (т.е. разности химических потенциалов.) В свою очередь, градиент концентраций (давлений) определяется различием размеров частиц, между которыми происходит массоперенос.
Количественная теория коагуляции была разработана польским ученым М.Смолуховским.
Согласно представлениям Смолуховского, при коагуляции происходит взаимодействие только между двумя частицами, а вероятность столкновения большого числа частиц мала.
Таким образом, слипаются частицы одиночные, образуя двойные, одиночные с двойными, двойные друг с другом и т.д. Такое представление позволяет формально применить теорию бимолекулярных химических реакций.
В связи с тем, что в процессе коагуляции число свободных частиц уменьшается, то согласно уравнению скорости бимолекулярных реакций
- dn/d = Кп2, (18)
где п - суммарная концентрация частиц разных размеров в данный момент, К - константа скорости коагуляции.
![]() ,
(19)
,
(19)
К0 - 8DRP для сферических частиц, Р - сферический фактор, D - коэффициент диффузии, R - эффективный радиус частиц (R 2r), К - постоянная Больцмана, U - потенциальный барьер (энергия активации) для слипания частиц.
Чтобы определить число частиц, остающихся после коагуляции к некоторому моменту времени , необходимо проинтегрировать выражение (18) от n0 при = 0 до n при
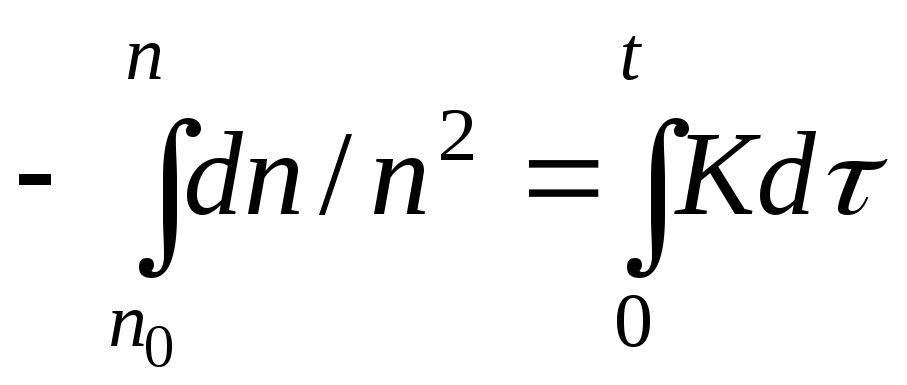 .
(20)
.
(20)
Тогда получим
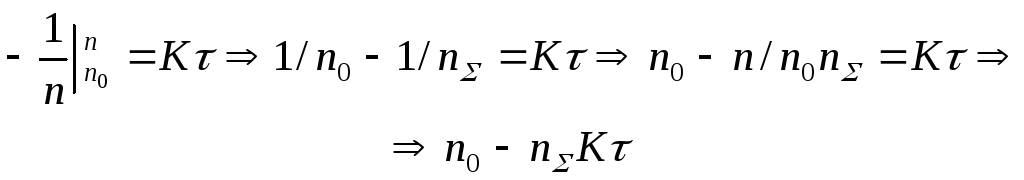
откуда
![]() .
(21)
.
(21)
Для
определения константы скорости коагуляции
Смолуховский ввел понятие периода
половинной коагуляции
- времени, в течение которого общая
концентрация частиц уменьшается до
половины от начальных, т.е. при
=
n
=
![]() п.
Тогда из (25.21) следует
п.
Тогда из (25.21) следует ![]() ,
,![]() (22)
(22)
и ![]() .
(23)
.
(23)
Выражение (23) для концентрации частиц через время коагуляции в теории Смолуховского широко используется для обработки экспериментальных данных,
Различают быструю и медленную коагуляции. При быстрой коагуляции все столкновения приводят к слипанию частиц.
В этом случае U = 0 (нет потенциального барьера и Р=1. Тогда из (19) имеем
![]() .
.
Для медленной коагуляции
U
0, Р
1
и ![]() .
.
Рассмотренные процессы коагуляции дисперсных частиц подтверждены многочисленными экспериментами и наблюдениями:
- при объединении аэрозольных частиц (твердых и жидких) в атмосфере, сопровождающемся образованием облаков,
- при получение связующих материалов в строительном деле,
- при образовании тонких пленок,
- в коллоидной химии,
- при объединения кластеров-зародышей в переохлажденном расплаве,
- при спекании порошков.
Порошковая металлургия позволяет создавать сплавы любого состава из металлических или смеси металлических и неметаллических порошков, которые практически взаимно не растворяются при плавлении или могут разлагаться при высоких температурах. Например, железо и свинец, алюминий и никель, медь и графит, металлы и оксиды, металлы и бориды и др.
Производство изделий из вольфрама и тантала, которые обладают высокой температурой плавления (3387С и 2997С соответственно), осуществляется преимущественно методами порошковой металлургии. Порошковая металлургия позволяет изготовлять некоторые конструкционные детали (кулачки, втулки и др.) без последующей механической обработки.
Изделия из металлокерамических сплавов нашли применение для металлорежущего инструмента, для волок и фильер при производстве проволоки для подшипников скольжения и тормозных устройств, для постоянных магнитов, электроконтактов, нагревателей электропечей и др.
К недостаткам порошковой металлургии следует отнести высокую стоимость порошков, значительные затраты на изготовление пресс-форм и другой оснастки, низкие показатели вязкости и пластичности порошковых материалов.
