
- •Кафедра «Теплоэнергетика»
- •Краткий курс лекций
- •5В071700 - «Теплоэнергетика» направление – «Бакалавриат»
- •Лекция № 1. Тема: основные определения термодинамики.
- •Предмет и метод термодинамики
- •Принцип построения термодинамики
- •Основные понятия и определения термодинамики
- •Лекция № 2. Тема: параметры состояния тела.
- •В настоящее время применяют различные температурные шкалы-Цельсия. Реомюра, Фаренгейта, Ренкина, соотношения между которыми приводятся в таблице 2.3
- •Лекция № 3. Тема: идеальный газ. Основные газовые законы.
- •Лекция № 4. Тема: смеси идеальных газов.
- •Лекция № 5. Тема: теплоемкость газов.
- •Теплоемкость газовой смеси
- •Лекция № 6. Тема: первый закон термодинамики. Внутренняя энергия
- •Теплота
- •Первый закон термодинамики
- •Закон сохранения и превращения энергии :
- •Формулировка и уравнение первого закона термодинамики
- •Энтальпия газов
- •Лекция № 7 Тема: основные термодинамические процессы. Основными термодинамическими процессами являются:
- •Метод исследования процессов состоит в следующем:
- •Политропный процесс ()
- •Тема: второй закон термодинамики.
- •Энтропия идеального газа
- •Тепловая диаграмма (ts-диаграмма)
- •Лекция № 9 Тема: водяной пар. Процессы водяного пара. Уравнение состояния реального газа
- •Водяной пар
- •Сухой насыщенный пар
- •Влажный насыщенный пар
- •Перегретый пар
- •Энтропия пара
- •Лекция № 10 Тема: влажный воздух.
- •Изображение адиабатного процесса
- •Изобарный процесс водяного пара
- •Цикл Карно. Теорема Карно
- •Теорема Карно
- •Лекция № 12. Уравнение первого закона термодинамики для потока. Истечение газов и паров. Дросселирование.
- •Лекция № 13 Тема: циклы поршневых компрессоров, двс, гту.
- •Теоретическая мощность двигателя для привода компрессора
- •Теоретические циклы поршневых двигателей внутреннего сгорания
- •Циклы газотурбинных установок
- •Лекция № 14
- •1 Паросиловой цикл Ренкина
- •2 Теплофикационный цикл
- •3Регенеративный цикл
- •4 Цикл воздушной холодильной установки
- •Лекция № 15
Перегретый пар
Перегретый пар имеет более высокую температуру tпо сравнению с температуройtнсухого насыщенного пара того же давления. Следовательно, перегретый пар определённого давления может иметь различные температуры.
Для характеристики перегретого пара необходимо знать два его параметра, например давление и температуру.
Разность температур
перегретого и насыщенного пара того же
давления
![]() называютперегревом пара.
называютперегревом пара.
Важным является определение количества теплоты, затрачиваемой на отдельные стадии процесса парообразования и изменения внутренней энергии.
Теплота жидкости– это количество теплоты, затраченной для подогрева жидкости от 00С до температуры кипения при постоянном давлении. Её можно определить как разность энтальпий жидкости в состоянии кипения и жидкости при том же давлении и 00С
 (11)
(11)
Так как
 при невысоких давлениях можно считать
равным нулю, то
при невысоких давлениях можно считать
равным нулю, то
![]() (12)
(12)
Внутренняя энергия жидкости равна энтальпии жидкости
![]() ,
(13)
,
(13)
где значения i’, а следовательно иu’ приводятся в таблицах насыщенного пара.
Теплота парообразования(r) – это количество теплоты, необходимое для перевода 1кг кипящей жидкости в сухой насыщенный пар при постоянном давлении. Это количество теплоты расходуется на изменение внутренней энергии, связанное с преодолением сил сцепления (d) между молекулами жидкости, и на работу расширения (ψ).
Величина (d) – внутренняя теплота парообразования.
Величина (ψ) – внешняя теплота парообразования.
![]() (14)
(14)
![]() (15)
(15)
Значения rприводятся в таблицах насыщенного пара.
Теплота перегрева– количество теплоты, необходимое для перевода 1кг сухого насыщенного пара в перегретый при постоянном давлении.
Значения энтальпии перегретого пара приводятся в таблицах воды и перегретого водяного пара.
Энтропия пара
Энтропия водяного пара отсчитывается от условного нуля, в качестве которого принимают энтропия воды при 0,010С и при давлении насыщения, соответствующем этой температуре 0,0006108МПа.
Энтропия жидкостиопределяется по формуле
![]() ,
(16)
,
(16)
где 4,19 - теплоёмкость воды, кДж/(кг∙К);
Тн– температура насыщения, К.
Если жидкость подогревается не до температуры кипения, а до произвольной температуры Т, то под Тнв формуле (16) следует понимать эту произвольную температуру.
Энтропия сухого насыщенного пара s”определяется
![]() ,
(17)
,
(17)
где r– теплота парообразования.
Энтропия влажного насыщенного параопределяется
![]() (18)
(18)
![]() ,
(19)
,
(19)
где х – степень сухости пара.
Энтропия s’
иs” приводится в таблицах
насыщенного пара, а![]() можно получить из этих же таблиц как
разностьs”-s’.
можно получить из этих же таблиц как
разностьs”-s’.
TS-диаграмма для водяного пара
Важное значение в теплотехнических расчётах имеют диаграммы TSиis.

Рисунок 2 - TS-диаграмма для водяного пара
Кривая О1К – нижняя пограничная кривая (х=0), кривая КВ1– верхняя пограничная кривая (х=1).Точка О1соответствует температуре 273К (00С), точка К – критическому состоянию пара.
Нижняя пограничная кривая совпадает с изобарами жидкости, поэтому кривая О1К одновременно изображает процесс подогрева жидкости при постоянном давлении от 00С до температуры кипения.
Линии АВ представляют собой одновременно изобары и изотермы и изображают процесс парообразования.
Линии ВС представляют собой изобары и изображают процесс перегрева пара. Вся область жидкости в TS-диаграмме совпадает с кривой О1К. между кривыми О1К и КВ1расположена область влажного насыщенного пара. ВTS-диаграмме наносятся также кривые одинаковой степени сухости параNP,LMи другие. Так как площадиTS-диаграммы, ограниченные кривой процесса, крайними ординатами и осью абсцисс, измеряют в определённом масштабе количества теплоты, подведённой к рабочему телу при постоянном давлении, то площадь ОО1А1Gсоответствует энтальпии жидкостиi’, площадь А1В1FG– теплоте парообразования (r) и площадь В1С1DF– теплоте перегрева. Вся площадь ОО1А1В1С1Dсоответствует энтальпии перегретого параi.
is-диаграмма для водяного пара
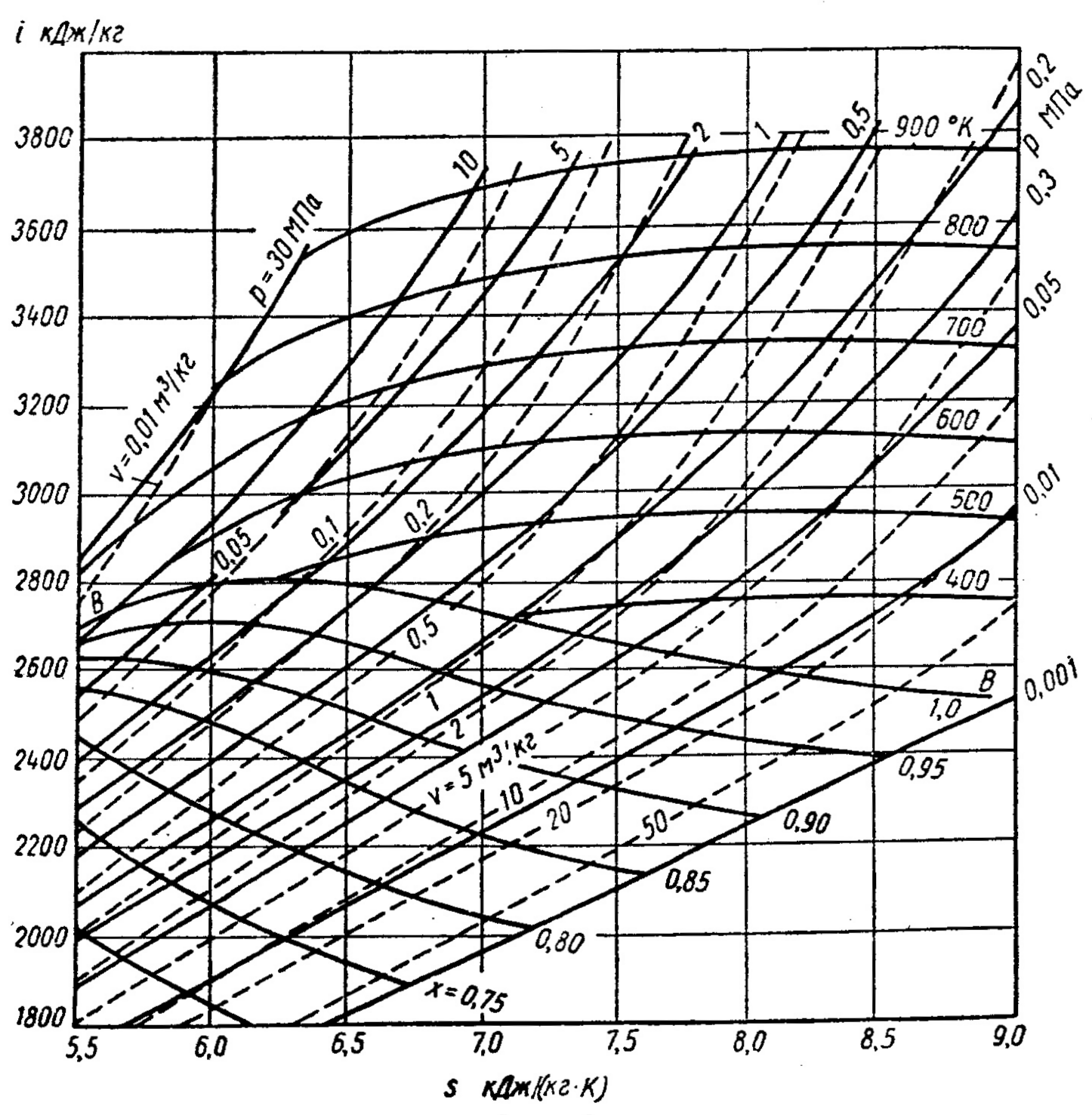
Рисунок 3 - is-диаграмма для водяного пара
На ней нанесены изохоры (пунктирные кривые), изобары, изотермы и линии равной сухости пара. Линия ВВ – верхняя пограничная кривая. Ниже её расположена область влажного насыщенного пара, выше её – область перегретого пара. Изобары в области насыщенного пара – прямые линии, являющиеся одновременно изотермами. При переходе в область перегретого пара изобары и изотермы разделяются, и каждая из них представляет собой отдельную кривую. is-диаграмма позволяет быстро определить параметры пара с достаточной точностью, даёт возможность определять энтальпию водяного пара и разности энтальпий в виде отрезков, наглядно изображает адиабатный процесс, имеющий большое значение при изучении паровых двигателей.
