
- •Основы гидрогеологии
- •130101.65 «Прикладная геология»
- •Введение
- •1. Вода в геосферах Земли
- •1.1. Надземная гидросфера
- •1.1.1. Влажность воздуха
- •1.1.2.Испарение и Транспирация
- •1.1.3.Атмосферные осадки
- •1.1.4.Виды воды в атмосфере
- •1.2. Наземная гидросфера
- •1.2.1. Гидрологический круговорот воды
- •1.2.2. Малый и большой круговороты воды
- •1.2.3. Поверхностный сток
- •1.2.4.Подземный сток
- •1.3. Подземная гидросфера
- •2. Гидрогеологические структуры структурные типы подземных вод
- •3. Подземные водные резервуары
- •3.1.Гидрогеологический цикл и его этапы
- •4. Проблема формирования подземных вод и ее сущность
- •4.1.Формирование ресурсов подземных вод
- •4.1.1. Процессы формирования состава подземных вод
- •5. Гидрогеологическая стратификация
- •5.1. Гидрогеологическая стратификация зсмб
- •6. Виды воды в горных породах
- •Классификация видов воды
- •7. Основные виды движения подземных вод
- •7.1.Элементы фильтрационного потока. Закон Дарси
- •7.1.1. Методы определения коэффициента фильтрации
- •7.1.2. Водопроводимость
- •7.2. Особенности движения подземных вод повышенной минерализации
- •7.3. Установившееся и неустановившееся движение
- •8. Гидрогеотермия
- •8.1. Гидрогеотермический режим земной коры
- •8.1.1. Виды теплопереноса
- •8.1.2. Геотермические зоны земной коры
- •8.1.3. Геотемпературное поле
- •8.1.4. Практическое применение геотермических методов в гидрогеологии
- •9. Свойства и состав природных вод
- •9.1. Распространение воды на Земле и уникальность ее свойств
- •9.1.1. Строение и структура воды
- •9.1.2. Изотопный состав воды
- •9.1.3. Физические свойства воды
- •9.1.4. Химический состав воды
- •9.1.5. Макрокомпоненты
- •9.1.6. Классификация вод по величине минерализации
- •9.1.7. Микрокомпоненты
- •9.1.8. Ионное произведение и активная реакция воды. РН.
- •9.1.9. Окислительно-восстановительный потенциал воды
- •9.1.10. Типы химического анализа при гидрогеологических исследованиях
- •9.1.11. Бактериологический состав воды
- •9.1.12. Газовый состав воды
- •9.1.13. Жесткость воды
- •9.1.14. Агрессивность воды
- •10. Подземные воды криолитозоны
- •Надмерзлотные воды
- •10.1.Надмерзлотные воды деятельного слоя
- •10.1.1.Межмерзлотные воды
- •10.1.2.Подмерзлотные воды
- •11. Основы палеогидрогеологии
- •12. Основы нефтегазовой гидрогеологии
- •12.1. Теоретические основы нефтегазовой гидрогеологии
- •12.1.1. Растворенные углеводородные газы
- •12.1.2. Воднорастворенные органические вещества (вров)
- •12.2. Гидрогеологические условия, благоприятные для сохранения и разрушения залежей нефти и газа
- •13. Нефтегазопромысловая гидрогеология
- •Основные понятия о залежах нефти и газа
- •Основные категории и группы скважин при бурении на
- •Промысловая классификация подземных вод
- •Воды здесь классифицируются по их пространственно-геологическому отношению к залежам, которые служат объектами разработки.
- •Промысловая классификация подземных вод нефтяных и газовых месторождений
- •Движение контурных вод при эксплуатации
- •Режим нефтегазоводоносных пластов
- •Гидрогеологические условия проявления различных режимов нефтегазоносных пластов
- •Гидрогеологические исследования Гидрогеологические исследования в процессе бурения и испытания опорных, разведочных и эксплуатационных скважин
- •Гидрогеологические исследования в процессе разведки и разработки нефтяных и газовых месторождений
- •Требования к технологии и технике закачки рабочих агентов в пласт
- •Показатели и нормы качества воды
9.1.8. Ионное произведение и активная реакция воды. РН.
Как известно, вода диссоциирует по уравнению:
Н2О↔Н+ + ОН-
Однако степень диссоциации воды очень мала. При температуре = 220С из 55,51 г/молей воды, содержащихся в 1л (1000:18,016 = 55,51) только 10-7г/моль находятся в виде ионов. На основании закона действующих масс константа диссоциации воды (при температуре 220С)
К Н2О = [H+][ ОH] = 10-7·10-7/55,51
[H2О]
Поскольку 55,51>>10-7, изменение степени ионизации воды даже в сотни тысяч раз практически не изменит величины [ H2О], что позволяет считать ее постоянной (константа диссоциации воды-Кв).
Тогда, Кв = [H+][ ОH] = 10-7·10-7 = 10-14
Это постоянное (для данной температуры) произведение называется ионным произведением воды. Концентрацию ионов водорода и гидроксила выражают в виде отрицательного логарифма - рН и рОН. рН = -lg [H+] рОН = -lg [ОH-]
- lgН = рН = 7. В чистой воде имеется равенство ионов Н+ и ОH- и вода является нейтральной. Но вода, содержащая растворенные вещества, имеет кислую или щелочную реакцию. При кислой реакции [H+] > [ОH-], а при щелочной - [H+] < [ОH-].
рН+рОН = -lg10-14 = 14. Значит, при нейтральной реакции при t = 220С
рН = рОН = 14/2= 7
рН >7 – щелочная рОН < 7
рН < 7 –кислая рОН > 7
При температуре кипения (1000С) [H+][ ОH] = 10-6·10-6 = 10-12
Нейтральная вода при рН = 6
При надкритической температуре (4000С) - нейтральная вода при рН=4,5.
9.1.9. Окислительно-восстановительный потенциал воды
Окислительно-восстановительные реакции, связаны с потерей или присоединением электронов:
Fe2+ ↔ Fe3++e или Fe2+ - e = Fe3+
Окислительно-восстановительная способность системы определяется окислительно-восстановительным потенциалом (ОВП), который замеряется при сравнении с индифферентным (золотым или платиновым) электродом и выражается следующим уравнением:

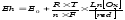
где, Еh – потенциал индифферентного электрода, отнесенный к нормальному водородному полуэлементу, Е0 – нормальный потенциал системы – постоянная, характеризующая данную ОКВ – систему, значение которой замеряется при концентрациях окисленной и восстановленной части системы, соответствующей 1 молю каждая: R – газовая постоянная – 8,313 дж/град, Т – абсолютная температура, n – число электронов, участвующих в реакции, F – заряд грамм – иона, равный 96500 к, [Ox] и [red] – молярные концентрации окисленной и восстановленной формы
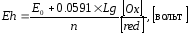

Определяют ОКВ – потенциал электрометрическим измерением с помощью компенсационной схемы разности потенциалов электрохимической ячейки: платиновый электрод, погруженный в исследуемую воду, каломельный электрод. Последний электрод имеет постоянный потенциал, зависящий только от температуры. Обычно применяют чувствительный приборы – потенциометры с ламповыми усилителями, выпускаемыми нашей промышленностью. Для полевых условий – рН – метры ППМ-01-М. Потенциал – задающими в водах обычно являются элементы с переменной валентностью при концентрации не менее 1·10-5 моль/л. Это Fe,Mn,H2S, органически вещества и др.
9.1.10. Типы химического анализа при гидрогеологических исследованиях
Химический анализ природных вод проводится при решении следующих задач:
1) изучение закономерностей формирования и распространения природных вод различного состава;
2) поиски месторождений полезных ископаемых (нефти и газа, металлов, солей и др.) гидрогеохимическим методом;
3) оценка природных вод как химического сырья для получения J, Br, B, Cu, Ba и др.;
4) поиски месторождений минеральных вод;
5) оценка качества воды для питьевого, технического, сельскохозяйственного и других видов использования;
6) оценка условий загрязнения.
Для общей характеристики ионно-солевого состава природных вод применяют три типа анализа воды – полевой, сокращенный и полный.
Полевой анализ производится в полевых условиях с помощью походных лабораторий различных конструкций. Определение обычно делается массово для предварительной оценки состава природных вод изучаемого района. При полевом анализе проводится определение физических свойств Сl, SO4, NO3, HCO3, CO3, Ca, Mg, Fe+2, Fe+3, СО2, Н2S, О2.
Вычисляются Na+K, Mg или Ca, карбонатная жесткость, общая минерализация.
Сокращенный анализ проводится более точными методами в стационарной или полустационарной лаборатории. Он позволяет произвести контроль анализа. В комплексе сокращенного анализа в дополнение к перечисленному для полевого входит определение NH4 ,NO2, H2SiO3, агрессивная СО2, жесткость общая.
Полный анализ производится наиболее точными методами в стационарной лаборатории. Кроме компонентов, перечисленных в комплексе сокращенного анализа он предусматривает раздельное определение Na и K, окисляемость воды, а при изучении артезианских вод - J, Br, B.
При проведении специальных исследований проводится определение состава спонтанных и растворенных газов: Н2S, СО2, О2, СН4, N2++ редк., Аr + Кr + Хe, Нe, + Ne и тяжелые углеводороды.
При постановке гидрогеохимических исследований необходимо определять большой комплекс микрокомпонентов: Li, Rb, Cr, Ba, As, Sb, Pb, Zn, Cd, Ni, Co, U, R, органические вещества и др.
Для их определения разработаны и разрабатываются различные методы: экстрационно-колориметрический, спектральный, полярографический, флуориметрический, пламенно-фотометрический и др.
Очень низкое содержание многих микрокомпонентов в водах заставляет применять предварительное концентрирование веществ, т.е. получать водные концентраты, а затем уже определять в них соответствующие элементы.
В настоящее время широко применяются три метода концентрирования:
1) выпаривание до сухого остатка. Метод трудоемок и ограничен водами с минерализацией 1-2 г/л;
2) метод соосаждения с гидратом гидроокиси алюминия (метод ТПИ). Он позволяет концентрировать микрокомпоненты почти в 20000 раз и определять свыше 20 химических элементов.
Второй метод наиболее широко применяется в Сибири и на Дальнем Востоке;
3) метод соосаждения с сульфидом кадмия (Витр-ЛТИ). Степень концентрации здесь меньше и составляет 3000-4000.
Методы, перечисленные выше, относятся к групповому концентрированию. Существуют и методы индивидуального концентрирования отдельных компонентов (элюация на угле, адсорбция на ионно-обменных смолах и др.).
