
- •Розділ 5. Структура, функції та метаболізм ліпідів
- •5.1. Біологічні функції та класифікація ліпідів
- •5.2. Структурна організація біомембран
- •5.3. Циркуляторний транспорт і депонування ліпідів у жировій тканині
- •5.4. Катаболізм тріацилгліцеролів і його регуляція
- •5.5. Біосинтез тріацилгліцеролів
- •5.6. Біосинтез фосфоліпідів
- •5.7. Метаболізм сфінголіпідів. Сфінголіпідози
- •5.8. Окиснення жирних кислот
- •5.9. Окиснення гліцеролу
- •5.10. Синтез жирних кислот
- •5.11. Метаболізм кетонових тіл
- •5.12. Метаболізм холестерину
- •5.13. Гіперліпемії
- •5.14. Стеатоз
- •5.15. Ожиріння
5.4. Катаболізм тріацилгліцеролів і його регуляція
Основним ендогенним джерелом жирних кислот є резервний жир. Прийнято вважати, що тригліцериди жирових депо виконують таку саму роль, як глікоген у печінці при обміні вуглеводів, а жирні кислоти нагадують собою глюкозу. При фізичній роботі та інших станах організму, які потребують затрат енергії, використання тріацилгліцеролів збільшується. Оскільки джерелом енергії можуть служити жирні кислоти, то тригліцериди гідролізують під дією тканинних ліпаз, вільні жирні кислоти переходять у плазму крові, де розносяться до різних органів і тканин.
Основне місце локалізації резервних тріацилгліцеролів в організмі - адипоцити жирової тканини, яка містить до 65 % нейтральних жирів.
Розпад тріацилгліцеролів у тканинах здійснюється тканинною тригліцеридліпазою, яка гідролізує їх на гліцерин та вільні жирні кислоти. Є декілька різновидів тканинних ліпаз, які відрізняються насамперед оптимумом рН і локалізацією у клітині. Кисла ліпаза міститься в лізосомах, лужна – у мікросомах, нейтральна - у цитоплазмі. Характерною властивістю тканинної ліпази є чутливість до гормонів, які активують аденілатциклазу, викликають перехід неактивної ліпази тканин в активну форму шляхом фосфорилювання за допомогою протеїнкінази А. Під дією ліпази проходить мобілізація тріацилгліцеролів за схемою поданою на рис. 5.8. Процес називають також тканинним ліполізом.
Рис. 5.8. Схема
катаболізму тріацилгліцеролів
Внутрішньоклітинний ліполіз тріацилгліцеролів здійснюється в декілька стадій, продуктами яких є діацилгліцероли, моноацилгліцероли, гліцерин та вільні жирні кислоти.
Утворені в жировій тканині при гідролізі тріацилгліцеролів гліцерин та жирні кислоти не піддаються окисненню, а надходять у кров і використовуються іншими органами.
Вільні жирні кислоти є субстратами окиснення для клітин багатьох тканин, зокрема міокарда, гладкої мускулатури та інших, крім головного мозку. Після надходження у кров високомолекулярні жирні кислоти транспортуються у зв'язаній з альбуміном молекулярній формі.
5.4.1. Молекулярний механізм регуляції тріацилгліцеролліпази. Гідроліз тріацилгліцеролів у жировій тканині каталізується трьома ліпазами: тріацилгліцерол-, діацилгліцерин- і моноацилгліцеринліпазою. Найменш активна тріацилгліцеролліпаза, яка є регуляторним ферментом. Стимулюється процес гідролізу жирів гормонами - адреналіном, глюкагоном, кортикостероїдами, інсуліном, соматотропіном.
Молекулярною основою регуляції активності тріацилгліцеролліпази є її ковалентна модифікація шляхом оберненого фосфорилювання- дефосфорилювання. Фосфорильофана форма тріацилгліцеролліпази є каталітично активною, дефосфорильована – неактивна (рис. 5.9). Через аденілатциклазну систему адреналін і глюкагон активують тріацилгліцеролліпазу, механізм активації включає синтез цАМФ, активацію протеїнкінази і фосфорилювання ліпази. Інсулін протидіє активації аденілатциклази цими гормонами і тим самим пригнічує ліполіз.
Ф
Рис.
5.9. Каскадний механізм регуляції
тріацилгліцеринліпази

5.4.2. Нейро-гуморальна регуляція ліполізу. Кора головного мозку впливає на жирову тканину через нижчі відділи центральної нервової системи - симпатичну і парасимпатичну або через ендокринні залози. Відомо цілий ряд біохімічних механізмів, що лежать в основі дії гормонів на ліпідний обмін.
Так, негативний емоційний стрес як гострий, так і хронічний, що супроводжується збільшенням секреції катехоламінів у кров’яне русло, може супроводжуватися помітною втратою маси тіла. Жирова тканина іннервується волокнами симпатичної нервової системи і збудження цих волокон супроводжується виділенням норадреналіну безпосередньо в жирову тканину (рис. 5.10).
Рис.
5.10. Гормональна регуляція ліполізу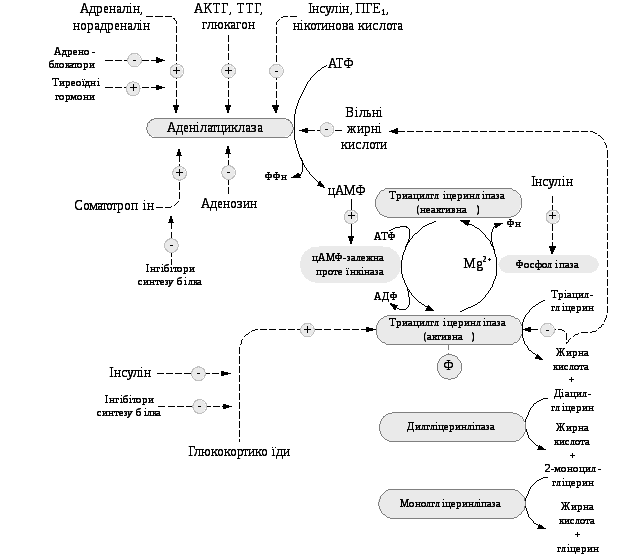
Адреналін та норадреналін – катехоламіни, що активують ліполіз у жировій тканині за рахунок стимуляції цАМФ- залежного каскадного механізму регуляції активності тріацилгліцеролліпази адипоцитів.
Ліполітична дія цих гормонів реалізується практично миттєво за умов фізичного напруження, зниження температури навколишнього середовища та психологічних стресів.
Глюкагон стимулює ліполітичну систему в нервовій тканині за механізмом, подібним до дії катехоламінів, тобто за рахунок підвищення вмісту цАМФ, пов’язаного з активацією аденілатциклази. Метаболічні ефекти катехоламінів та глюкагону призводять до швидкої стимуляції глікогенолізу в печінці і м’язах й ліполізу в жировій тканині, що забезпечує енергетичні потреби організму за умов стресу або голодування.
Інсулін має протилежну дію адреналіну і глюкагону, діє на ліполіз і мобілізацію жирних кислот, гальмує процес ліполізу та вивільнення жирних кислот. Інгібуюча дія інсуліну відносно ліполізу в адипоцитах реалізується за рахунок двох біохімічних механізмів:
а) зменшення концентрації цАМФ, що може бути пов’язаним з активацією фосфодіестерази цАМФ. Оскільки фосфодіестераза відіграє важливу роль у підтримці стаціонарного рівня цАМФ у тканинах, збільшення вмісту інсуліну повинно викликати підвищення активності фосфодіестерази, що у свою чергу призводить до зменшення концентрації цАМФ у клітинах, а отже, і утворення активної форми ліпази.
б) збільшення проникності мембран адипоцитів до глюкози, результатом чого є активація в жировій тканині гліколізу і накопичення продуктів гліколізу діоксіацетонфосфату і та 3- фосфогліцеринальдегіду. Ці метаболіти є попередники при біосинтезі тріацилгліцеролів. Підвищення надходження в адипоцити глюкози під впливом інсуліну переключає метаболізм жирних кислот на використання в синтетичних реакціях і зменшує їх вихід у кров.
Крім цього, інсулін сприяє утворенню тріацилгліцеролів із вуглеводів, що, в цілому, забезпечує відкладання ліпідів у жировій тканині, а також утворення холестерину в інших тканинах. Тироксин і трийодтиронін сприяють окисненню бічного ланцюга холестерину і виведенню його з жовчю в кишечник.
Соматотропін – гормон передньої частки гіпофізу, який також стимулює ліполіз у жировій тканині за умов голодування, але його дія відрізняється від впливу катехоламінів та глюкагону. Соматотропін спричинює підвищення процесів ліполізу за рахунок посилення синтезу відповідних ферментів. Його вплив на ліполіз є повільним, що має значення в адаптації при голодуванні.
Гіпофункція залози призводить до відкладення жиру в організмі, настає гіпофізарне ожиріння. Навпаки, підвищена продукція гормону росту стимулює ліполіз, вміст жирних кислот у плазмі крові збільшується. Доведено, що стимуляція ліполізу гормоном росту блокується інгібіторами синтезу мРНК. Крім цього, відомо, що дія гормону росту на ліполіз характеризується наявністю латентної фази тривалістю біля години. Інші гормони, зокрема тироксин, статеві гормони, також впливають на ліпідний обмін. Наприклад, відомо що видалення статевих залоз (кастрація) викликає у тварин надлишкове відкладення жиру.
