
- •Механизм действия ферментов. Этапы ферментативного катализа.
- •Повышение температуры неоднозначно влияет на активность фермента
- •Ферменты характеризуются высокой специфичностью
- •Изостерическая и аллостерическая регуляция.
- •Аллостерическая регуляция.
- •У аллостерических ферментов особые свойства
- •Две модели объясняют механизмы аллостерии.
- •В основе связывания субстрата - индуцированное взаимодействие.
- •Изменение конформации одной субъединицы индуцирует изменения структуры другой
- •Конкурентные ингибиторы не влияют на Vmax, они понижают Км.
- •Принципы конкурентного торможения находят применение в медицинской практике.
- •Смешанные неконкурентные ингибиторы
- •Кинетика смешанных неконкурентных ингибиторов
- •Неконкурентных ингибиторы неактивны при низких концентрациях субстрата.
- •Торможение продуктом реакции- пример конкурентного торможения.
- •Субстрат может быть ингибитором фермента
- •Регуляция активности с помощью гормонов.
Смешанные неконкурентные ингибиторы
Неконкурентный ингибитор связываясь со специальным центром на ферменте, расположенным вдали от активного центра, вызывает конформационные изменения в активном центре. Это несколько напоминает один из типов конкурентных ингибиторов, но в отличие от этого механизма изменения конформации активного центра не препятствуют связыванию субстрата а тормозит проведение реакции и образование продукта..
Классический неконкурентный ингибитор не оказывает влияния на связывание субстрата. Изменения формы активного центра незначительны, хотя сродство к субстрату все же снижается. Такие ингибиторы часто называются смешанными ингибиторами, поскольку они проявляют свойства конкурентных и неконкурентных типов. Фактически классические неконкурентные ингибиторы встречаются очень редко.
Кинетика смешанных неконкурентных ингибиторов
Фермент может связываться и с субстратом и с ингибитором с образованием комплексов:
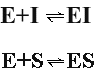
Однако в отличие от конкурентного торможения и субстрат ингибитор способны одновременно связываться с ферментом, образуя тройные комплексы:
Т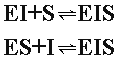 акой
комплекс не способен катализировать
реакцию.
акой
комплекс не способен катализировать
реакцию.
О![]() братите
внимание, что комплекс EIS
может возникать двумя путями, но конечный
результат один и тот же - образуется
неактивный фермент. Ингибитор может
работать одинаково хорошо при низких
концентрациях субстрата, когда большая
часть молекул фермента находится в
форме свободного фермента, и при высоких
концентрациях субстрата, когда фермент
находится в форме ES
комплекса, поскольку ингибитор связывается
одинаково хорошо с обоими из них.
братите
внимание, что комплекс EIS
может возникать двумя путями, но конечный
результат один и тот же - образуется
неактивный фермент. Ингибитор может
работать одинаково хорошо при низких
концентрациях субстрата, когда большая
часть молекул фермента находится в
форме свободного фермента, и при высоких
концентрациях субстрата, когда фермент
находится в форме ES
комплекса, поскольку ингибитор связывается
одинаково хорошо с обоими из них.
Влияние на Km Классический смешанный неконкурентный ингибитор не оказывает влияния на связывание субстрата, сродство фермента к субстрату и следовательно не влияет на Км.
Смешанный ингибитор позволяет субстрату связываться, но снижает его сродство, так что Км повышается.

График Лаинуивера-Берка для неконкурентного классического(слева) и смешанного типов ингибиторов
Влияние на Vmax Неконкурентные и классический и смешанный варианты, тормозят активность при высоких концентрациях субстрата, так что Vmax снижается.
Влияние на Vmax/Km Неконкурентные ингибиторы могут работать при низких концентрациях субстрата так, что Vmax/Km снижается.
Г![]() рафик
Лайнуивера-Берка для типичного
классического смешанного неконкурентного
ингибитора и для смешанного неконкурентного.
На графике для смешанного конкурентного
ингибитора две линии по разному пересекают
1/ [S], указывая на увеличение
Км, хотя на графике для классического
смешанного неконкурентного ингибитора,
значения Km идентичны.
Однако оба графика показывают увеличение
наклона в пересечении на оси 1/V,
демонстрируя, что ингибитор является
эффективным при высоких и низких
концентрациях фермента.
рафик
Лайнуивера-Берка для типичного
классического смешанного неконкурентного
ингибитора и для смешанного неконкурентного.
На графике для смешанного конкурентного
ингибитора две линии по разному пересекают
1/ [S], указывая на увеличение
Км, хотя на графике для классического
смешанного неконкурентного ингибитора,
значения Km идентичны.
Однако оба графика показывают увеличение
наклона в пересечении на оси 1/V,
демонстрируя, что ингибитор является
эффективным при высоких и низких
концентрациях фермента.
Заключение. Смешанные неконкурентные ингибиторы связываются с центром, который является отдаленным от активного центра. Они тормозят активность фермента, вызывая изменения конформации , препятствующие превращению субстрата в продукт. Субстрат и ингибитор способны к связыванию с ферментом одновременно, образуя тройной комплекс. Это означает, что ингибитор не конкурирует с субстратом при высоких концентрациях субстрата и работает одинаково хорошо и при низких и высоких концентрациях субстрата. Правда способность связываться (сродство) с комплексом ингибитор+фермент у субстрата может снижаться, хотя на практике нет особых различий между так называемым смешанным ингибитором и классическим неконкурентным ингибитором.
Неконкурентные ингибиторы не могут связаться со свободным ферментом.
Понятие неконкурентный ингибитор часто смешивают с понятием смешанный неконкурентный ингибитор! Ингибиторы такого типа встречаются редко, хотя они имеют прямое отношение к изучению мультисубстратных ферментов.
Главная особенность этих ингибиторов - они не способны связываться со свободным ферментом. Они связываются только с фермент-субстратным комплексом. Это объясняется тем, что субстрат сам непосредственно включен в связывание ингибитора или связывание субстрата вызывает изменение конформации в связывающем ингибитор центре, облегчающее связывание ингибитора. Связывание ингибитора вызывает торможение активности фермента и превращение субстрата в продукт. Это может быть следствием прямого взаимодействия, или изменения конформации активного центра.
