
Лекции по физической химии / 22 ГЛАВА
.docГЛАВА 22. ЦЕПНЫЕ РЕАКЦИИ
22.1. Основные понятия о цепных реакциях
В ряде случаев в химических реакциях в качестве промежуточных продуктов выступают такие активные частицы как свободные атомы и радикалы, которые имеют свободные валентности и потому обладают высокой реакционной способностью. Эти частицы вступают в реакции, в результате которых вновь возникают свободные атомы и радикалы. Такая последовательность периодически повторяющихся реакций с участием активных частиц (свободных атомов и радикалов) называется цепной реакцией.
Хотя процесс образования свободных атомов или радикалов требует большой энергии активации, но их высокая реакционная способность и возникновение новых активных частиц при реакциях с насыщенными молекулами приводят к тому, что скорость цепных реакций оказывается обычно значительно выше скорости нецепных реакций. Зарождение в начале реакции небольшого количества реакционноспособных частиц приводит к превращению большого количества исходных веществ. Так как цепные реакции протекают циклически, то активная частица, возникающая в конце цикла, дает начало новому циклу, в конце которого происходит вновь регенерация активной частицы.
К цепным относятся реакции различных классов. По цепному механизму протекают, например, реакции горения или медленного окисления в газовой фазе:
2Н2 + О2 2Н2О
СН4 + 2О2 СО2 + 2Н2О
К цепным относятся многие реакции с участием углеводородов (реакции полимеризации, разложения), фотохимические реакции (образование НСl, НВr, СОСl2 и др.), цепные ядерные реакции – распад урана-235 или плутония в ядерном реакторе или бомбе.
Характерной особенностью цепных реакций является большая чувствительность скорости этих реакций к наличию некоторых примесей. Например, тщательно высушенные водород и кислород реагируют между собой очень медленно, но реакция протекает с нормальной скоростью в присутствии незначительного количества паров воды. Смесь водорода с хлором не реагирует в темноте при комнатной температуре, но быстро реагирует при введении в систему малых количеств паров натрия. В других случаях присутствие примесей приводит к резкому снижению скорости реакции. Например, при фотохимическом инициировании реакции водорода с хлором скорость образования хлороводорода уменьшается примерно в тысячу раз в присутствии одного процента кислорода.
На скорость многих газовых реакций влияет форма и материал сосуда, в котором протекает реакция. Обычно реакции замедляются при увеличении отношения S/V (S – площадь поверхности сосуда, V – его объем). Это отношение практически можно изменять, вводя в сосуд осколки материала сосуда – стекла, кварца и т.п.
Для многих реакций окисления в газовой фазе характерно то, что быстрая реакция (самопроизвольное воспламенение) протекает лишь в определенных пределах давления и температуры. На рисунке 22.1 показана зависимость пределов воспламенения от давления и температуры, которая наблюдается при окислении водорода, паров фосфора, сероуглерода и др.
Рис. 22.1. Пределы
воспламенения для реакции окисления
водорода

Объяснение указанных особенностей дает теория цепных реакций, начало развития которой относится к 1913 г., когда Боденштейном было введено понятие цепной реакции.
Различают два типа цепных реакций: с неразветвленными и разветвленными цепями. Примером первого типа реакций может служить реакция образования хлороводорода из водорода и хлора
Н2 + Сl2 2НСl,
схема механизма которой была предложена Нернстом.
В схеме можно выделить три группы реакций. Начинается процесс с реакции зарождения цепи:
Cl2 Cl + Cl
Эта реакция диссоциации молекулы хлора на атомы может происходить при поглощении света
Cl2 + h Cl + Cl,
термическим путем – при столкновении, например, двух молекул хлора с повышенной энергией:
Cl2 + Cl2 Cl + Cl + Cl2,
химическим путем – например, при взаимодействии молекулы хлора с атомом натрия, пары которого введены в систему. Образующиеся атомы хлора обладают высокой реакционной способностью и вступают в дальнейшее взаимодействие с исходными веществами, протекает вторая группа реакций – развитие цепи:
Cl + H2 HCl + H
H + Cl2 HCl + Cl
В результате первой реакции появляется атом водорода, который легко вступает во взаимодействие молекулой хлора, в результате чего образуется хлороводород и регенерируется атом хлора, который дает начало следующему звену:
Cl + H2 HCl + H
H + Cl2 HCl + Cl
и так далее. В результате возникают последовательно идущие один за другим циклы – развивается цепь реакций
Cl H Cl H Cl ...
При благоприятных условиях такая цепь может состоять из многих тысяч звеньев. В результате на одну первоначально активированную молекулу хлора образуется не две молекулы HCl, как при обычной бимолекулярной реакции, а тысячи и десятки тысяч молекул.
Для приведенной реакции характерным является то, что на одну вступающую в реакцию активную частицу Сl или Н вновь образуется одна активная частица. Такие цепи и называют неразветвленными.
Кроме приведенных реакций зарождения и развития цепи в системе протекает третья группа реакций – реакции обрыва цепи, приводящие к гибели активных частиц при соударении с какой-либо третьей частицей М или стенкой сосуда S:
Н + Н + М Н2 + М
Н + Н + S Н2 + S
Cl + Cl + M(S) Cl2 + M(S)
Н + Cl + M(S) HCl + M(S)
В присутствии, например, кислорода обрыв цепи может происходить в результате реакции
Н + О2 + М
![]() +
М
+
М
Образующийся малоактивный радикал
![]() гибнет на стенках сосуда или по реакции
гибнет на стенках сосуда или по реакции
![]() + Н Н2 + О2
+ Н Н2 + О2
При низких давлениях активные центры гибнут в основном на стенках сосуда, а при высоких давлениях происходит тримолекулярный обрыв в объеме. Поэтому для цепных реакций и характерны особенности, о которых говорилось выше – зависимость скорости реакции от величины удельной поверхности сосуда, от присутствия какого-либо инертного вещества, от давления или концентрации реагирующих веществ.
Кинетическое уравнение неразветвленной цепной реакции можно получить, исходя из механизма реакции. Например, детальное изучение реакции между водородом и бромом
Н2 + Br2 2HBr
показало, что реакция проходит в несколько элементарных стадий с разными константами скорости k:
Br2 Br + Br k1
Br + H2 HBr + H k2
H + Br2 HBr + Br k3
H + HBr H2 + Br k4
Br + Br Br2 k5
Исходя из этой схемы, скорость образования бромистого водорода можно представить уравнением:
![]()
![]() +
+
![]() –
–
![]() . (22.1)
. (22.1)
Рассматривая атомы брома и водорода как промежуточные продукты, можно применить к ним принцип стационарных концентраций Боденштейна (см. разд. 20.6):
![]() . (22.2)
. (22.2)
![]() . (22.3)
. (22.3)
Из суммы этих равновесий находим концентрацию атомов брома:
![]() . (22.4)
. (22.4)
После подстановки этой концентрации в уравнение (22.3) получим концентрацию атомов водорода:
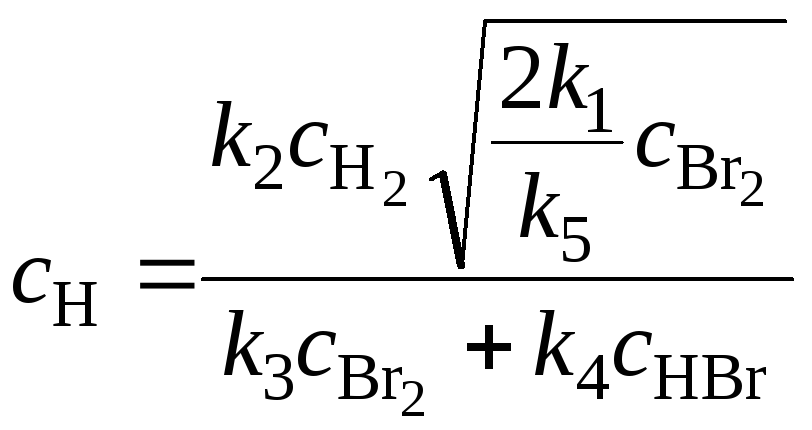 . (22.5)
. (22.5)
Подстановка концентраций атомов брома и водорода в уравнение (22.1) дает окончательное уравнение для скорости реакции:
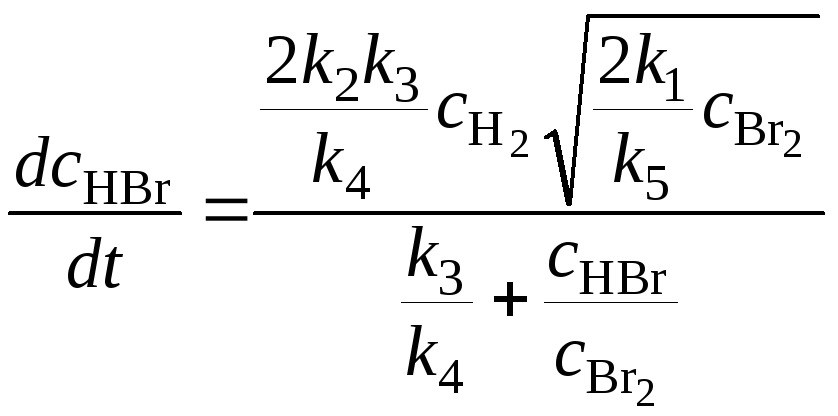 . (22.6)
. (22.6)
Это уравнение совпадает с уравнением (20.6), полученным по экспериментальным данным.
В ряде реакций в результате одного элементарного акта может возникать не одна, а две или больше химически активных частиц, т.е. происходит разветвление цепи. Такие реакции получили название разветвленных цепных реакций. В таких реакциях в начальный период времени число активных частиц, а следовательно, и скорость реакции лавинообразно нарастают вплоть до того момента, когда из-за израсходования исходного вещества скорость реакции начинает уменьшаться. Примером таких процессов может служить реакция окисления водорода, механизм которой по современным представлениям можно представить совокупностью последовательно протекающих элементарных химических актов:
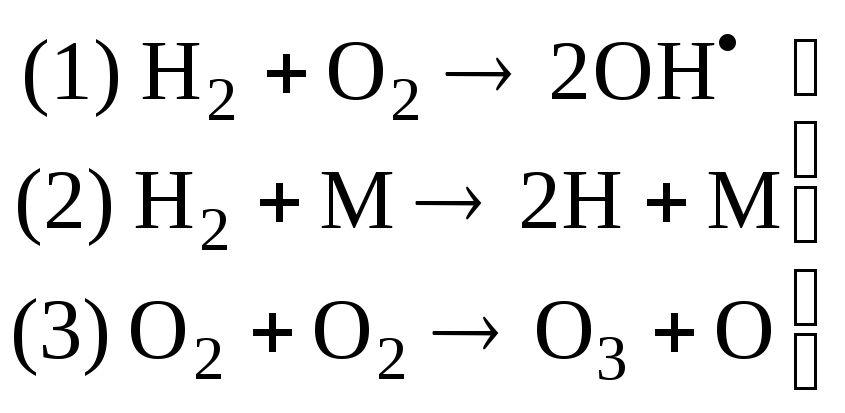 Зарождение цепи
Зарождение цепи
(4)
![]() + Н2 Н2О
+ Н Продолжение цепи
+ Н2 Н2О
+ Н Продолжение цепи
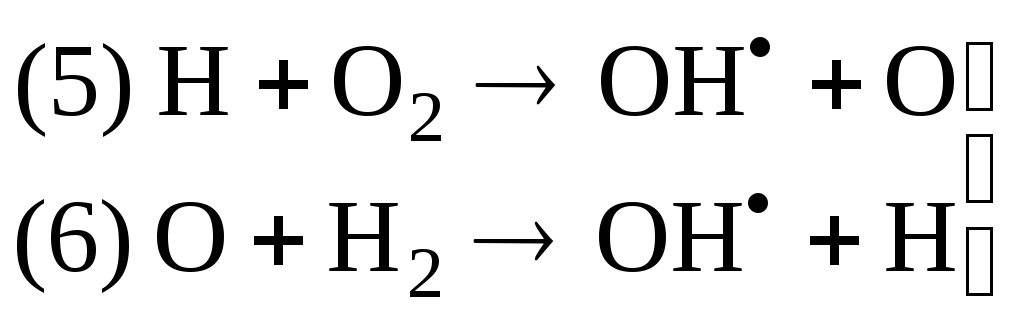 Разветвление цепи
Разветвление цепи
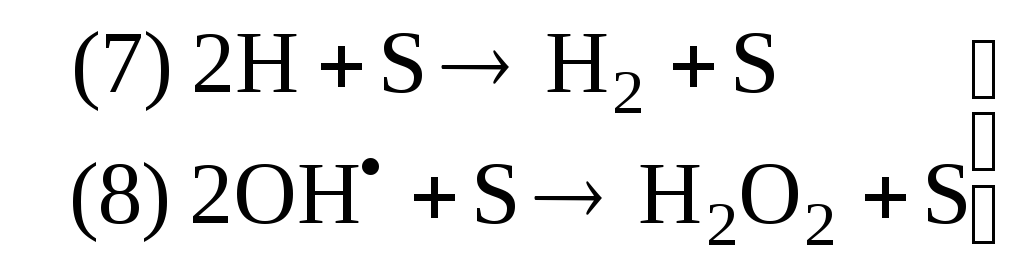 Обрыв цепи на стенке
Обрыв цепи на стенке
(9) Н + О2 + М
![]() + М Обрыв цепи в объеме
+ М Обрыв цепи в объеме
Образующиеся малоактивные радикалы
![]() могут распадаться на стенке:
могут распадаться на стенке:
2![]() + S Н2О2
+ О2 + S
+ S Н2О2
+ О2 + S
При больших давлениях возможны реакции в объеме:
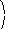 (10)
(10)
![]() + Н2 Н2О2
+ Н Продолжение цепи через
+ Н2 Н2О2
+ Н Продолжение цепи через
(11)
![]() + Н2О Н2О2
+
+ Н2О Н2О2
+
![]() малоактивний радикал
малоактивний радикал
Если разветвление цепи осуществляется часто, то даже одна первоначально возникшая цепь может привести к развитию многих цепей. В предельном случае можно представить, что разветвление происходит в каждом звене, и тогда говорят о сплошь разветвленной цепной реакции. В других случаях разветвление может происходить более редко.
Существование нижнего и верхнего пределов воспламенения качественно можно объяснить следующим образом. При давлениях, меньших нижнего предела, активные частицы легко диффундируют к стенкам сосуда, где происходит их гибель. Обрыв цепей на стенках преобладает над разветвлением, и быстрая реакция не развивается. При повышении давления диффузия к стенкам затрудняется, а возрастает число двойных соударений типа (5) и (6), которые ведут к разветвлению цепей; зарождение и разветвление цепей начинают преобладать над обрывом. В результате реакция самоускоряется и может закончиться самовоспламенением или взрывом, что и происходит внутри полуострова воспламенения.
Рис. 22.2.
Зависимость
скорости разветвленной
цепной реакции от времени внутри
полуострова
воспламенения
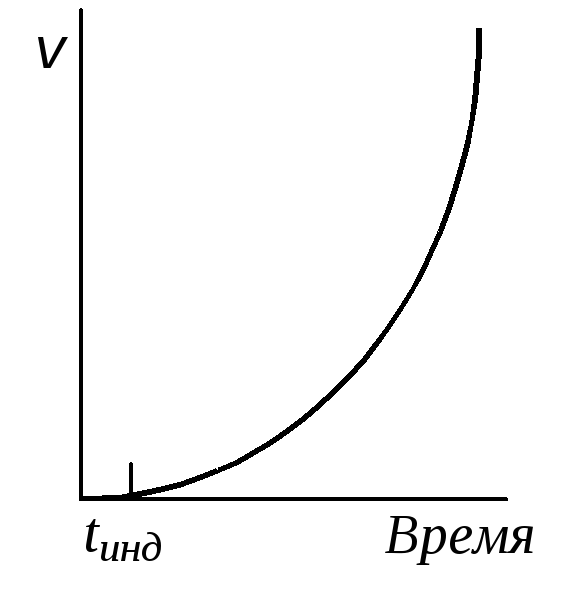
Воспламенению горючей смеси внутри полуострова воспламенения предшествует индукционный период tинд (рис. 22.2). Он объясняется тем, что сначала число цепей может быть очень малым и практически реакция незаметна из-за недостаточной чувствительности методов анализа. Но по истечении некоторого времени tинд число цепей очень быстро нарастает вследствие их размножения и наступает самовоспламенение или взрыв. Зависимость скорости реакции v от времени t можно представить уравнением:
![]() , (22.7)
, (22.7)
где A и – постоянные для данной реакции и зависящие от ряда условий. При выводе этой зависимости не учитывалось уменьшение концентрации реагирующих веществ вследствие выгорания, поэтому стремление скорости к бесконечности с течением времени не имеет физического смысла – скорость становится большой, но не бесконечной.
В некоторых случаях наблюдается и третий предел воспламенения (рис. 22.1), лежащий при более высоких давлениях. Его существование связывают с протеканием цепных реакций за счет малоактивных радикалов или с развитием теплового взрыва.
22.2. Элементарная теория цепных реакций
Имеется два варианта теории цепных реакций – более строгий, основанный на решении системы дифференциальных уравнений, и менее строгий, но более наглядный вероятностный вариант, который и рассматривается далее.
Важной характеристикой цепной реакции является средняя длина цепи - среднее число элементарных реакций, вызываемых одной активной частицей (атомом или радикалом), возникшей первоначально каким-либо независимым путем. Если no – число таких независимо возникающих частиц в единицу времени в единице объема, то no можно назвать скоростью зарождения цепей.
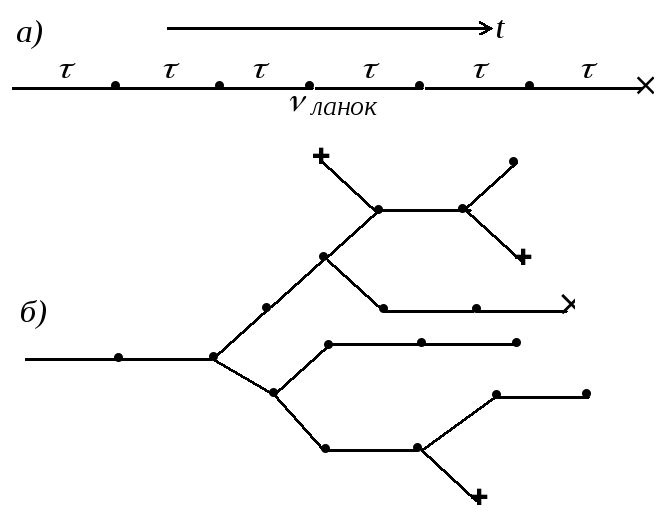
Величина, обратная средней длине цепи, представляет собой вероятность обрыва цепи . Эту связь можно понять с помощью схематического изображения цепи на рисунке 22.3. На схеме точка означает появление и регенерацию активной частицы, а крестик – ее гибель, т.е. обрыв цепи.
Рис. 22.3. Схематическое
изображение цепной реакции:
а
– неразветвленная цепь; б
– разветвленная цепь
=1/. (22.8)
Допустим также возможность разветвления цепи – появление в каком-либо звене двух или более активных частиц и охарактеризуем такую возможность вероятностью разветвления цепи .
Обозначим через время, в течение которого в среднем протекает одно звено цепной реакции. Тогда произведение равно среднему времени прохождения всей цепи от момента зарождения до обрыва. Концентрация активных частиц, т.е. их число в единице объема, пусть будет n. Скорость изменения концентрации этих частиц будет равна разности скоростей их образования no и исчезновения.
Если длина цепи = 1 (т.е. фактически цепь отсутствует), то активная частица гибнет в каждом звене. Тогда за среднее время развития одного звена прореагируют все n частиц, а скорость исчезновения будет равна n/ частиц/см3 с. Если же цепи развиваются и их средняя длина равна > 1, частица в среднем будет реагировать раз, а среднее время ее жизни будет равно . Следовательно, скорость уменьшения концентрации частиц выразится соотношением
![]() . (22.9)
. (22.9)
Если возможно разветвление цепи, т.е. > 0, то его влияние можно учесть, считая, что разветвление действует как бы в направлении, обратном обрыву, удлиняя цепь и уменьшая вероятность обрыва до величины ( – ). Тогда для скорости изменения концентрации активных частиц можно записать выражение:
![]() . (22.10)
. (22.10)
Решение этого дифференциального уравнения можно провести следующим образом. Для простоты записи введем обозначение a = ( – )/. Тогда
![]() . (22.11)
. (22.11)
Полагаем вначале, что no = 0, и после разделения переменных получаем:
![]() , (22.12)
, (22.12)
интегрирование которого дает:
lnn = –at + lnZ(t), (22.13)
где Z(t) – некоторая условная “постоянная” интегрирования. Тогда
n = Z(t)e–at. (22.14)
Продифференцируем это уравнение с учетом того, что Z не является постоянной величиной:
![]() . (22.15)
. (22.15)
Из сопоставления этого уравнения с уравнением (22.11) следует, что
![]() (22.16)
(22.16)
и
![]() . (22.17)
. (22.17)
После интегрирования этого уравнения получим
![]() , (22.18)
, (22.18)
где I – постоянная интегрирования. Подстановка этой величины в уравнение (22.15) дает
![]() . (22.19)
. (22.19)
Из условия, что в начальный момент реакции (t = 0) величина n = 0, следует, что
![]() (22.20)
(22.20)
и
![]() . (22.21)
. (22.21)
После подстановки значения a получим
![]() . (22.22)
. (22.22)
Скорость реакции v можно определить как скорость увеличения концентрации молекул продукта реакции. Так как в одном звене за время появляется одна молекула, то общее число молекул, образующихся в единице объема за единицу времени, равно n/. Таким образом, мы получаем основное уравнение теории цепных реакций:
![]() . (22.23)
. (22.23)
Рассмотрим использование этого уравнения для некоторых частных случаев.
При протекании неразветвленной цепной реакции = 0. Так как средняя длина цепи = 1/, то скорость такой реакции
![]() . (22.24)
. (22.24)
1 –
= 0; 2 – 0 <
< ;
3 –
>
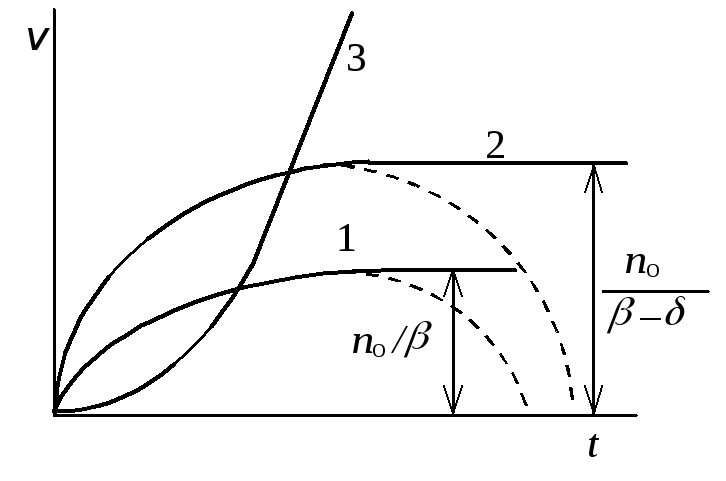 Рис.
22.4. Зависимость скорости
цепной
реакции от времени:
Рис.
22.4. Зависимость скорости
цепной
реакции от времени:
При возможности протекания разветвленной цепной реакции вероятность разветвления может оказаться меньше вероятности обрыва, т.е. 0 < < . В этом случае, согласно уравнению (22.23), система также должна достигать стационарной скорости, но эта скорость больше, чем в первом случае:
Если же вероятность разветвления больше вероятности обрыва, т.е. > , уравнение (22.23) принимает вид:
![]() , (22.25)
, (22.25)
где A и являются положительными постоянными. Полученное уравнение совпадает с приведенным ранее уравнением (22.7). Уравнение показывает, что скорость реакции может стать бесконечно большой (рис. 22.4), т.е. свидетельствует о возможности развития цепного воспламенения или взрыва.
Следует, однако, отметить, что полученные зависимости относятся к некоторым идеализированным условиям протекания реакции – предполагается, что концентрации исходных веществ поддерживаются постоянными, а продукты реакции выводятся из реакционной зоны. В реальных условиях, например, при проведении реакции в замкнутом сосуде, происходит “выгорание” исходных веществ, а продукты остаются в реакционной смеси. Поэтому для неразветвленных цепных реакций или для разветленных реакций с < скорость проходит через максимум (пунктир на рис.22.4). Возможно, что стационарное состояние вообще не будет достигнуто, так как максимальная скорость может оказаться меньше стационарной. В случае разветвленной цепной реакции с > учет выгорания реагентов должен дать, как уже указывалось ранее, очень большую, но все же конечную скорость.
Условие > соответствует протеканию реакции в области полуострова воспламенения, а условие > – вне него. Таким образом, теория разветвленных цепных реакций количественно объясняет существование нижнего и верхнего пределов воспламенения.
К воспламенению или взрыву может также привести, независимо от механизма реакции, саморазогрев реагирующей смеси. По уравнению Аррениуса, скорость реакции увеличивается при повышении температуры по экспоненциальному закону, в то время как скорость теплоотвода – более медленно (пропорционально разности температур). В случае экзотермической реакции, если теплота не будет отводиться из реакционной зоны с достаточной скоростью, реакционная смесь начнет саморазогреваться, а скорость реакции все более возрастать. Развитие этих процессов может привести к воспламенению реакционной смеси или взрыву. В этом случае говорят о тепловом самовоспламенении (тепловом взрыве). Кинетика теплового самовоспламенения внешне может не отличаться от кинетики цепного воспламенения, что нужно иметь в виду при изучении реакций, переходящих в воспламенение или взрыв.
