
- •Міністерство освіти і науки, молоді та спорту україни
- •Міністерство освіти і науки, молоді та спорту україни
- •Самостійна робота № 1
- •Основні параметри хімічного зв’язку
- •Ковалентний зв'язок
- •Ковалентний неполярний та полярний зв'язок.
- •Іонний зв'язок
- •Металічний зв'язок
- •Водневий зв'язок
- •Завдання для самостійної роботи.
- •Самостійна робота № 2
- •Оксиген Електронна будова
- •Хімічні властивості
- •Застосування кисню
- •Застосування озону
- •Сульфур Електронна будова
- •Фізичні властивості
- •У природі
- •Хімічні властивості
- •Застосування
- •Добування
- •Застосування сульфатної кислоти
- •Застосування сульфатів
- •Виробництво сульфатів Контактний спосіб
- •Нітроген і фосфор
- •Застосування
- •Солі амонію
- •Добування солей амонію в лабораторії.
- •Промисловий синтез амоніаку
- •Хімічні властивості
- •Нітратна і ортофосфатна кислота Нітратна кислота – hno3
- •Застосування
- •Ортофосфатна кислота - н3ро4
- •Застосування
- •Силіцій (кремній)
- •Хімічні властивості силіцію
- •Оксиди карбону і силіцію
- •Добування карбону (іv) оксиду
- •Карбонатна кислота і карбонати
- •Твердість води
- •Колообіг карбону у природі
- •Силікатна кислота і силікати
- •Генетичний зв'язок між класами неорганічних сполук
- •Приклади хімічних рівнянь
- •Гідроген
- •Поширення в природі
- •Ізотопи гідрогену
- •Одержання
- •Фізичні властивості
- •Хімічні властивості
- •Використання
- •Галогени (f, Cl, Br, I). Загальна характеристика
- •Хлоридна кислота.
- •Бром. Йод.
- •Завдання для самостійної роботи.
- •Самостійна робота № 3
- •Алотропні модифікації карбону
- •Будівельні матеріали
- •Завдання для самостійної роботи
- •Самостійна робота № 4
- •Корозія металів
- •Захист від корозії
- •Лужні метали
- •Поширення у природі
- •Одержання
- •Фізичні та хімічні властивості
- •Сполуки лужних металів
- •Використання лужних металів та їх сполук
- •Лужноземельні метали
- •Фізичні та хімічні властивості
- •Сполуки лужноземельних металів
- •Біологічна роль лужних та лужноземельних металів
- •Завдання для самостійної роботи
- •Самостійна робота № 5
- •Алюміній
- •Найважливіші сполуки алюмінію
- •Застосування
- •Фізичні та хімічні властивості заліза
- •Найважливіші сполуки феруму Сполуки феруму (іі)
- •Сполуки феруму (ііі)
- •Застосування
- •Завдання для самостійної роботи
Колообіг карбону у природі
Важлива роль у колообігу Карбону належить оксиду карбону (IV), що входить до складу атмосфери Землі. 3 повітря СО2 поглинається рослинами та
планктоном Світового океану. Із рослин, що служать кормом для тварин, Карбон переходить у тваринні організми. Тварини виділяють Карбон у вигляді вуглекислого газу під час дихання. При відмиранні тварини і рослини гниють, перетворюються на СО2. Частково перетворюються на горючі копалини кам’яне вугілля, нафту, природний газ. Використовуються як паливо. Утворюються вапняки, доломіти, карбонати.
Силікатна кислота і силікати
Силікатні кислоти: Н4SiO4 – ортосилікатна; Н2SiO3 – метасилікатна.
Слабкіші за карбонатну, нерозчинні, легко утворюють колоїдні розчини. Нестійкі при нагріванні: H2SiO3 = H2O + SiO2
Добування:
Na2SiO3 + 2H2O + 2CO2 = 2NaHCO3 + H2SiO3↓
драглистий осад
K2SiO3 + 2HCI = H2SiO3↓ + 2KCI
Солі – силікати: нерозчинні, крім солей Na і К, водні розчини яких називають рідкими склом (силікатний клей).
Приклади солей: СaSiO3 – кальцій силікат (або Сa ∙ SiO2);
 Na2SiO3
– натрій силікат (або Na2О
∙ SiO2);
Na2SiO3
– натрій силікат (або Na2О
∙ SiO2);
Біла глина AI2O3 ∙ 2SiO2 ∙ 2H2O
Польовий шпат K2O ∙ AI2O3 ∙ 6SiO2 алюмосилікати
Нефелін Na2О ∙ AI2O3 ∙ 2SiO2
П
 риродні
→ Силікатна 1) виробництво
в’яжучих
риродні
→ Силікатна 1) виробництво
в’яжучих
с илікати
промисловість2)
виробництво
скла
илікати
промисловість2)
виробництво
скла
3) виробництво кераміки
1) Наприклад, порт ланд - цемент
2 )
Віконне скло (Na2О
∙ СаО ∙ 6SiO2),
кришталеве скло, хімічне скло, емаль
)
Віконне скло (Na2О
∙ СаО ∙ 6SiO2),
кришталеве скло, хімічне скло, емаль
3) цегла, черепиця, облицювальні плитки, фарфор, фаянс.
Генетичний зв'язок між класами неорганічних сполук

|
Електроліти | ||
|
Сильні |
Середні |
Слабкі |
|
H2SO4, HCI, HNO3, луги, розчинні солі
|
H3PO4, H2SO3, Mg(OH)2 |
H2S, H2CO3, H2SiO3, NH4OH, органічні кислоти |
Приклади хімічних рівнянь
CuSO4 + Fe → Cu + FeSO4
Zn + 2HCI → ZnCI2 + H2↑
2Na + CI2 → 2NaCI
4Li + O2 → 2Li2O
Na2CO3 + 2HCI → 2NaCI + H2O + CO2↑
SiO2 + 2Mg
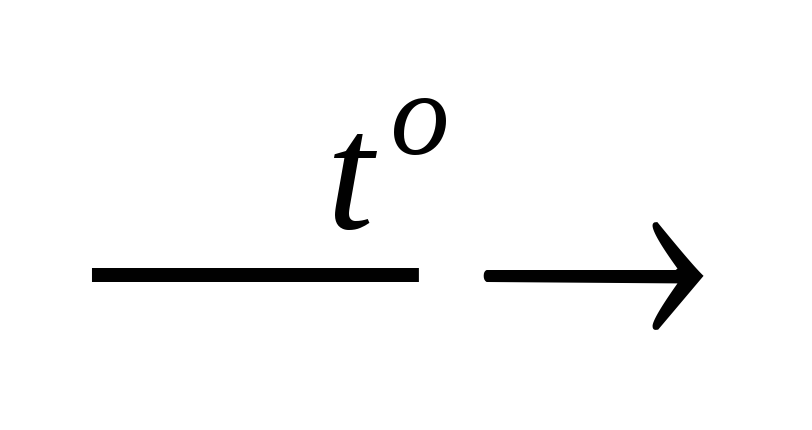 Si
+ 2MgO
Si
+ 2MgO4HCI + MnO2 → MnCI2 + CI2 + 2H2O
CaCO3
 CaO + CO2↑
CaO + CO2↑ZnO + 2NaOH → Na2ZnO2 + H2O
AI(OH)3 + NaOH → NaAIO2 + 2H2O
HCI + AgNO3 → AgCI↓ + HNO3
BaCI2 + Na2SO4 → BaSO4 + 2NaCI
2KI + 2H2O → H2 + I2 + KOH
H2SiO3
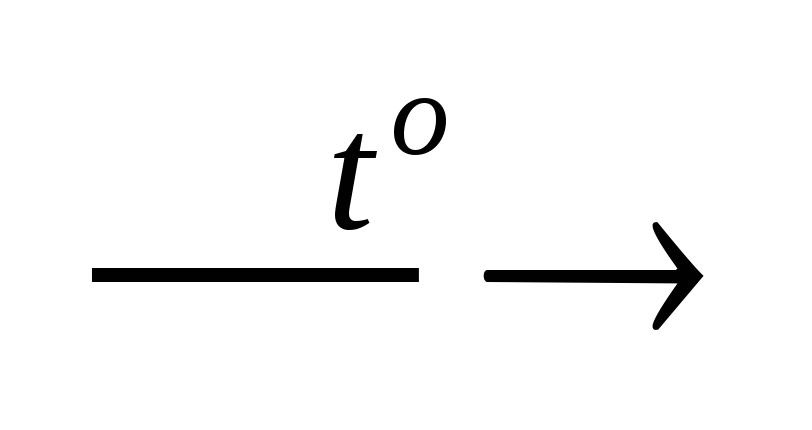 SiO2
+ H2O
SiO2
+ H2OCaO + H2O → Ca(OH)2
Гідроген
Гідроген – хімічний елемент І групи періодичної системи елементів Д.І.Менделєєва. Електронна конфігурація атома гідрогену в основному стані 1s1. У твердому стані при
-259 оС проводить електричний струм, у розчинах утворює гідратований позитивний одно заряджений іон Н3О+.
Поширення в природі
Гідроген – один з найпоширеніших елементів не тільки на нашій планеті, але і і Всесвіті. З кожних 100 атомів, які входять до складу земної кори, 17 є атомами гідрогену. В атмосфері Сонця вміст гідрогену складає 75-85%. У вільному стані на Землі він зустрічається досить рідко. В атмосферу гідроген потрапляє при розкладанні деяких органічних речовин у мікроорганізмами. Основна маса гідрогену в земній корі міститься у вигляді хімічних сполук – води, вуглеводнів, нафти і горючих газів. Гідроген входить до складу, з яких складаються рослинні та тваринні організми.
