
- •Предисловие
- •Введение
- •Роберт Вильгельм Бунзен
- •Анри Луи Ле Шаталье
- •Вильгельм Фридрих Оствальд
- •Сванте Август Аррениус
- •Якоб Генрих Вант-Гофф
- •Иоханн Николаус Брёнстед и Михаил Ильич Усанович
- •Николай Николаевич Семенов
- •Химическая термодинамика учебно-целевые задачи – научить студентов:
- •Значимость темы
- •Основные понятия и определения химической термодинамики
- •Внутренняя энергия
- •Теплота и работа
- •Первый закон термодинамики
- •Применение I закона к простейшим процессам
- •Тепловые эффекты. Закон гесса
- •Теплоемкость
- •Второй закон термодинамики
- •Некоторые формулировки 2-го закона
- •Изменение энтропии при различных процессах
- •Пастулат планка
- •Термодинамические потенциалы
- •Соотношение между термодинамическими потенциалами
- •Закон действующих масс
- •Вопросы по теме: "термодинамика"
- •Примеры решения типовых задач
- •Пример решения контрольного задания по теме "Термодинамика"
- •Решение
- •Задачи для самостоятельной работы
- •Варианты заданий для домашней контрольной работы
- •Лабораторная работа №1.
- •Особые условия выполнения работы:
- •Устройство и настройка термометра Бекмана
- •Термодинамика фазовых превращений
- •Термодинамика фазовых равновесий
- •Основные понятия
- •Уравнение клайперона-клаузиуса
- •Диаграммы состояния однокомпонентных систем
- •Диаграмма состояния воды
- •Диаграмма состояния диоксида углерода
- •Бинарные системы Диаграммы плавкости
- •Взаимная растворимость жидкостей
- •Трехкомпонентные системы
- •Равновесие жидкость-жидкость в трехкомпонентных системах.
- •Распределение растворяемого вещества между двумя жидкими фазами. Экстракция.
- •Вопросы для подготовки к занятиям по теме: "термодинамика фазовых равновесий".
- •Примеры решения типовых задач.
- •Задачи для самостоятельной работы.
- •Лабораторная работа 1: построение диаграммы плавкости 2-х компонентной системы с простой эвтектикой.
- •Лабораторная работа № 2. Изучение взаимной растворимости фенола и воды.
- •Лабораторная работа № 3. Определение коэффициента распределения уксусной кислоты между водой и бензолом.
- •Свойства разбавленных растворов электролитов и неэлектролитов.
- •Повышение температуры кипения растворов.
- •Понижение температуру замерзания растворов.
- •Биологическое значение осмотического давления
- •Указания к выполнению работы.
- •Вопросы для самоконтроля по технике выполнения работы
- •Вопросы для самоконтроля при выполнении данного задания
- •Вопросы и задачи для самоконтроля усвоения темы
- •Вопросы для самоконтроля усвоения материала практической работы
- •Биологический статус изучаемой темы
- •Вопросы для подготовки:
- •Диссоциация воды
- •Водородный показатель
- •Механизм действия буферных систем
- •РН буферных систем
- •Влияние изменения объема буферных систем на рН.
- •Кислотно-щелочное равновесие крови
- •Роль внутренних органов в поддержании кислотно-щелочного резерва.
- •Изменение кислотно-щелочного равновесия при различных заболеваниях.
- •Задачи и задания для самостоятельной работы
- •Экспериментальная часть
- •Работа №3. Определение буферной ёмкости.
- •Электрохимия. Учебно-целевые задачи: Изучив этот раздел учебной программы, студент должен знать:
- •Значение электрохимических явлений для медицины.
- •Электродные процессы и электродвижущие силы.
- •Электрод и электродный потенциал.
- •Строение двойного электрического слоя на границе раствор-металл
- •Уравнение нернста
- •Гальванические элементы и их электродвижущие силы
- •Концентрационные гальванические элементы.
- •Диффузный потенциал.
- •Электроды первого рода.
- •Водородный электрод.
- •Ионоселективные электроды
- •Стеклянный электрод
- •Электроды второго рода.
- •Хлорсеребряный электрод Аg ׀ Ag Cl. KCl
- •Сопровождается реакцией растворения или осаждения соли АgСl:
- •Окислительно – восстановительные системы (ов) и ов –электроды.
- •Уравнение Петерса.
- •Классификация обратимых электродов.
- •Измерение эдс гальванических элементов.
- •Потенциометрия.
- •Прямые потенциометрические методы.
- •Приложение
- •Экспериментальная часть. Лабораторная работа №1. Измерение эдс гальванических элементов.
- •Порядок выполнения работы.
- •Изменение потенциалов отдельных электродов.
- •Потенциалов отдельных электродов.
- •Лабораторная работа № 3.
- •Лабораторная работа №4. Потенциометрическое измерение окислительно – восстановительных потенциалов. Редокс – системы.
- •Кинетика
- •Значение для медицины и фармации
- •Вопросы для подготовки к занятию
- •Введение
- •Понятие о скорости химического процесса
- •Основной закон химической кинетики
- •Кинетические уравнения реакций
- •Реакции первого порядка
- •Реакции второго порядка
- •Сложные реакции
- •Гетерогенные реакции
- •Температурная зависимость константы скорости реакции.
- •Методы расчета энергии активации и предэкспоненциального множителя а.
- •Основы молекулярной кинетики
- •Теория активных столкновений
- •Теория переходного состояния
- •Задачи и задания для самостоятельного решения.
- •Экспериментальная часть
- •Опыт № 1.Зависимость от концентрации.
- •Опыт №2. Зависимость от температуры
- •Учебно-методическое и информационное обеспечение дисциплины
- •По технике безопасности
- •И производственной санитарии при работе
- •В химических лабораториях
- •Медицинских учебных заведений
- •Содержание
Биологическое значение осмотического давления
Осмос имеет большое значение для растительных и животных организмов, способствуя достаточному оводнению клеток и межклеточных структур. Возникающее при этом осмотическое давление обусловливает тургор клеток.
Каждая живая клетка имеет оболочку или поверхностный слой протоплазмы, обладающие свойством полупроницаемости. Помещая животные или растительные клетки в дистиллированную воду, можно наблюдать перемещение воды внутрь клеток, что ведет к их набуханию, а затем к разрыву оболочек и вытеканию клеточного содержимого. Подобное разрушение клеток путем разрыва их оболочек (или поверхностных слоев протоплазмы) называют лизисом, а в случае эритроцитов – гемолизом.
В крепких растворах солей отмечается, наоборот, сморщивание клеток (плазмолиз), обусловленное потерей воды, перемещающейся из них в более концентрированный внешний раствор.
Растворы с осмотическим давлением, равным давлению раствора, взятого за стандарт, называются изотоническими (изоспо-гречески равный). Растворы с осмотическим давлением более высоким, чем в стандарте, называются – гипертоническими, с меньшим давлением – гипотоническими.
Осмотические давление биологических жидкостей в различных организмах неодинаково: так, осмотическое давление крови у лягушек несколько ниже, чем у человека, а у некоторых морских животных, обитающих в воде со значительным содержанием солей, оно выше. У растений, а также у многих морских животных и акуловых рыб осмотическое давление тканевых жидкостей в определенной степени меняется в зависимости от осмотического давления внешней среды.
Более высокоорганизованные животные имеют постоянное осмотическое давление крови, независящее от внешней среды. Постоянство этого показателя называют изоосмией. Нарушение изоосмии оказывается губительным для организма гораздо раньше, чем наступает плазмолиз или лизис клеток. Понижение осмотического давления введением больших избытков воды или в результате интенсивной потери солей, например с потом, вызывает рвоту, судороги, затемнение сознания и т.п., вплоть до гибели организма. Повышение же осмотического давления путем введения больших количеств воды. Вода скапливается в тех тканях, в которых откладывается избыточное количество солей, что вызывает их отеки (в первую очередь подкожной клетчатки); в то же время обезвоживание слизистых оболочек обусловливает чувство жажды, нарушает нормальную деятельность нервной системы и других жизненно важных органов.
В организм человека и животных можно вводить в больших количествах только изотонические растворы. Такие растворы вводят больным после тяжелых операций для возмещения потерь жидкости с кровью. При хирургических операциях извлеченные из брюшной полости петли кишок предохраняют от высыхания, обкладывая их марлевыми салфетками, смоченными физиологическим раствором.
В клинической практике применяются гипертонические растворы. небольшое количество их вводят внутривенно, например при глаукоме, характеризующейся повышенным внутриглазным давлением, чтобы «оттянуть» избыточное количество влаги из передней камеры глаза.
В хирургии широко применяют гипертонические повязки, представляющие собой марлевые полоски, смоченные в гипертонических растворах NaCl и введенные в гнойные раны; согласно законам осмоса ток раневой жидкости направляется по марле наружу, что способствует постоянному очищению раны от гноя, микроорганизмов, продуктов распада и пр.
Используемые в качестве слабительных средств плохо всасывающиеся в желудочно-кишечном тракте соли MgSO4 и Na2SO4 применяют также в виде гипертонических растворов. Это вызывает переход больших количеств воды из слизистой оболочки в просвет кишечника, что способствует послабляющему действию сульфатов.
Создание изоосмической (изотонической) среды совершенно необходимо при экспериментальных исследованиях на выделенных из организма органах и тканях.
КОЛЛИГАТИВНЫЕ СВОЙСТВА РАСТВОРОВ ЭЛЕКТРОЛИТОВ.
Растворам электролитов присущи все основные свойства растворов неэлектролитов. Однако, в растворах электролитов отсутствует та пропорциональность между молярной концентрацией и осмотическим давлением, повышением температуры кипения и т.п., которая была установлена для растворов неэлектролитов.
В растворах электролитов осмотическое давление и температура кипения выше, а температура замерзания ниже, чем следовало бы ожидать исходя из молярной концентрации. Причина этих отклонений заключается в диссоциации электролитов, в результате чего в растворах оказывается большее число кинетически активных частиц (сумма молекул и ионов), чем в эквимолярных растворах неэлектролитов.
Чтобы законы, применяемые для электролитов, можно было использовать и для растворов неэлектролитов, Вант-Гофф ввел поправку – коэффициент i. Коэффициент Вант-Гоффа показывает, во сколько раз истинная концентрация кинетически активных частиц и, следовательно, осмотическое даление, понижение температуры замерзания, понижение давления пара, повышение температуры кипения в растворе электролита больше, чем в эквимоляльном растворе неэлектролита:
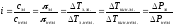
Величина связана со степенью диссоциации электролита следующим соотношением:

υ – количество ионов, на которое диссоциирует одна молекула электролита.
Используя коэффициент i, можно применять закон Рауля, его следствия и законы осмотического давления к растворам электролитов:
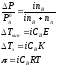
При одинаковой температуре растворы электролитов, содержащие равные количества частиц (молекул и ионов) в единице объема растворителя, изотоничны. Из двух растворов электролитов с одинаковой молярной концентрацией осмотическое давление будет выше в растворе электролита с более высокой степенью диссоциации. При одинаковой степени диссоциации в растворе электролита, диссоциирующего на большее число ионов, осмотическое давление будет выше.
Изучение коллигативных свойств разбавленных растворов электролитов и неэлектролитов привело к формированию физической теории растворов.
При подготовке к занятию необходимо, используя конспект лекций, а также указанные учебные пособия, подготовить следующие вопросы:
Какие растворы называются идеальными, предельно разбавленными и неидеальными?
Какие способы выражения концентраций называются моляльностью и моляльной долей?
Что называется равновесным давлением насыщенного пара над жидкостью? Зависит ли оно от температуры?
Сформулируйте закон и следствия из закона Рауля.
Объясните, почему температура замерзания раствора ниже, а температура кипения раствора выше, чем у чистого растворителя?
напишите уравнение криометрии и эбулиометрии и обоснуйте данные зависимости.
В чем заключается физический смысл криоскопической и эбуллиоскопической постоянных
Какое явление называют осмосом и каков его механизм?
Что называется осмотическим давлением и какие факторы его определяют?
Напишите математическое выражение закона Вант-Гоффа и дайте его определение.
Какие свойства растворов относятся к коллигативным и для решения каких вопросов их используют.
Как отличаются коллигативные свойства разбавленных растворов электролитов от идентичных свойств растворов неэлектролитов и почему?
В чем заключается физический смысл изотонического коэффициента?
Записать уравнение криометрии и эбулиометрии применительно к разбавленным растворам слабых и сильных электролитов.
В чем заключается биологическая значимость изучаемых вопросов?
