
- •Предисловие
- •Введение
- •Роберт Вильгельм Бунзен
- •Анри Луи Ле Шаталье
- •Вильгельм Фридрих Оствальд
- •Сванте Август Аррениус
- •Якоб Генрих Вант-Гофф
- •Иоханн Николаус Брёнстед и Михаил Ильич Усанович
- •Николай Николаевич Семенов
- •Химическая термодинамика учебно-целевые задачи – научить студентов:
- •Значимость темы
- •Основные понятия и определения химической термодинамики
- •Внутренняя энергия
- •Теплота и работа
- •Первый закон термодинамики
- •Применение I закона к простейшим процессам
- •Тепловые эффекты. Закон гесса
- •Теплоемкость
- •Второй закон термодинамики
- •Некоторые формулировки 2-го закона
- •Изменение энтропии при различных процессах
- •Пастулат планка
- •Термодинамические потенциалы
- •Соотношение между термодинамическими потенциалами
- •Закон действующих масс
- •Вопросы по теме: "термодинамика"
- •Примеры решения типовых задач
- •Пример решения контрольного задания по теме "Термодинамика"
- •Решение
- •Задачи для самостоятельной работы
- •Варианты заданий для домашней контрольной работы
- •Лабораторная работа №1.
- •Особые условия выполнения работы:
- •Устройство и настройка термометра Бекмана
- •Термодинамика фазовых превращений
- •Термодинамика фазовых равновесий
- •Основные понятия
- •Уравнение клайперона-клаузиуса
- •Диаграммы состояния однокомпонентных систем
- •Диаграмма состояния воды
- •Диаграмма состояния диоксида углерода
- •Бинарные системы Диаграммы плавкости
- •Взаимная растворимость жидкостей
- •Трехкомпонентные системы
- •Равновесие жидкость-жидкость в трехкомпонентных системах.
- •Распределение растворяемого вещества между двумя жидкими фазами. Экстракция.
- •Вопросы для подготовки к занятиям по теме: "термодинамика фазовых равновесий".
- •Примеры решения типовых задач.
- •Задачи для самостоятельной работы.
- •Лабораторная работа 1: построение диаграммы плавкости 2-х компонентной системы с простой эвтектикой.
- •Лабораторная работа № 2. Изучение взаимной растворимости фенола и воды.
- •Лабораторная работа № 3. Определение коэффициента распределения уксусной кислоты между водой и бензолом.
- •Свойства разбавленных растворов электролитов и неэлектролитов.
- •Повышение температуры кипения растворов.
- •Понижение температуру замерзания растворов.
- •Биологическое значение осмотического давления
- •Указания к выполнению работы.
- •Вопросы для самоконтроля по технике выполнения работы
- •Вопросы для самоконтроля при выполнении данного задания
- •Вопросы и задачи для самоконтроля усвоения темы
- •Вопросы для самоконтроля усвоения материала практической работы
- •Биологический статус изучаемой темы
- •Вопросы для подготовки:
- •Диссоциация воды
- •Водородный показатель
- •Механизм действия буферных систем
- •РН буферных систем
- •Влияние изменения объема буферных систем на рН.
- •Кислотно-щелочное равновесие крови
- •Роль внутренних органов в поддержании кислотно-щелочного резерва.
- •Изменение кислотно-щелочного равновесия при различных заболеваниях.
- •Задачи и задания для самостоятельной работы
- •Экспериментальная часть
- •Работа №3. Определение буферной ёмкости.
- •Электрохимия. Учебно-целевые задачи: Изучив этот раздел учебной программы, студент должен знать:
- •Значение электрохимических явлений для медицины.
- •Электродные процессы и электродвижущие силы.
- •Электрод и электродный потенциал.
- •Строение двойного электрического слоя на границе раствор-металл
- •Уравнение нернста
- •Гальванические элементы и их электродвижущие силы
- •Концентрационные гальванические элементы.
- •Диффузный потенциал.
- •Электроды первого рода.
- •Водородный электрод.
- •Ионоселективные электроды
- •Стеклянный электрод
- •Электроды второго рода.
- •Хлорсеребряный электрод Аg ׀ Ag Cl. KCl
- •Сопровождается реакцией растворения или осаждения соли АgСl:
- •Окислительно – восстановительные системы (ов) и ов –электроды.
- •Уравнение Петерса.
- •Классификация обратимых электродов.
- •Измерение эдс гальванических элементов.
- •Потенциометрия.
- •Прямые потенциометрические методы.
- •Приложение
- •Экспериментальная часть. Лабораторная работа №1. Измерение эдс гальванических элементов.
- •Порядок выполнения работы.
- •Изменение потенциалов отдельных электродов.
- •Потенциалов отдельных электродов.
- •Лабораторная работа № 3.
- •Лабораторная работа №4. Потенциометрическое измерение окислительно – восстановительных потенциалов. Редокс – системы.
- •Кинетика
- •Значение для медицины и фармации
- •Вопросы для подготовки к занятию
- •Введение
- •Понятие о скорости химического процесса
- •Основной закон химической кинетики
- •Кинетические уравнения реакций
- •Реакции первого порядка
- •Реакции второго порядка
- •Сложные реакции
- •Гетерогенные реакции
- •Температурная зависимость константы скорости реакции.
- •Методы расчета энергии активации и предэкспоненциального множителя а.
- •Основы молекулярной кинетики
- •Теория активных столкновений
- •Теория переходного состояния
- •Задачи и задания для самостоятельного решения.
- •Экспериментальная часть
- •Опыт № 1.Зависимость от концентрации.
- •Опыт №2. Зависимость от температуры
- •Учебно-методическое и информационное обеспечение дисциплины
- •По технике безопасности
- •И производственной санитарии при работе
- •В химических лабораториях
- •Медицинских учебных заведений
- •Содержание
Распределение растворяемого вещества между двумя жидкими фазами. Экстракция.
Если к системе из двух взаимно нерастворимых или ограниченно растворимых жидкостей добавлять третью жидкость, способную в них растворяться, то добавляемая жидкость будет распределятся между обеими жидкими фазами в соответствии с законом распределения Нернста-Шилова:
третий компонент, добавляемый к системе, состоящий из двух взаимно нерастворимых или ограниченно растворимых жидкостей, распределяется между обеими жидкими слоями в определенном, постоянном при данной температуре отношении:
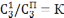
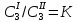 ,
,
где К - коэффициент распределения.
При распределении третьего вещества между двумя несмешивающимися жидкостями возможен случай, когда степень диссоциации распределяющегося вещества в разных растворителях отличается. В этих случаях закон распределения имеет вид:
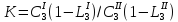
 ;
;
LI, LII - степень диссоциации или ассоциации распределяемого вещества в I и II фазах.
Коэффициент распределения, таким образом, зависит от температуры, природы всех веществ, входящих в систему, и от степени диссоциации или ассоциации третьего компонента, но не зависит от концентрации распределяемого вещества. Закон распределения широко используется при экстрагировании вещества из раствора.
Экстракцией называют процесс извлечения вещества, растворенного в одном растворителе, другим растворителем (экстрагентом), который не смешивается с первым и лучше растворяет извлекаемое вещество.
Экстракцию широко применяют в фармации для извлечения из растительного сырья эфирных масел, алколоидов и других физиологически активных веществ. Экстракция бывает однократной и. дробной. При однократной - экстрагент добавляется в один прием, при дробной - добавление экстрагента проводится порциями в несколько приемов, причем, чем больше число последовательных стадий извлечения, тем больше полнота извлечения при одном и том же количестве взятого экстрагента. После n экстрагирований в исходном растворе остается mnkп растворенного вещества:
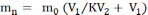

mo - начальное количество экстрагируемого вещества;
V, - объем раствора в котором находится экстрагируемое вещество;
V2 - объем растворителя, употребляемый на одно экстрагирование;
n - общее количество операций экстрагирования.
Для оценки степени извлечения сравнивают массу извлеченного вещества от теоретически возможной
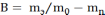
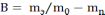
mэ - экспериментально найденная масса извлеченного вещества при экстракции.
Вопросы для подготовки к занятиям по теме: "термодинамика фазовых равновесий".
Основные понятия и определения: фаза, составляющие вещества, компоненты, число компонентов и число степеней свободы.
Правило фаз Гиббса. Прогнозирование фазовых переходов при изменении условий.
Диаграммы состояния однокомпонентных систем (вода, сера, углекислый газ).
Уравнение Клапейрона-Клаузиуса. Связь с принципом ЛеШателье.
Термический анализ. Вид кривых охлаждения и построение диаграммы плавкости 2-х компонентной системы с простой эвтетикой.
Анализ диаграмм плавкости:
а) с простой эвтетикой;
б) с образованием химических соединений;
в) с неограниченной растворимостью в твердом состоянии.
Применение правил фаз Гиббса и рычага к диаграммам плавкости. Определение состава лекарственной смеси по диаграмме плавкости.
Анализ диаграмм растворимости ограниченно растворимых жидкостей:
а) с верхней критической температурой растворения;
б) с нижней критической температурой растворения;
в) с замкнутой областью расслоения.
9. Трехкомпонентные системы. Способы изображения состава.
Закон распределения веществ между двумя несмешивающимися жидкостями. Коэффициент распределения.
Теоретические основы экстрагирования. Применение экстрагирования в медицине.
