-
Реальні гази та рівняння ван-дер-ваальса
Рівняння
(2.1.16) є справедливим доти, доки є коректними
наші припущення щодо ідеальності газу.
Наприклад, при високій густині газу вже
не можна нехтувати власними розмірами
молекул порівняно з відстанню поміж
ними, оскільки вони стають порівняльними
поміж собою. Окрім того в реальних газах
завжди існує додатковий до зовнішнього
( )
більший, або менший тиск (
)
більший, або менший тиск ( ),
який пов’язаний із слабкою, але існуючою
в реальних газах взаємодією поміж
молекулами.
),
який пов’язаний із слабкою, але існуючою
в реальних газах взаємодією поміж
молекулами.
Одним
з найпростіших рівнянь стану для реальних
газів є так зване рівняння Ван-дер-Ваальса.
В цьому рівнянні:
|

|
(2.1.17)
|
де
ми бачимо дві константи ( ),
котрі описують конкретний реальний
газ і наводяться в таблицях фізичних
констант для різних газів.
),
котрі описують конкретний реальний
газ і наводяться в таблицях фізичних
констант для різних газів.
Константа
 пов’язана із згаданим додатковим
тиском:
пов’язана із згаданим додатковим
тиском:
 ,
тоді як константа
,
тоді як константа
 враховує власний об’єм всіх молекул:
величина
враховує власний об’єм всіх молекул:
величина
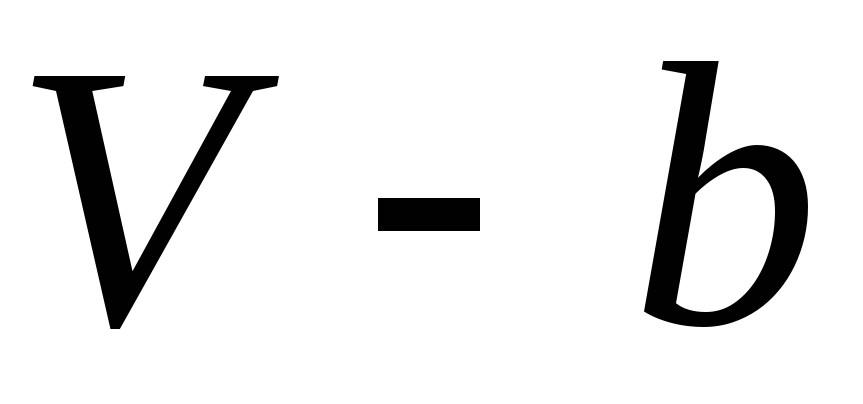 є об’ємом, доступним для молекул
реального газу.
є об’ємом, доступним для молекул
реального газу.
Додатковий
тиск
 в реальних газах виникає за рахунок
слабкої взаємодії поміж молекулами,
якою нехтують для ідеального газу. Сили
взаємодії з боку молекул оточення
взаємно компенсують одна одну для
будь-якої молекули в об’ємі реального
газу внаслідок симетрії їх розташування.
Втім для молекул на межі газу з іншим
середовищем це не так: сили взаємодії
з молекулами газу не компенсують сили
взаємодії з оточуючим середовищем.
Результатом є виникнення поверхневих
сил, нормальних до межі газ-оточуюче
середовище. Саме вони створюють додатковий
тиск в реальному газі.
в реальних газах виникає за рахунок
слабкої взаємодії поміж молекулами,
якою нехтують для ідеального газу. Сили
взаємодії з боку молекул оточення
взаємно компенсують одна одну для
будь-якої молекули в об’ємі реального
газу внаслідок симетрії їх розташування.
Втім для молекул на межі газу з іншим
середовищем це не так: сили взаємодії
з молекулами газу не компенсують сили
взаємодії з оточуючим середовищем.
Результатом є виникнення поверхневих
сил, нормальних до межі газ-оточуюче
середовище. Саме вони створюють додатковий
тиск в реальному газі.
Якщо
припустити, що
 ,
тобто знехтувати виправленнями
Ван-дер-Ваальса, то рівняння Ван-дер-Ваальса
(2.1.17) переходить в рівняння
Мендєлєєва-Клапейрона (2.1.17) для ідеального
газу. Варто також зауважити, що рівняння
Менделєєва-Клапейрона є лінійним
рівнянням відносно об’єму газу
,
тобто знехтувати виправленнями
Ван-дер-Ваальса, то рівняння Ван-дер-Ваальса
(2.1.17) переходить в рівняння
Мендєлєєва-Клапейрона (2.1.17) для ідеального
газу. Варто також зауважити, що рівняння
Менделєєва-Клапейрона є лінійним
рівнянням відносно об’єму газу
 ,
у той час як рівняння Ван-дер-Ваальса –
кубічним, що стає особливо наочним, якщо
переписати його у вигляді:
,
у той час як рівняння Ван-дер-Ваальса –
кубічним, що стає особливо наочним, якщо
переписати його у вигляді:
|

|
(2.1.18)
|
де
 - кількість кіломолей газу.
- кількість кіломолей газу.
|
Факультет
машинобудування
|
|
|
|
Лектор
Дон Н.Л.
|
|
стор.
10 з 10
|

