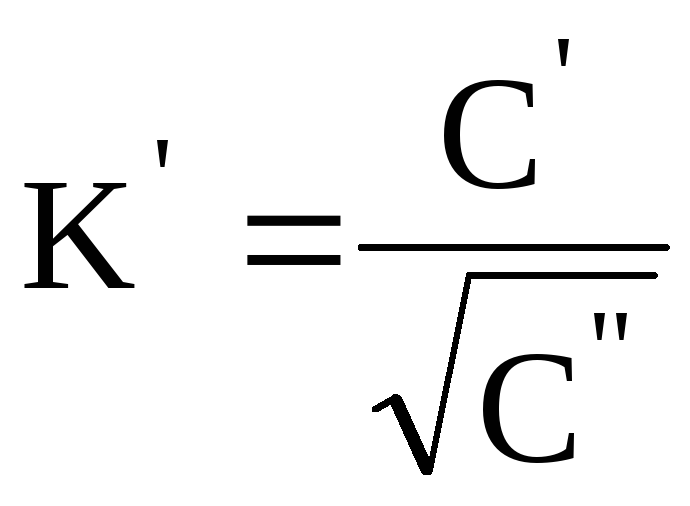- •Лабораторний практикум
- •Фізична хімія
- •Передмова
- •Оформлення результатів вимірювань
- •Складання таблиць
- •Молярна електрична провідність водних розчинів
- •Побудова графіків
- •Розділ і термохімія
- •Лабораторна робота №1 визначення теплової сталої калориметра
- •Запис вимірювання температури під час досліду
- •Лабораторна робота №2 визначення теплоти гідратоутворення купрум (II) сульфату
- •Визначення теплоти нейтралізації сильної кислоти сильною основою у воді
- •Контрольні питання
- •Будова атома і молекули, електричні та оптичні властивості Рефрактометрія
- •Визначення рефракції речовини і встановлення його структури
- •Контрольні питання
- •Хімічна рівновага
- •Визначення залежності константи рівноваги від температури в гомогенній системі
- •Послідовність виконання роботи
- •Розрахунок рівноважних концентрацій речовин
- •Експерементальні данні
- •Контрольні питання
- •Розділ іv фазові рівноваги
- •Побудова та аналіз діаграм плавкості і3 простою евтектикою
- •Типи термопар
- •Визначення кристалізації речовини 3 розчину при низьких температурах
- •Послідовність виконання роботи
- •Лабораторна робота №7 кристалізація бінарних сумішей (система NaNо3 – kno3)
- •Контрольні питання
- •Розділ V розчини
- •Лабораторна робота №8 розподіл речовини між двома рідкими фазами
- •Послідовність виконання роботи
- •Визначення ступеня асоціації оцтової кислоти в бензолі (чи хлороформі)
- •Вивчення процесу екстрагування
- •Контрольні питання
- •Кріоскопія, ебуліоскопія
- •Установка термометра Бекмана для кріоскопії.
- •Лабораторна робота №11 визначення молекулярної маси речовини кріоскопічним методом
- •Послідовність виконання роботи.
- •Визначення молекулярної маси речовини ебуліоскопічним методом (метод визначення молекулярної маси по Сиволобову)
- •Послідовність виконання роботи.
- •Завдання до лабораторної роботи
- •Контрольні питання
- •Електрохімія
- •Водневий показник як кількісна характеристика кислотності-основності розчинів
- •Потенціометрія
- •Визначення рН буферних розчинів
- •Послідовність виконання роботи
- •Контрольні питання
- •Хімічна кінетика
- •Вивчення швидкості йодування ацетону
- •Послідовність виконання роботи
- •Контрольні питання
- •Вивчення швидкості інверсії цукру
- •Теоретичні відомості
- •Послідовність виконання роботи
- •Підготовка до роботи поляриметра
- •Контрольні питання
- •Вивчення кінетики розчинення твердої кислоти у воді
- •Дифузія
- •Послідовність виконання роботи
- •Котрольні питання
- •Додатки
- •Значення деяких фундаментальних сталих
- •Знаки деяких математичних дій
- •Множники і префікси для утворення десяткових кратних і дольних одиниць
- •Густина води при різних температурах
- •Питома електрична провідність 0,01м розчину kСl при різних температурах
- •Інтегральна теплота розчинення солей, які утворюють кристалогідрати, при температурі 18°с.
- •Йонні електричні провідності при нескінченному розведені λ∞
- •Йонні електричні провідності при нескінченному розведені при температурі 25°c
- •Література
- •Періодична система елементів д. І. Менделєєва
Лабораторна робота №8 розподіл речовини між двома рідкими фазами
Мета роботи: Визначення коефіцієнта розподілу бензойної кислоти між органічним розчинником і водою, а також константи асоціації бензойної кислоти в органічному розчиннику.
Послідовність виконання роботи
У мірній колбі на 100 см3 готують розчин бензойної кислоти (наважка 2-4 г) в органічному розчиннику (бензол, толуол, ксилол). Відбирають 50 см3 отриманого розчину піпеткою за допомогою груші і переносять у мірний ціліндр з притертою пробкою. Послідовно з розчину, що залишився, готують ще три робочих розчини (відбираючи 25, 15 і 10 см3 в мірні ціліндри на 50см3), доливають органічний розчинник до мітки 50. У кожен розчин додають по 50см3 другого розчинника - дистильованої води. Мірні ціліндри закривають пробками й енергійно струшують вміст 3-4 рази по 2 хв. з інтервалом у 2 хв., після чого розчини переносять в ділильні лійки і залишають стояти протягом 1год. до повного розшарування рідин (встановлення рівноваги). Шари послідовно розділяють, переносять у колби і з кожної беруть по три проби для титрування піпетками на 5 см3 за допомогою груші. Відібрану пробу переносять у колбу для титрування, додають 2-3 краплі індикатора - фенолфталеїну і 20 см3 дистильованої води, струшують, повільно титрують 0,1 М розчином NaOH до появи забарвлення, що не зникає при енергійному струшуванні колби. Титрування обов'язково повторюють 2-3 рази до одержання близьких результатів (результати повинні відрізнятися не більше ніж на 0,1 см3) і беруть середній результат. Для кожного шару потрібна окрема піпетка.
Концентрацію досліджуваної речовини в кожнім шарі визначають за рівнянням:
|
|
(5.8) |
де V1 і V2 - відліки по бюретці до і після титрування, см3;
V - об'єм взятого для титрування розчину, см3;
![]() - концентрація
лугу, моль/л.
- концентрація
лугу, моль/л.
Усі розчини, що містять органічні розчинники, необхідно зливати в окрему колбу. По закінченні роботи органічний розчинник за допомогою ділильної лійки відокремлюють від водного шару, зливають у банку для збереження залишків.
Отримані дані зводять у табл. 5.1.
По отриманим даним будують залежність СІІ/СІ від СІ і визначають коефіцієнт розподілу речовини між двома рідинами, що незмішуються, по складам фаз і константу асоціації кислоти в органічному розчиннику, по формулі:
|
|
(5.9) |
де К - константа асоціації.
Таблиця 5.1
|
Номер пробірки |
Кількість лугу витраченого на титрування, см3 (мл) | |||||||||
|
Водного шару |
концентрація бензойної кислоти в водному шарі, СІ |
Органічного шару |
концентрація бензойної кислоти в органічному шарі, СІІ | |||||||
|
1-е титрування |
2-е титрування |
3-е титрування |
середнє |
1-е титрування |
2-е титрування |
3-е титрування |
середнє | |||
|
1 2 3 4 … |
|
|
|
|
|
|
|
|
|
|
Лабораторна робота №9