
- •Часть 6. Химический состав живых организмов. Потребности в веществах и энергии
- •Глава 6.1. Элементный состав
- •Супероксиддисмутаза
- •Каталаза
- •Глутатионпероксидаза
- •Витамин е
- •Витамин с
- •Витамин а
- •Биофлавоноиды
- •6.1.7. Щелочноземельные металлы
- •Глава 6.2. Потребность живых организмов в углеводах, липидах, белках и нуклеиновых кислотах
- •Простагландины
- •Лейкотриены
- •Глава 6.3. Витамины
- •Библиографический список
- •Физиологическая химия
Каталаза
Образовавшийся пероксид водорода подвергается превращениям под действием каталазы:
2 Н2О2 → 2 Н2О + О2 (11)
Каталаза (К.Ф. 1.11.1.6) локализована в основном в пероксисомах, где образуются наибольшие количества пероксида водорода, и в лейкоцитах для защиты клеток от последствий «респираторного взрыва» (см. п. 6.1.2.2).
Каталаза в зависимости от структуры относится к одному из трех семейств. Семейство 1 каталаз − это тетрамерные белки, состоящие из больших или малых субъединиц, содержащих гем. Гем включается в фермент во время его сборки в пероксисомах из мономеров, которые гем не содержат. Семейство 2 − это бифункциональные ферменты, проявляющие и каталазную, и пероксидазную активности и являющиеся гемсодержащими асимметричными димерами. Семейство 3 − гексамерные белки, содержащие по два иона марганца на мономер (рис. 6.2).
Реакция, катализируемая семействами 1 и 2 каталаз, состоит из двух стадий: сначала один атом кислорода из пероксида водорода включается в состав молекулы воды, а второй восстанавливается гемом с образованием оксоферрильного порфирин-π-радикального комплекса (compound I) (один электрон передается ионом железа, второй происходит из порфиринового кольца) (см. схему (12)). Во время второй стадии реакции оксоферрильное производное взаимодействует со второй молекулой пероксида водорода с образованием молекул воды, кислорода и восстановлением исходной формы фермента (схема (13)).
Enz (Por-Fe3+) + H2O2 → Cpd I (Por+.-Fe4+ = O) + H2O (12)
Cpd I (Por+.-Fe4+= O) + H2O2 → Enz (Por-Fe3+) + H2O + O2 , (13)
где Enz − каталаза, Por − порфирин, Cpd I − промежуточное производное I (compound I).
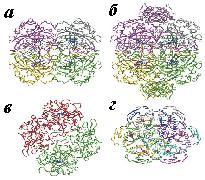
Рис. 6.2. Пространственная структура каталазы: а − тетрамер, состоящий из малых субъединиц (Pseudomonas syringae); б − тетрамер, в состав которого входят большие субъединицы (E. сoli); в − димерная структура бифункционального фермента каталазы-пероксидазы (Burkholderia pseudomallei); г − гексамер Мn2-содержащей каталазы (Lactobacillus plantarum). Гем в структурах а и б изображен синим цветом, ионы Мn в структуре г − красным (согласно [14])
В случае пероксидазной реакции, катализируемой ферментами семейства 2, необходим органический донор электронов для протекания второй стадии (8):
Cpd I (Por+.-Fe4+= O) + 2AH2 → Enz (Por-Fe3+) + 2AH• + H2O, (14)
где AH2 является органическим соединением − донором электронов.
Особенностью этой группы ферментов является наличие в структуре ковалентного аддукта Мet-Tyr-Trp, в случае его отсутствия протекает только пероксидазная реакция.
Каталазы, относящиеся к семейству 3, катализируют реакции превращения пероксида водорода, где роль восстановителя выполняет комплекс из двух катионов марганца:
H2O2 + Mn2+-Mn2+ (2H+) → Mn3+-Mn3+ + 2 H2O (15)
H2O2 + Mn3+-Mn3+ → Mn2+-Mn2+ (2H+) + O2 , (16)
т. е. центр, содержащий два иона марганца, ведет себя аналогично гему в каталазах семейств 1 и 2.
