
- •Федеральное агентство по образованию
- •2.Тесты первого промежуточного контроля знаний по общей химии Контролируемые темы:
- •3.Тесты второго промежуточного контроля знаний по общей химии Контролируемые темы:
- •4.Тесты третьего промежуточного контроля знаний по общей химии Контролируемые темы:
- •5.Образец итогового экзаменационного теста.
5.Образец итогового экзаменационного теста.
Рассчитать молярную массу эквивалента HNO3при ее восстановлении доNO2.
а ) 21 г б) 63 г в) 0,031 г г) 3,1 г
Чему равна молярная масса эквивалента ортофосфорной кислоты в обменных реакциях?
а ) 21 г б) 32,6 в) 31 г г) 27 г
Объем равный 11,2 л занимает: а) 14 г N2б) 2 гH2 в) 8 гO2г) 17 гCl2
Укажите сколько нейтронов в ядре изотопа бария
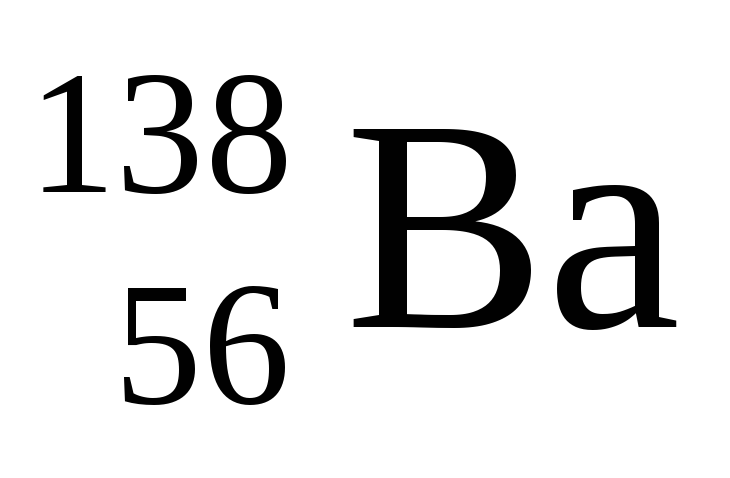 а
)56 б )82 в )138 г ) 194
а
)56 б )82 в )138 г ) 194
Какому иону соответствует формула: 1S22S22P63S23P63d104S2
a)Zn2+ б ) Са2+в )As3+г )Se
На энергетическом уровне с главным квантовым числом, равным 3, максимально может расположиться электронов: а) 2 б) 18 в) 32 г) 26
На каком подуровне энергия электрона максимальна:
а) 2sб) 2p6в) 3d г) 4P
Как меняется электроотрицательность в ряду: F,CI,Br,I?
а ) возрастает, б ) убывает в ) периодически меняется г) остается постоянной.
Для какого элемента справедливо уравнение реакции:
Э2О7+ Н2О ↔ 2НЭО4
а ) Р б ) Nв )CIг )S
Формула высшего оксида элемента, образующего летучий гидрид состава ЭН2:
а ) ЭО б ) ЭО2в ) ЭО4г ) ЭО3
При взаимодействии SO2 с избытком едкого натра образуются:
а ) гидросульфит натрия б ) гидросульфат натрия в ) сульфит натрия и вода г ) сульфат натрия и вода.
В какой смеси веществ возможна химическая реакция?
а ) SO2 + HCI ↔ б ) SO2 + Na2O↔
в ) SO2 + CO2 ↔ г ) SO2 + Na2SO4
В каком из соединений образуется наиболее прочная химическая связь?
а ) LiFб )LiCIв )LiBrг )LiI
Укажите вещества с преимущественно ионным типом связи: а)Na2O б)H2O в)HCl г)H2
Вещества, содержащие только ковалентные полярные связи:
а)H3PO4, BF3, CH3COONH4
б) H2SO4, F2, P2O5
в) PF5, Cl2O7, NH4Cl
г)NO2, SOCl2, CH3COOH
Степень окисления и к.ч. комплексообразователя [Pt(NH3)4CI2]2+
а ) +2;4 б) +4;6 в) +2;6 г) +4; 4
Какой комплексный ион образуется при взаимодействии двух солей CrCl3+ 3KCl: а) [KCl6]3-б)[K3(CrCl6)]3+в) [CrCl6]3-г) [Cr(K3Cl)]3+
Стандартная энтальпия образования SO2равна -297 кДж/моль. Чему равно количество тепла, выделившееся при сгорании 16 г серы:
а) 74,25 кДж б) 148,5 кДж в) 297 кДж г) 594 кДж.
Как изменится скорость прямой реакции 2СО (г)+О2(г)↔2СО2(г), при увеличении концентрации [СО] в 3 раза?
а) увеличится втрое б) увеличится в 9 раз в) не изменится г) уменьшится в 3 раза
Чему равен температурный коэффициент, если при охлаждении на 300С скорость реакции уменьшилась в 8 раз.
а ) 2 б) 3 в) 4 г) 8
Куда сместится равновесие: Ст+ О2(г)↔СО2(г)при увеличении давления?
а) влево б) вправо в) не сместится г) в сторону угла
Смешали 200 г 20%-ного и 300г 10%-ного растворов глюкозы. Концентрация полученного раствора будет:
а) 15% б) 18% в) 16%г) 14%.
При растворении 11,6 г вещества в 400 г воды температура кристаллизации раствора стала составлять 0,93°C. Молярная масса вещества равна, г/моль: а) 93 б) 58 в) 180 г) 342.
Какой из растворов замерзает при более низкой температуре, если молярные концентрации равны?
а) KIб)CuCI2в)NaCIг) С12Н22О11
Указать уравнение реакции, практически осуществимой в растворе:
а) Ва(NО3)2+ NaOH→
б) Fe2(SO4)3+ НNO3→
в) Na NO3+ НCl →
г) CuSO4+ NaOH →
Раствор, в 500 мл которого растворено 1,825 г НCl, имеет рН, равный:
а) 1 б) 4 в) 7 г) 13
Какая из указанных солей дает щелочную реакцию среды за счет гидролиза: а ) Na2CO3б)AlCl3в) (NH4)2SO4г)KNO3
ПР (BaSO4) =1·10-10, ПР (CaSO4) =6·10-5ПР (PbSO4) =1, 8·10-8
Какой осадок при равных условиях образуется первым?
а) CaSO4б)BaSO4в) одновременно г) не образуется
Дисперсной системой является: а)соляной раствор, б) молоко; в) сахар; г) минеральная вода
Для золя AgI, полученного по реакцииAgNO3+KI(изб) =AgI↓ + КNO3коагуляцию вызывают : а)катионы, б) анионы; в) катионы +анионы; г) нейтральные частицы
При растворении в воде ПАВ величина поверхностного натяжения: а)уменьшается, б) не изменяется, ; в) увеличивается; г) уменьшается, затем увеличивается.
Полиэтилен получают в результате реакции: а) вулканизации, б) сополимеризации; в)поликонденсации, г)полимеризации Макромолекулы природного каучука имеют : а) сетчатую структуру, б) разветвленную структуру; в) линейную структуру, г) беспорядочную структуру.
Найдите сумму коэффициентов в уравнении окислительно-восстановительной реакции: Fe(OH)2+O2+H2O→Fe(OH)3а) 10 б) 9 в)11 г) 8
Методы анализа, основанные на способности вещества поглощать свет определенной длины: а)спектрофотометрические, б) потенциометрические, в) радиометрические, г) фотоэмиссионные
При взаимодействии Fe3+с гексацианоферритом (II) калия образуется: а)белый осадок, б) бурый осадок, в) синий осадок, г) красный осадок
