
- •1. Окускування дрібних матеріалів при виробництві кольорових металів. Обдавання, брикетування, агломерація: сутність процесів, їх переваги і недоліки (привести схему агломерації)
- •2. Шихтопідготовка в кольоровій металургії. Вимоги до якості шихт. Бункерний і штабельний способи приготування шихти, їх сутність і вживання (привести схеми приготування шихти)
- •3. Металургійні гази і пил, їх класифікація і характеристика. Технологічні і топкові гази, грубий і тонкий пил кольорової металургії (навести приклади)
- •8. Рафінувальні плавки в кольоровій металургії, їх види і призначення. Вогневе, лікваційне, сульфідуюче, хлорне, карбонільне, цементація рафінування (навести приклади хімічних реакцій)
- •9. Рудні плавки в кольоровій металургії. Плавка на штейн, відновна, електролітична, металотермічна, реакційна плавка (вкажіть призначення і наведіть приклади хімічних реакцій)
- •10. Обпалювання в кольоровій металургії. Кальцінуючий, окислювальний, агломеруючий, відновний, хлоруючий і фторуючий (дайте визначення і наведіть приклади хімічних реакцій)
- •Сушка в оборот
- •16. Збагачення руд кольорових металів. Завдання збагачення руд. Концентрат, проміжний продукт, хвости (дайте визначення і наведіть приклади). Способи збагачення руд
- •18. Руди і мінерали кольорових металів (дайте визначення і наведіть приклади). Класифікація руд і мінералів. Сульфідні, окислені, змішані, самородні, моно- і поліметалічні руди
- •19. Класифікація кольорових металів. Легкі, важкі, рідкісні, благородні метали. Основні властивості і сфери застосування кольорових металів
10. Обпалювання в кольоровій металургії. Кальцінуючий, окислювальний, агломеруючий, відновний, хлоруючий і фторуючий (дайте визначення і наведіть приклади хімічних реакцій)
Обпалювання– металургійний процес, що проводиться при високих температурах (500-12000С) з метою зміни хімічного складу сировини, яка переробляється. Обпалювальні процеси, за винятком обпалювання із спіканням, є твердофазними. У кольоровій металургії застосовують наступні види обпалювання:
1.Кальцінуюче обпалювання (прокалку) проводять з метою розкладання (дисоціації) нагрівом нестійких хімічних сполук – гідроксидів, карбонатів та ін. У загальному вигляді цей вигляд обпалювання описується наступними рівняннями:
Me(ОН)3 Me2O3 + H2O;
MeCO3 MEO + CO2 .
2. Окислювальне обпалювання застосовують для підготовчої обробки сульфідних руд і концентратів з метою повного або часткового перекладу сульфідів в оксиди:
2MеS + 3O2 2MeO + 2SO2 .
До окислювального процесу відноситься і агломеруюче обпалювання(обпалювання із спіканням). Останній має на меті одночасно окислювати і спікати матеріал. Спікання відбувається за рахунок утворення деякої кількості рідкої фази, яка при застиганні зв'язує тугоплавкі дрібні частки в кусковий пористий продукт – агломерат.
3. Відновне обпалювання проводять для відновлення вищих оксидів деяких металів до нижчих, наприклад:
3Fe2O3 + CO 2Fe3O4 + CO2 .
4. Хлоруюче і фторуюче обпалювання проводять з метою перекладу оксидів або сульфідів у водорозчинні або леткі хлориди (фториди).
Al2O3+6HCl=2AlCl3+3H2O .
11. Класифікація металургійних процесів при виробництві кольорових металів. Піро-, гідро- і електрометалургійні процеси, їх коротка характеристика і призначення. Наведіть приклади хімічних реакцій обпалювання, плавки, дистиляції, вилуговування, екстракції, цементації, електролізу
Всі використовувані при виробництві кольорових металів процеси підрозділяють на дві групи:
Пірометалургійні;
Гідрометалургійні.
Пірометалургія- сукупність металургійних процесів, що протікають при високих температурах. По технологічних ознаках виділяють наступні види пірометалургійних процесів: випалення, плавка, конвертація, рафінування, дистиляція.
Обпалення металургійний процес, що проводиться при високих температурах (500-12000С) з метою зміни хімічного складу сировини, яка переробляється. Характеризується тим, що матеріал зберігає твердий стан при зміні складу і деякому укрупненні частинок. Як приклад приведемо рівняння окислювального обпалювання:
2MeS + 3O2 Þ 2MeO + 2SO2.
Плавка- пірометалургійних процес, що проводиться при температурах, що забезпечують в більшості випадків повне розплавленняматеріалу, що переробляється. Розрізняють два різновиди плавок - рудні і рафінувальні. Як приклади приведемо відновну рудну плавку:
(MeO, SiO2, CаO, Fe2O3) + C + O2, N2 = Me + (SiO2, CаO, FеO) + CO2,N2.
Дистиляція(перегін) – процес випару речовини при температурі декілька вище за точку його кипіння, що дозволяє розділити компоненти оброблюваного матеріалу залежно від їх летючості. Дистиляційні процеси можуть використовуватися як для первинної переробки рудної сировини, так і для видалення легколетких домішок при рафінуванні металів або розділенні металевих сплавів. Як приклад, отримання цинку з окисненої сировини. Найбільш леткими в цинкової сировині є кадмій (Ткипіння=7670С) і цинк (Ткипіння=9070С), інші метали-супутники мають більшу Ткипіння>17000С.
T1
ZnO+CO→Znпар+СО2;
T2
CdO+CO→Cdпар+CO2 .
Гідрометалургійні процесипроводяться при низьких температурах на межі розділу, найчастіше твердої і рідкої фаз. Будь-який гідрометалургійний процес складається з трьох основних стадій: вилуговування, очищення розчинів від домішок і осадження металу з розчину.
Вилуговування– процес переведення витягуваних металів в розчин при дії розчинника на матеріали (руду, концентрат тощо), які переробляються, часто у присутності газового реагенту – кисню, водню й ін. Очищення розчинів від домішок проводять з метою запобігання їх попадання у витягуваний метал при подальшому його осадженні у вигляді хімічної сполуки або у вільному стані. Для очищення використовують різні методи, деякі з них приведені нижче.
У основі цементаційного осадження лежить принцип витіснення з розчину одного металу іншим (більш електронегативним). Прикладом цементаційного очищення служить процес виділення міді з сірчанокислих цинкових розчинів цинком:
(CuSО4 + Zn ZnSO4 + Cu).
Електролізвикористовують для обробки розчинів з підвищеним вмістом металів ( ≥ 25-40 г/дм3), застосовуючи нерозчинні аноди. В результаті на катоді відновлюються іони металу:
Меn++ nе = Meк,
а на аноді протікає реакція з утворенням молекулярного кисню:
Н2O+ 2е = 2Н++ 0,5О2.
Екстракція - процес розділення суміші рідких або твердих речовин за допомогою виборчих (селективних) розчинників (екстрагентів).
Процес екстракції включає 3 послідовних стадії: змішання початкової суміші речовин з екстрагентом; механічне розділення (розшарування) двох фаз, що утворюються; видалення екстрагента з обох фаз і його регенерацію з метою повторного використання.
Електрометалургійні процеси, що іноді відокремлюють в окрему групу можуть бути як піро-, так і гідрометалургійними. Особливістю електрометалургійних процесів є використання електроенергії як рушійної енергетичної сили для їх протікання. Електроліз - фізико-хімічне явище, що полягає у виділенні на електродах складових частин розчинених речовин або інших речовин, вторинних реакцій, що є результатом, на електродах, яке виникає при проходженні електричного струму через розчин або розплав електроліту.
Процес описується наступною схемою:
MеO (MeCl2) Me2+ + O2- (2Cl-).
Me2+ + 2e Me - на катоді;
O2- - 2e O2 або 2Cl- - 2e Cl2 на аноді.
В результаті на катоді виділяється метал (у рідкому або твердому стані), а на аноді – газ.
12. Вогнетривкі матеріали і їх класифікація за вогнетривкістю і характером хімічної активності оксиду, який служить вогнетривкою основою. Кремнеземні, алюмосилікатні, магнезійні, хромисті, вуглецеві вогнетриви. Робочі властивості вогнетривів
Для спорудження плавильних печей і ряду інших агрегатів, а також для створення в них внутрішнього захисного облицювання, яке називається футеровкою, використовують найчастіше вогнетривкі матеріали. Вогнетривкими називають будівельні матеріали, що витримують без розплавлення температури до 1600ºC і більше. За своїм складом вони, в основному, представляють оксидні системи. Вогнетривкі матеріали залежно від їх фізико-хімічних властивостей класифікуються за вогнетривкістю, хіміко-мінералогічним складом, хімічній активності оксидів й рядом інших характеристик.
Вогнетривкість – стійкість матеріалів при тривалій дії температур. За вогнетривкістю вироби підрозділяють на вогнетривкі (1580-1770ºС), високовогнетривкі (1770-2000ºС) й вищої вогнетривкості (більше 2000ºС).
За хіміко-мінералогічним складом вогнетривкі матеріали класифікують на наступні основні групи:
кремнеземні – вогнетривка основа SiO2 (динасові, кварцове скло)
алюмосилікатні – вогнетривка основа А12О3 і SiO2 (напівкислі, шамотні і високоглиноземисті)
магнезійні – основа MgO (магнезитові, доломітові, шпинельні, форстеритові)
хромисті – основа Cr2O3 · MgO (хромітові, хромомагнезитові)
вуглецеві – основа вуглець (графітові, вугільні, карборундові).
За характером хімічної активності оксиду, який служить вогнетривкою основою, вогнетриви бувають кислі (SiO2) і нейтральні (Аl2О3), а також основні (MgO, CаO).
Вогнетриви повинні володіти наступними робочими властивостями:
термічна стійкість;
здатність зберігати в процесі експлуатації первинний об'єм і форму.
пористість або газопроникність;
теплопровідність;
електропровідність та ряд інших властивостей.
13. Металургійне паливо. Класифікація його за агрегатним станом і способом здобуття (наведіть приклади основних видів палива). Теплотворна здатність палива. Повнота згорання палива (наведіть приклади реакцій згорання палива). Коефіцієнт надлишку дуття
Необхідні температури в металургійних процесах досягаються спалюванням палива або за рахунок використання електроенергії. Паливомназиваються речовини, які в процесах хімічних або ядерних перетворень здатні виділяти значну кількість теплоти, здобич і широке використання яких економічно доцільно. Основні різновиди палива мають органічне походження. До складу палива входять C, H2, S, O2, N2, присутні у вигляді різних з'єднань, які складаютьгорючу масу. Крім того, в паливі можуть міститися вода і зола –негорюча частина. Органічне паливо - це вуглецеві або вуглеводневі з'єднання, здібні вступати в реакцію окислення з киснем повітря з виділенням великої кількості теплоти.
За агрегатним станомрозрізняють тверде (кокс, брикети, деревне вугілля), рідке (розчини солей ) і газоподібне паливо (природний, доменний, генераторний, коксівний газ), а заспособом здобуття– природне (природний газ, копаливні вугілля) і штучне (доменний газ, кокс, брикети). Штучне паливо отримують в результаті направленої переробки природного палива. У металургії прагнуть використовувати тільки високоякісне паливо з високою теплотворною здатністю і низьким вмістом золи. Цим вимогам найбільшою мірою задовольняють природний газ, мазут, кокс і висококалорійний кам'яне вугілля.
У ряді металургійних процесів вуглецеві матеріали, крім функцій палива , виконують роль відновників. При спалюванні палива виділяється теплова енергія, кількість якої тісно пов'язана з хімічним складом палива й умовами його спалювання. Кількість тепла, яке виділяється при спалюванні палива, називається теплотою згорання палива або його теплотворною здатністю. Теплота згорання виражається в наступних одиницях: кДж/кг, кДж/м3 або кДж/моль. Наведемо приклади деяких реакцій згорання палива:
C + O2= CO2+ 34070кДж/кг
H2 + 1/2 O2 = H2O + 241800 кДж/моль
CH4 + 2O2 = CO2 + 2H2O + 35800 кДж/м3
Горіння палива здійснюється за рахунок кисню дуття: повітря (21%(об.) О2), суміші повітря з киснем або технологічного кисню (95-98%(об.) О2). Повнота спалювання палива характеризується коефіцієнтом надлишку дуття (α). Якщо кількість дуття відповідає теоретично необхідному для повного спалювання палива, то α = 1. При недостатності дуття α < 1, при його надлишку α > 1.
14. Дроблення і подрібнення рудної сировини кольорових металів. Крупне, середнє, дрібне дроблення, тонке подрібнення. Міра дроблення (подрібнення), (щокові, конусні, валкові і молоткасті дробарки, барабанні млини (намалюйте схему і поясніть принцип дії)
Дроблення в техніці, процес руйнування шматків твердого матеріалу для зменшення їх розміру. Дроблення принципово не відрізняється від подрібнення. Умовно вважають, що при дробленні отримують продукти більше, а при подрібненні дрібніше 5 мм.
Для витягання мінералів і відділення їх один від одного руду потрібно роздрібнити і подрібнити. При тісному взаємному зрощенні мінералів для їх розділення потрібне подрібнення до 0,2 мм і дрібніше. Міра дроблення (подрібнення) є відношенням діаметрів найбільших шматків руди (D) до діаметру шматків продукту подрібнення (d): K = D / d. Дроблення і подрібнення руди зазвичай ведуть в декілька стадій з використанням дробарок і млинів різних типів. Наведемо розміри шматків продуктів на кожній стадії: крупне дроблення - 100...300 мм, середнє дроблення – 10...50 мм, дрібне –3...10 мм, тонке – 0,05...2,0 мм й менше.
Для дроблення руд кольорових металів найчастіше застосовують щічні, конусні, валкові і молоткасті дробарки. У щокових дробарках дроблення руди відбувається при наближенні щоки, що гойдається, і нерухомо закріпленою щокою. Щокові дробарки – апарати періодичної дії. Це є основним недоліком щокових дробарок, які мають нижчу продуктивність в порівнянні з конусними дробарками безперервної дії. Дроблення в конусних дробарках здійснюється в кільцевому просторі між двома усіченими конусами. Валкові дробарки з гладкими і рифленими валками застосовують для дрібного дроблення. Вихідний матеріал подається в дробарку зверху захоплюється валками, які обертаються назустріч один одному, дробиться і розвантажується вниз під дробарку. В конусній дробарці подрібнення здійснюється в результаті гойдання внутрішньої конусної голоакі по нерухомій конусній воронці.
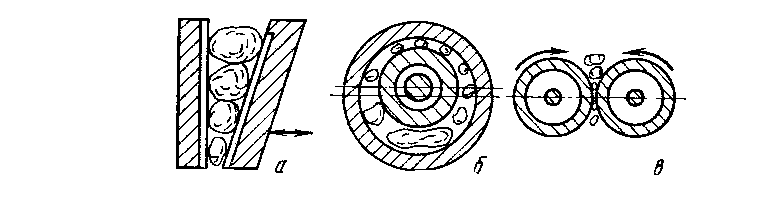
Рисунок 1. – Схема подрібнення в дробарках:
а – щоковій, б – конусній, в - валковій.
Молотко́ва дроба́рка — дробарка для середнього та дрібного дроблення з робочим органом у вигляді ротора з шарнірно закріпленими на ньому ударними елементами — молотками (рис. 2).
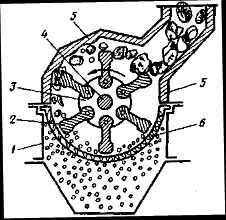
Рис. 2 - Молоткова дробарка:
1 – корпус; 2 – молоток; 3 – диск; 4 – вал; 5 – броньова плита; 6 – решето.
Для подрібнення кускових матеріалів до крупності часток менше ніж 1,2 мм використовують барабанні млини (рис. 3), які залежно від вигляду тіл, що дроблять, діляться на кульові, стержневі, самоподрібнюючі тощо. Наприклад, в кульовому млині 95% вихідного матеріалу подрібнюється металевими кулями до розмірів менш за 0,075 мм. Млини ефективно працюють тільки при певному ступені подрібнення, тому для отримання тонкого продукту подрібнення часто ведуть в два, рідше в три прийоми (стадії).
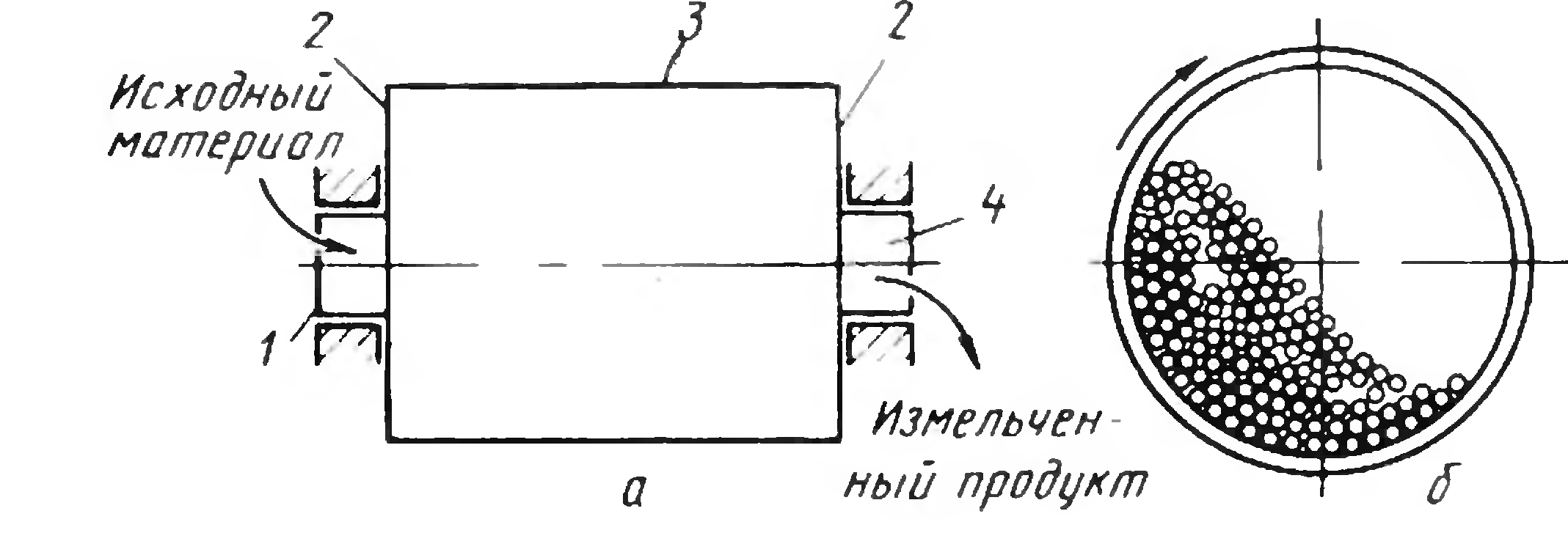
Рисунок 3. – Схема облаштування (а) і роботи (б) барабанного млину.
