
- •Содержание
- •Тема 6. Жесткость воды и реакции солей жесткости в водных растворах
- •Часть 2
- •Тема 7. Окислительно-восстановительные реакции и их использование
- •Тема 8. Электрохимические системы и процессы (базовый материал)……81
- •Часть 3
- •Введение
- •1. Темы лабораторных работ
- •Тема 1. Химическая термодинамика (базовый материал)
- •Тема 2. Скорость химических реакций и методы ее регулирования (базовый материал)
- •Тема 3. Химическое равновесие (базовый материал)
- •Тема 4. Гетерогенные химические системы и поверхностные явления в них (спецраздел с элементами уирс) (базовый материал)
- •5.1 Электролитическая диссоциация и водородный показатель среды (рН)
- •5.2 Реакции обмена в растворах электролитов, в том числе гидролиз
- •5.3 Представление о химическом анализе
- •Тема 6. Жесткость воды и реакции солей жесткости в водных растворах (базовый материал)
- •2 Список рекомендуемой литературы
- •Часть 2
- •1. Темы лабораторных работ
- •Тема 7. Окислительно-восстановительные реакции и их использование в химическом анализе (базовый материал)
- •Тема 8 Электрохимические системы и процессы (базовый материал)
- •Лабораторная работа № 8.3 Электролиз растворов электролитов
- •2. Список рекомендуемой литературы
- •Часть 3
- •1. Темы и методики лабораторных работ
- •Тема 9. Отличительные реакции углеводородов различных классов
- •Описание опытов
- •Лабораторная работа № 9. 1 Качественные реакции предельных и непредельных углеводородов
- •Тема 10. Химические свойства и качественная идентификация гидроксипроизводных углеводородов
- •10.1 Кислотные свойства спиртов и фенолов
- •10.2 Основные свойства спиртов и фенолов
- •10.3 Реакции спиртов в качестве нуклеофилов
- •10.4 Нуклеофильное замещение он-группы спиртов
- •10.5 Окисление спиртов
- •Лабораторная работа № 10. 1
- •Тема 11. Химические свойства и качественная идентификация карбонильных соединений
- •Лабораторная работа № 11.1
- •Тема 12. Химические свойства и качественная идентификация карбоновых кислот
- •12.1 Электролитическая диссоциация
- •12.2 Декарбоксилирование карбоновых кислот
- •12.3 Реакции нуклеофильного замещения групп он в карбоксильной группе
- •Лабораторная работа № 12.1
- •Вопросы для защиты лабораторных работ и подготовки к экзамену по разделу "Химические свойства и типичные реакции органических соединений"
- •Список рекомендуемой литературы
- •350072, Г. Краснодар, ул. Московская, 2, кор. А
Тема 12. Химические свойства и качественная идентификация карбоновых кислот
Рекомендуемая литература приведена на с. 128.
Функциональным признаком карбоновых кислот является наличие в их молекулах карбоксильных групп, которые сочетают в себе связанные гидроксильную и оксо- группы:
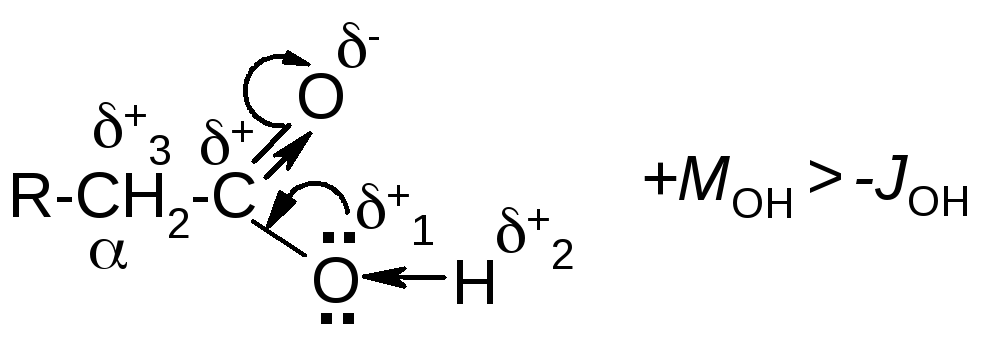
Между этими группами существует индуктивный и мезомерный эффекты, среди которых преобладает положительный мезомерный эффект группы ОН. В результате такого влияния на атомах карбоксильной группы возникают указанные выше частичные заряды. В целом вся карбоксильная группа оказывает электроноакцепторное действие на связанный с ней углеродный остаток.
Такое строение карбоксильной группы и взаимное влияние в ней атомов обусловливают следующие виды химических взаимодействий:
– проявление кислотных свойств в результате разрыва связи О-Н (реакции электролитической диссоциации и нейтрализации);
– нуклеофильное и электрофильное присоединение по группе С=О;
– нуклеофильное замещение ОН-группы;
– разложение группы СООН с выделением СО2 (реакция декарбоксилирования);
– замещение атомов водорода, связанных с углеродом в -звене.
В свою очередь, по углеводородному остатку также проходят различные химические реакции, обусловленные его химическим строением.
Ниже приведены примеры наиболее характерных и качественных реакций карбоксильной группы.
12.1 Электролитическая диссоциация
Это обратимый распад молекул кислоты на ионы под действием полярных молекул воды при ее растворении:
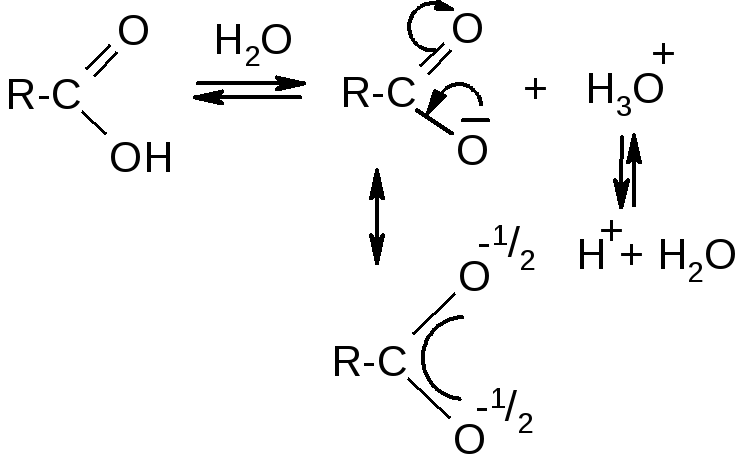
Этот процесс в присутствии воды проходит мгновенно и обусловливает значения рН раствора меньше 7. Это и является аналитическим сигналом. Легкость протекания этой реакции связана с тем, что в данном случае в группе О-Н оба атома имеют + (см. схему на с. 22). С другой стороны, при диссоциации образуется карбоксианион, в котором имеется сопряжение, что обусловливает его относительную устойчивость.
Примечательно, что в ряду органических соединений только для карбоновых кислот характерно свойство при растворении изменять рН воды вследствие их электролитической диссоциации.
На способность карбоновых кислот диссоциировать, т.е. на значение их констант диссоциации, оказывает влияние строение углеводородных остатков и характер имеющихся в них заместителей. Так, электроноакцепторные заместители повышают + на карбоксильном атоме углерода, а следовательно, и + 1 на кислороде ОН-группы, и тем самым облегчают диссоциацию. Электронодонорные заместители действуют наоборот.
Многоосновные кислоты диссоциируют в две стадии, при этом на первой стадии карбоксильные группы проявляют взаимное электроноакцепторное действие.
Например:
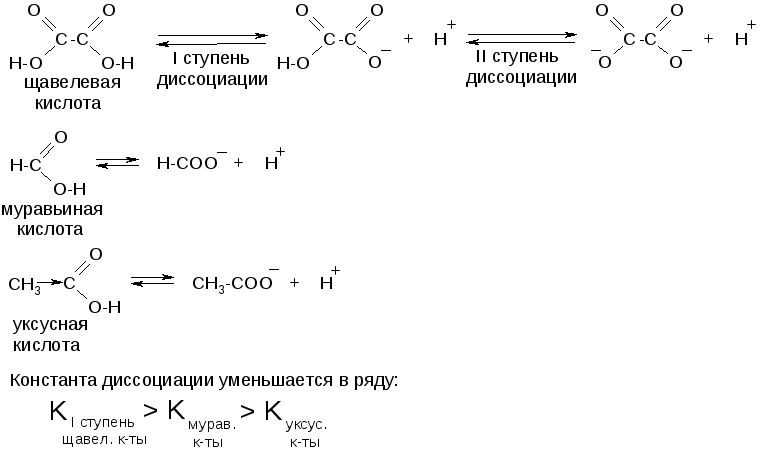
12.2 Декарбоксилирование карбоновых кислот
В карбоксильных группах карбоновых кислот указанные связи
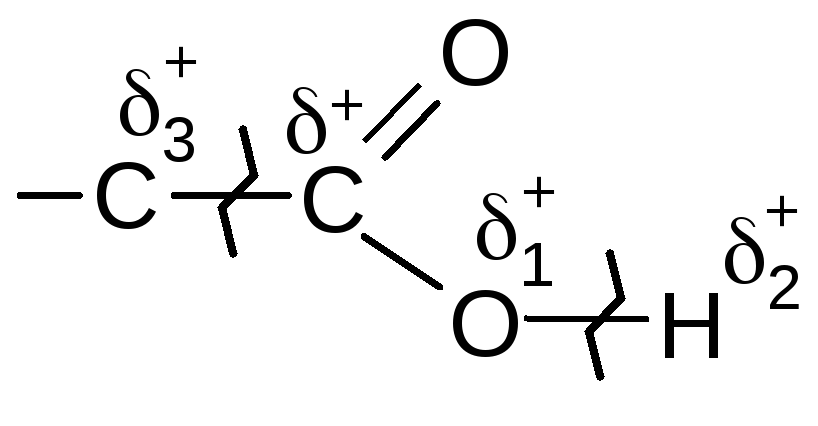
ослаблены в результате пониженной электронной плотности на связанных атомах. В связи с этим при нагревании свыше 120-180 0С (в зависимости от строения молекул кислоты) карбоксильная группа разлагается с выделением СО2, который легко обнаружить при пропускании через раствор Са(ОН)2. Например:
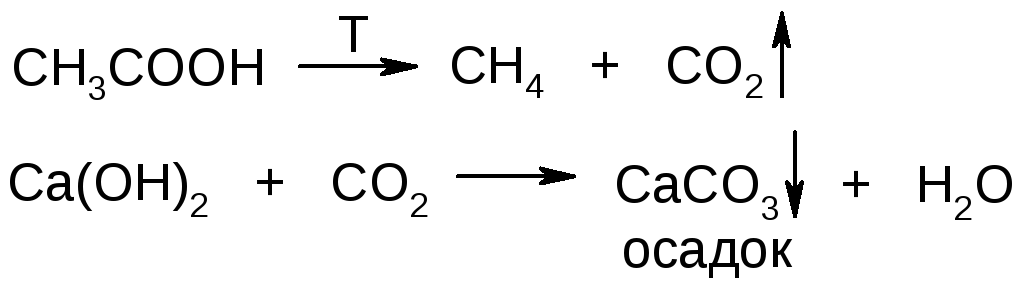
Это и является аналитическим сигналом. Такие реакции называются "декарбоксилирование" и в ряду органических соединений они характерны только для карбоновых кислот.
