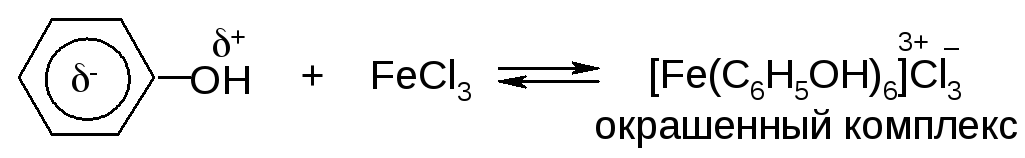- •Содержание
- •Тема 6. Жесткость воды и реакции солей жесткости в водных растворах
- •Часть 2
- •Тема 7. Окислительно-восстановительные реакции и их использование
- •Тема 8. Электрохимические системы и процессы (базовый материал)……81
- •Часть 3
- •Введение
- •1. Темы лабораторных работ
- •Тема 1. Химическая термодинамика (базовый материал)
- •Тема 2. Скорость химических реакций и методы ее регулирования (базовый материал)
- •Тема 3. Химическое равновесие (базовый материал)
- •Тема 4. Гетерогенные химические системы и поверхностные явления в них (спецраздел с элементами уирс) (базовый материал)
- •5.1 Электролитическая диссоциация и водородный показатель среды (рН)
- •5.2 Реакции обмена в растворах электролитов, в том числе гидролиз
- •5.3 Представление о химическом анализе
- •Тема 6. Жесткость воды и реакции солей жесткости в водных растворах (базовый материал)
- •2 Список рекомендуемой литературы
- •Часть 2
- •1. Темы лабораторных работ
- •Тема 7. Окислительно-восстановительные реакции и их использование в химическом анализе (базовый материал)
- •Тема 8 Электрохимические системы и процессы (базовый материал)
- •Лабораторная работа № 8.3 Электролиз растворов электролитов
- •2. Список рекомендуемой литературы
- •Часть 3
- •1. Темы и методики лабораторных работ
- •Тема 9. Отличительные реакции углеводородов различных классов
- •Описание опытов
- •Лабораторная работа № 9. 1 Качественные реакции предельных и непредельных углеводородов
- •Тема 10. Химические свойства и качественная идентификация гидроксипроизводных углеводородов
- •10.1 Кислотные свойства спиртов и фенолов
- •10.2 Основные свойства спиртов и фенолов
- •10.3 Реакции спиртов в качестве нуклеофилов
- •10.4 Нуклеофильное замещение он-группы спиртов
- •10.5 Окисление спиртов
- •Лабораторная работа № 10. 1
- •Тема 11. Химические свойства и качественная идентификация карбонильных соединений
- •Лабораторная работа № 11.1
- •Тема 12. Химические свойства и качественная идентификация карбоновых кислот
- •12.1 Электролитическая диссоциация
- •12.2 Декарбоксилирование карбоновых кислот
- •12.3 Реакции нуклеофильного замещения групп он в карбоксильной группе
- •Лабораторная работа № 12.1
- •Вопросы для защиты лабораторных работ и подготовки к экзамену по разделу "Химические свойства и типичные реакции органических соединений"
- •Список рекомендуемой литературы
- •350072, Г. Краснодар, ул. Московская, 2, кор. А
Тема 10. Химические свойства и качественная идентификация гидроксипроизводных углеводородов
Рекомендуемая литература приведена на с. 128.
К гидроксипроизводным углеводородов относятся спирты и фенолы. В молекулах алифатических и ароматических спиртов гидроксильные группы связаны с атомами углерода, орбитали которых имеют sp3-гибридизацию. В молекулах фенолов гидроксильные группы связаны с атомами углерода ароматического цикла, орбитали которых находятся в состоянии sp2-гибридизации.
Химические свойства спиртов и фенолов как нельзя лучше подтверждают положения теории химического строения А.М. Бутлерова о том, что строение определяет свойства соединений, а зная свойства, можно судить о строении, а также о взаимном влиянии атомов в молекуле.
Распределение электронной плотности в молекулах спиртов и фенолов определяется электронными эффектами, возникающими в результате взаимного влияния атомов.
Например, в спиртах:
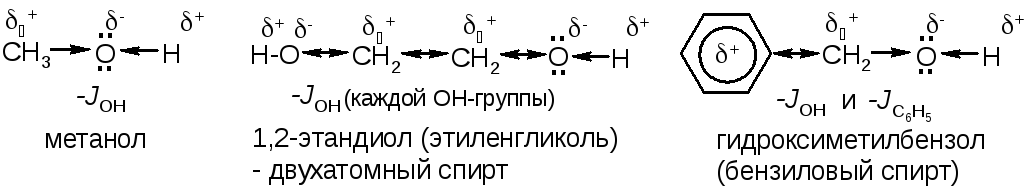
В фенолах:
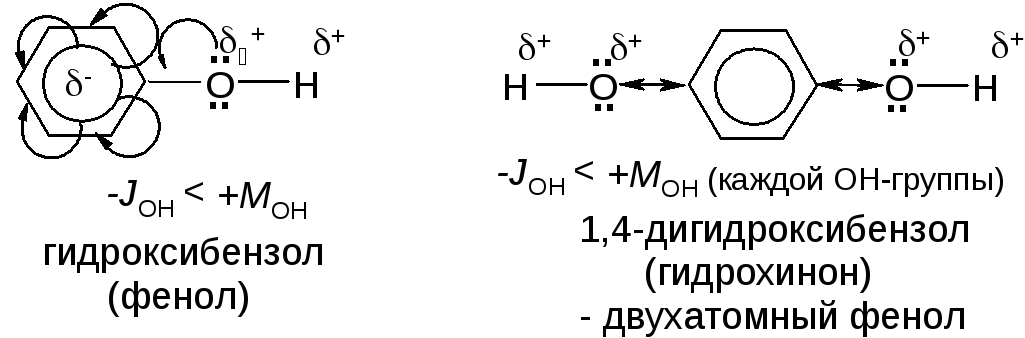
Исходя из приведенных схем распределения электронной плотности, прогнозируются свойства спиртов и фенолов:
10.1 Кислотные свойства спиртов и фенолов
Кислотные свойства их групп ОН весьма слабые. При этом они больше выражены у фенолов, чем у спиртов, т.к. в молекулах фенолов на кислороде понижена электронная плотность (+), и электронодефицитный водород (Н+) слабее удерживается в группе ОН. По этой причине фенолы обратимо взаимодействуют со щелочами (реакция нейтрализации), а спирты нет. Кислотные свойства одноатомных спиртов проявляются только в реакциях с активными металлами (окислительно-восстановительная реакция замещения водорода ОН-групп спиртов на металл).
В молекулах многоатомных спиртов ОН-группы оказывают друг на друга электроноакцепторное действие, поэтому - на атоме кислорода в этих группах ниже, чем у одноатомных спиртов, и их кислотность несколько выше. По этой причине многоатомные спирты вступают в реакции с гидроксидами d-металлов, например Cu(OH)2. Такие соединения способны также взаимодействовать с ОН-группами спиртов по донорно-акцепторному типу, что обусловливает образование устойчивых комплексных солей:
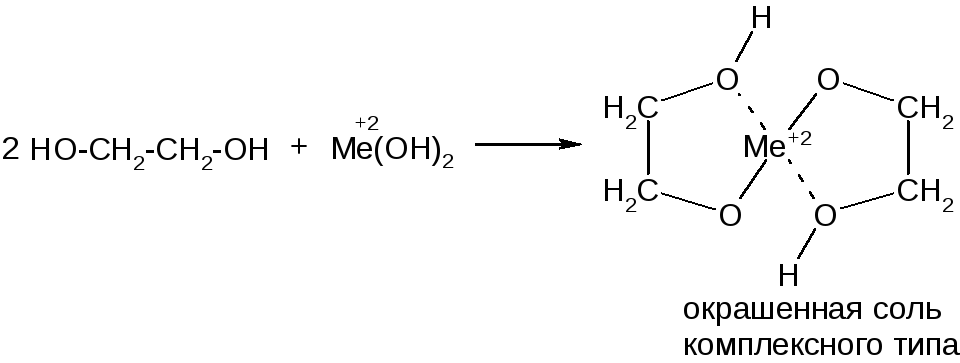
10.2 Основные свойства спиртов и фенолов
В молекулах спиртов на атоме кислорода имеются неподеленные электронные пары и повышена электронная плотность, поэтому они способны присоединять протон, проявляя слабые основные свойства. Например, это имеет место в реакциях дегидратации спиртов, которые проводятся в кислых средах:
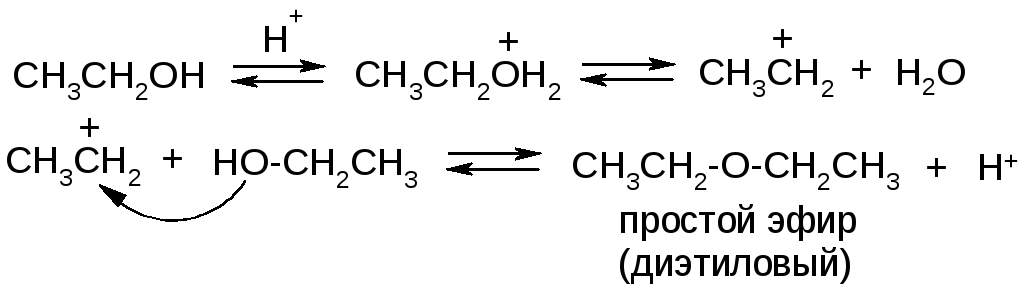
Для фенолов основные свойства не характерны, т.к. в их молекулах электронная плотность на атоме кислорода понижена.
10.3 Реакции спиртов в качестве нуклеофилов
Наличие на атоме кислорода спиртов неподеленных электронов и повышенной электронной плотности обусловливает их нуклеофильные свойства в реакциях с карбоновыми кислотами (реакция этерификации), производными кислот, а также с другими реагентами, в молекулах которых имеется атом-электрофил (с пониженной электронной плотностью).
Например, реакция алкилирования:
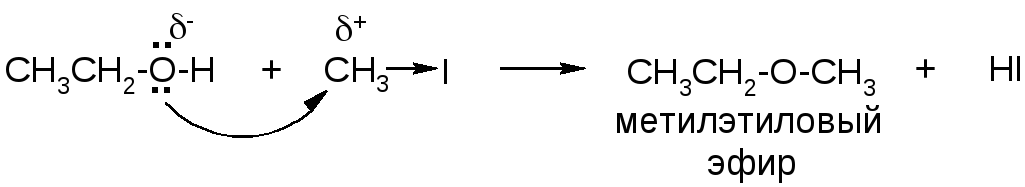
Фенолы не проявляют нуклеофильных свойств за счет ОН-группы, т.к. на атоме кислорода в их молекулах электронная плотность понижена. Однако в ароматическом ядре фенолов электронная плотность повышена за счет преобладающего мезомерного эффекта ОН-группы. В результате -электронная сопряженная система ядра выступает в качестве донора электронов (лиганда) при образовании комплексных соединений с некоторыми солями, например, FeCl3, катионы которых выполняют роль комплексообразователя: