
- •Введение. Общие вопросы фармакологии.
- •Определение фармакологии и ее место среди других медико-биологических наук. Цели и задачи фармакологии.
- •Природа лекарств. Основные понятия лекарствоведения.
- •Источники получения лекарственных средств. Пути изыскания новых лекарств. Основные этапы их внедрения в медицинскую практику.
- •Фармакологический и Фармакопейных комитеты и их назначение. Национальная и международная фармакопея.
- •Принципы классификации лекарственных средств
- •Понятие о международных непатентованных и фирменных (торговых) наименованиях лекарств.
- •Научная информация о лекарственных средствах
- •Фармакокинетика
- •Пути и способы введения лекарственных средств в организм. Сравнительная характеристика. Факторы, обуславливающие выбор пути введения и лекарственной формы.
- •Основные механизмы проникновения лекарства через биологические мембраны. Факторы, влияющие на процессы абсорбции лекарств.
- •Понятие о биодоступности
- •Транспорт и распределение лекарств
- •Элиминация лекарств
- •Биотрансформация лекарств. Несинтетические и синтетические реакции метаболизма.
- •Индивидуальные различия в скорости метаболизма лекарств
- •Эффект первого прохождения. Пролекарства. «Суицидальные» лекарства.
- •Выведение лекарственных средств из организма
- •Количественные законы элиминации лекарств. Кинетика элиминации первого и нулевого порядка.
- •Клиренс и период полуэлиминации, их значение для управления режимом дозирования.
- •Принципы дозирования лекарств. Доза, ее способы и варианты введения.
- •Дискретное (прерывистое) введение лекарств
- •Непрерывное внутрисосудистое введение
- •Терапевтический лекарственный мониторинг
- •Фармакоэкономические понятия
- •Фармакодинамика
- •Механизмы возникновения первичной фармакологической реакции. Природа рецепторов.
- •Взаимодействие лекарственных веществ с рецепторами.
- •Теории взаимодействия лекарственных веществ с рецепторами.
- •Соотношение между концентрацией лекарственного вещества и его фармакологическим эффектом Градуальная и квантовая кривые зависимости «доза-эффект»
- •Зависимость действия лекарств от их структуры, физико-химических свойств, лекарственной формы и путей введения.
- •Проблема биоэквивалентности лекарственных средств
- •Взаимодействие лекарственных средств
- •Усиление эффектов комбинации лекарств
- •Ослабление эффектов комбинации лекарств
- •Лекарственная несовместимость
- •Механизмы взаимодействия лекарств
- •Нежелательное действие лекарств
- •Реакции типа в
- •Реакции типа с
- •Реакции типа е
- •Значение индивидуальных особенностей организма для реализации действия лекарств
- •Общие принципы лечения отравлений
- •Фармакология синаптической передачи в периферической нервной системе
- •Станислав Лем
- •Передача импульсов в вегетативной нервной системе.
- •Характеристика холинорецепторов
- •Основные этапы холинергической передачи и их фармакологическая коррекция
- •Характеристика адренорецепторов
- •Основные этапы адренергической передачи и их фармакологическая коррекция
- •Эффекты активации симпатических и парасимпатических нервов
- •Неадренергический и нехолинергический отдел вегетативной нервной системы.
- •Холинергческие средства. Холинергические агонисты.
- •Классификация холинергических агонистов
- •М-холиномиметические средства
- •М,н-холиномиметики
- •М,н-холиномиметики прямого действия
- •Непрямые м,н-холиномиметики (антихолинэстеразные средства)
- •Интоксикация фос
- •Реактиваторы холинэстеразы
- •Н-холиномиметики
- •Стимуляторы высвобождения ацетилхолина
- •Холинергические антагонисты
- •Новые селективные антагонисты м-холинорецепторов
- •Отравление м-холиноблокирующими средствами
- •Ганглиоблокирующие средства (нн-холиноблокаторы)
- •Миорелаксанты (нм-холиноблокаторы)
- •Антидеполяризующие миорелаксанты
- •Деполяризующие миорелаксанты
- •М,н-холинонегативные средства
- •Средства для наркоза
- •Классификация средств для наркоза.
- •Ингаляционные анестетики
- •Неингаляционные анестетики
- •Фв: флаконы с порошком по 0,5 и 1,0
- •Противопаркинсонические средства
- •Противоэпилептические и противосудорожные средства
- •Рд: Терапевтические дозы составляют 1800-3600 мг в день.
- •Фв: капс. 100, 300 и 400 мг
- •Фэ: табл. По 25, 50 и 100 мг, табл. Жевательные по 5, 25 и 100 мг
- •Опиоидные (наркотические) анальгетики
- •Витамины и витаминоподобные средства. Средства, влияющие на процессы тканевого дыхания. Биогенные стимуляторы
- •Жирорастворимые витамины.
- •Водорастворимые витамины13.
- •Витаминоподобные средства
- •Поливитаминные средства
- •Классификация витамин-содержащих препаратов
- •Средства, влияющие на процессы тканевого дыхания Общие представления о физиологии и патофизиологии тканевого дыхания.
- •Определение понятий и классификация
- •Классификация лекарственных средств, влияющих на процессы тканевого дыхания:
- •Биогенные стимуляторы
Водорастворимые витамины13.
Тиамина хлорид (Thiamine
chloride, Vitamin
B1)Тиамин описан в литературе как витамин
В1, витаминFили
аневрин. В кристаллическом состоянии
он стабилен при температуре 100С.
Водные растворы тиамина при рН < 5,0
устойчивы к действию высоких темпер атур
и окислителей, при рН > 5,0 они достаточно
быстро разрушаются при автоклавировании,
а при рН > 7,0 – даже при кипячении. Если
рН раствора превышает 8,0 то тиамин быстро
образует окрашенные в желтый цвет
комплексы, которые через ряд необратимых
реакций быстро утрачивают витаминную
активность.
атур
и окислителей, при рН > 5,0 они достаточно
быстро разрушаются при автоклавировании,
а при рН > 7,0 – даже при кипячении. Если
рН раствора превышает 8,0 то тиамин быстро
образует окрашенные в желтый цвет
комплексы, которые через ряд необратимых
реакций быстро утрачивают витаминную
активность.
Пищевая роль. Несмотря на то, что тиамин широко распространен в продуктах растительного и животного происхождения, основным его источником являются:
-
Источник
Содержание мг/100 г массы
Дрожжи
Нежирная свинина
Плоды бобовых
6-24
0,72-1,04
0,53-1,00
В незначительном количестве тиамин синтезируется микрофлорой кишечника, но при этом нет убедительных данных, что синтез тиамина в кишечнике является доступным источником витамина.
Суточная потребность в тиамине составляет 1,0-2,0 мг, но может изменяться в зависимости от количества потребляемых углеводов. В среднем считают, что необходимо0,3 мг тиамина на каждые 1000 ккал пищи.
Таблица 4. Суточная потребность в витаминах для разных категорий людей.
|
Витамин |
Новорожденные |
Дети до 5 лет |
Взрослые |
Беременные |
|
A K E D |
1200-1500 МЕ 5-10 мкг 4-5 мг 400 МЕ |
1500-3000МЕ 15 мкг 7-10 мг 400 МЕ |
3000-5000МЕ 1 мкг/кг веса 12-30 мг 400 МЕ |
5000-8000МЕ 65 мкг 15-30 мг 400 МЕ |
|
C B1 B2 PP B6 B12 BC B5 |
20-30 мг 0,3-0,5 мг 0,4-0,6 мг 3-8 мг 0,3-0,5 мг 0,3 мкг 40-50 мкг 3 мг |
20-45 мг 0,7-1,2 мг 0,8-2,0 мг 9-13 мг 0,6-1,4 мг 1,5-3,0 мкг 100-300 мкг 5 мг |
30-60 мг 1-2 мг 1,5-3,0 мг 15-20 мг 1,6-2,0 мг 2-4 мкг 200-400 мкг 10-12 мг |
60-80 мг 1,7-2,0 мг 2,0 мг 20 мг 2,5 мг 4-8 мкг 600-800 мкг 10 мг |
МД: В организме тиамин в стенке кишечника превращается при участии АТФ в моно-, ди- и трифосфаты. Наиболее активной является дифосфатная форма – тиаминпирофосфат, которая выступает в роли кофермента следующих ферментов:
Пируватдекарбоксилазы – фермент обеспечивает окислительное декарбоксилирование пировиноградной кислоты с образованием ацетил-КоА, который в дальнейшем используется для синтеза жирных кислот, стероидных гормонов, ацетилхолина.
-кетоглутаратдегидрогеназы – фермент цикла трикарбоновых кислот, обеспечивает синтез НАДН·Н+, необходимый для образования АТФ.
Транскетолазы – фермент пентозофосфатного пути превращения углеводов. Участвует в синтезе нуклеотидов, жирных кислот и аминокислот.
ФК: Тиамин можно вводить внутрь, внутримышечно и внутривенно (в последнем случае только капельно, очень медленно). Всасывание тиамина в кишечнике происходит в его проксимальных отделах, главным образом, путем активного транспорта, при помощи специальной Na+/тиамин-АТФазы. Насыщение фермента происходит в дозе 10 мг тиамина (2 мкмоль/л). В более высоких дозах часть витамина может поступать путем пассивной диффузии.
Еще в процессе всасывания тиамин подвергается фосфорилированию в коферментные формы в стенке кишечника и печени. Транспорт тиамина в крови происходит в связанном с альбуминами состоянии. Тиамин хорошо проникает во все органы и ткани (в том числе и через гематоплацентарный барьер, при этом его концентрация у плода превышает уровень витамина в крови матери). Наибольшие количества тиамина содержат скелетные мышцы (50% всего количества), миокард, печень и мозг.
Элиминация тиамина осуществляется путем его деградации в печени (при этом образуется до 10 метаболитов, которые удаляются с мочой). Период полуэлиминации тиамина 9-18 дней. Всего в сутки метаболизируется до 1 мг тиамина.
ФЭ:
Тиамин регулирует углеводный обмен, обеспечивает его взаимосвязь с процессом липогенеза.
За счет декарбоксилирования пировиноградной, -кетоглутаровой кислот и других-кетокислот тиамин позволяет быстро ликвидировать метаболический ацидоз.
Облегчает нервно-мышечную проводимость. Данный эффект связан, по крайней мере, с двумя механизмами. С одной стороны, тиамин ингибирует активность холинэстеразы и замедляет, тем самым, разрушение ацетилхолина. За счет увеличения концентрации медиатора в нейро-мышечных синапсах передача импульсов облегчается. Кроме того, было установлено, что фосфорилированные формы тиамина (тиаминпирофосфат и тиаминтрифосфат) могут связываться с Na+-каналами скелетных мышц вблизи воротного механизма. При прохождении нервного импульса, тиамин дефосфорилируется и открывает натриевые каналы даже в отсутствии медиатора, вызывая при этом мышечное сокращение.
Показания к применению и режимы дозирования:
Лечение авитаминоза В1 («бери-бери»). Различают 2 формы болезни – «сухую» и «влажную».
«Сухая» бери-бери проявляется в основном неврологическими симптомами – полиневритами с выпадением чувствительности, гиперестезиями (ощущением покалывания и ползанья «мурашек»). Развивается мышечная слабость и атрофии мышц, которые проявляются симптомами «свисающих кистей и стоп» (пациент не может удерживать кисть и стопу на весу в горизонтальном положении). Наблюдаются нарушения мышления, памяти, замедление психических процессов. Со стороны ЖКТ отмечается потеря аппетита, запор.
«Влажная» бери-бери чаще проявляется у детей первых лет жизни. Ведущими являются кардиальные симптомы. Возникает тахикардия, одышка, кардиомегалия и другие симптомы сердечной недостаточности (но сердечный выброс при этом остается высоким, а не сниженным, как при классической форме сердечной недостаточности; это связано с тем, что на фоне дефицита тиамина происходит гиперактивация холинэстеразы и разрушение ацетилхолина с преобладанием симпатического тонуса). Возникающий дефицит белка приводит к снижению онкотического давления плазмы и развитию массивных отеков (анасарки).
Лечение проводят путем внутримышечного или внутривенного введения тиамина в дозе 100 мг/сут до исчезновения симптомов заболевания, затем назначают поддерживающие дозы по 5-10 мг/сут внутрь.
Лечение энцефалопатии Вернике и Корсаковского психоза у лиц, страдающих хроническим алкоголизмом. Метаболизм этанола протекает путем его окисления до ацетил-КоА и требует, поэтому, большого количества тиамина для работы дегидрогеназ. Вследствие этого у пациентов возникает дефицит тиамина в нервной системе. Энцефалопатия Вернике проявляется спутанностью сознания, параличом глазодвигательных мышц (офтальмоплегия), нистагмом, тремором рук. Для Корсаковского психоза характерно сочетание фиксационной амнезии (выпадения памяти на только что произошедшие события) с симптомами полиневрита. Лечение проводят высокими дозами тиамина по 100 мг/сут внутримышечно.
Лечение редких наследственных заболеваний, связанных с нарушением обмена витамина В1:
Лейциноз – нарушение декарбоксилирования аминокислот с разветвленной боковой цепью (лейцин, валин, изолейцин) вследствие дефицита дегидрогеназ -кетокислот. Проявляется накоплением этих аминокислот в ткани мозга и вытеснением из синапсов естественных медиаторов – ГАМК и глютаминовой кислоты. Основные симптомы заболевания – приступы цианоза, ригидность мышц, тонико-клонические судороги, остановки дыхания – возникают через несколько дней после рождения ребенка. Моча приобретает запах кленового сиропа. Лечение проводят высокими дозами тиамина (10-20 мг/сут новорожденным и 50-100 мг/сут детям до 5 лет) и переводом ребенка на вскармливание искусственными смесями, лишенными разветвленных аминокислот.
Тиамин иногда применяют в высоких дозах внутривенно очень медленно (100 мг) для экстренного оказания помощи (временного протрезвления) при тяжелой алкогольной интоксикации. Полагают, что действие тиамина связано с тем, что он включается в процессы метаболизма ацетил-КоА и резко усиливает тем самым окисление этанола.
В настоящее время тиамин довольно часто назначают в неврологии для лечения всевозможных невритов, невралгий, парезов, рассчитывая при этом на эффект, аналогичный таковому при лечении невритов у лиц с бери-бери. Однако, до настоящего времени нет убедительных доказательств об эффективности тиамина при этих состояниях, равно как и при использовании его для коррекции астенических состояний, иммунодефицитов, экземы и псориаза.
НЭ: Прием тиамина может вызвать развитие аллергических реакций, вплоть до анафилактического шока.
Синаптоплегия – состояние, которое возникает при быстром внутривенном введении тиамина, в результате чего создается очень высокая концентрация лекарства в крови и тиамин приобретает способность образовывать комплексы с различными медиаторами. При этом развивается падение АД, аритмия, нарушение мышечных сокращений (вплоть до паралича дыхательных мышц), угнетение ЦНС.
ФВ: таблетки по 2, 5 и 10 мг; раствор 2,5 и 5% в ампулах по 1 мл.
Р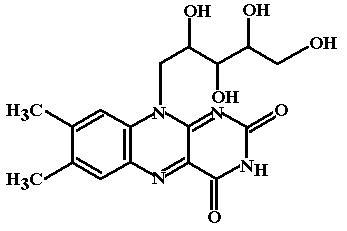 ибофлавин
(Riboflavin, Vitamin
B2)Является желтым флавоновым пигментом,
который содержится в молоке, яйцах,
печени, зеленых листьях растений, зернах
злаков. Часть рибофлавина в организме
человека синтезируется флорой толстой
кишки, однако не известно, способен ли
всасываться этот витамин. Суточная
потребность в рибофлавине составляет
около 1,5-3,0 мг или приблизительно 0,4 мг
на 1000 ккал пищи.
ибофлавин
(Riboflavin, Vitamin
B2)Является желтым флавоновым пигментом,
который содержится в молоке, яйцах,
печени, зеленых листьях растений, зернах
злаков. Часть рибофлавина в организме
человека синтезируется флорой толстой
кишки, однако не известно, способен ли
всасываться этот витамин. Суточная
потребность в рибофлавине составляет
около 1,5-3,0 мг или приблизительно 0,4 мг
на 1000 ккал пищи.
МД: В организме рибофлавин превращается в коферментные формы – ФМН (флавинмононуклеотид) и ФАД (флавинадениндинуклеотид), которые входят в состав ферментов из группы оксидаз и редуктаз (т.к. они образуют окислительно-восстановительную систему), а также дыхательных цепей.
ФК: Рибофлавин назначают внутрь, он хорошо всасывается в тонком кишечнике активным транспортом, сопряженным с переносом ионов натрия. Рибофлавиновые транспортеры полностью насыщаются при приеме доз 25 мг. В организме наибольшие количества витамина содержатся в сердце, печени, почках и мозге. Экскреция витамина осуществляется почками.
ФЭ:
Рибофлавин формирует редокс системы дыхательных цепей и обеспечивает тканевое дыхание и нормальное функционирование бессосудистых эпителиальных тканей (хрусталик, эпидермис и др.).
Рибофлавин необходим для синтеза катехоламинов, т.к. он входит в состав фенилаланин-гидроксилазы и обеспечивает синтез L-ДОФА – предшественника дофамина и норадреналина в ЦНС и надпочечниках.
Рибофлавин стимулирует синтез эритропоэтина – основного стимулятора эритропоэза.
Рибофлавин входит в состав моноаминооксидаз (обеспечивают разрушение катехоламинов) и ксантиноксидазы (обеспечивает разрушение пуринов и синтез мочевой кислоты).
Показания для применения и режимы дозирования. В настоящее время единственным показанием для применения рибофлавина является лечение авитаминоза – арибофлавиноза. Арибофлавиноз – крайне редкая форма авитаминоза, которая может возникнуть у пациентов с тяжелыми заболеваниями ЖКТ, сопровождающимися нарушением кишечной абсорбции питательных веществ (синдромом мальабсорбции). Основные симптомы арибофлавиноза могут быть объединены в 3 группы:
Изменения эпителиальных тканей: наблюдается выпадение волос, развитие сосудов в роговице глаза, катаракта (помутнение хрусталика), себорейный фолликулярный кератоз носогубных складок;
Изменения ЖКТ: хейлоз (воспаление красной каймы губ), ангулярный стоматит («заеды» - трещинки в углах рта), глоссит (воспаление слизистой оболочки языка, его «фуксиновая» пигментация), спру-подобные нарушения (обильная зловонная диарея с остатками пищи в фекалиях);
Изменения ЦНС: ипохондрия, депрессия, судороги мышц и жжение подошв.
В чистом виде арибофлавиноз редок, как правило он протекает как компонент полигиповитаминоза. Рибофлавин назначают внутрь по 2-20 мг/сут в зависимости от тяжести состояния.
НЭ: Крайне редко может вызвать аллергические реакции, иногда способен привести к зеленой флуоресценции мочи (за счет образования люмохромов).
ФВ: порошок для приготовления растворов; таблетки по 2, 5 и 10 мг.
К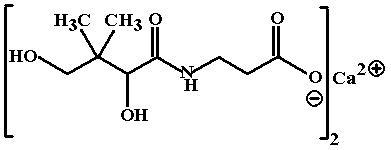 альция
пантотенат (Calcii
pantothenas, Pantotene)МД: Пантотеновая кислота образована
пантоевой кислотой и-аланином.
При участии витамина В6в печени
может происходить синтез пантотеновой
кислоты из этих предшественников. В
организме человека пантотеновая кислота
присоединяет остаток-меркаптоэтиламина
и превращается в пантетеин (незаменимый
фактор роста йогуртообразующих бактерий
–Lactobacillus bulgaricus).
После того, как пантетеин соединяется
с АТФ образуется коэнзим А – активная
форма витамина, с которой и связывают
его биологическую активность – участие
в транспорте ацетата и других ацильных
групп.
альция
пантотенат (Calcii
pantothenas, Pantotene)МД: Пантотеновая кислота образована
пантоевой кислотой и-аланином.
При участии витамина В6в печени
может происходить синтез пантотеновой
кислоты из этих предшественников. В
организме человека пантотеновая кислота
присоединяет остаток-меркаптоэтиламина
и превращается в пантетеин (незаменимый
фактор роста йогуртообразующих бактерий
–Lactobacillus bulgaricus).
После того, как пантетеин соединяется
с АТФ образуется коэнзим А – активная
форма витамина, с которой и связывают
его биологическую активность – участие
в транспорте ацетата и других ацильных
групп.
С уточная
потребность в пантотенате составляет
10-12 мг. Наиболее богаты им маточное
молочко пчел, икра тунца и трески.
уточная
потребность в пантотенате составляет
10-12 мг. Наиболее богаты им маточное
молочко пчел, икра тунца и трески.
ФК: После перорального или внутримышечного введения пантотеновая кислота хорошо всасывается и проникает в разные ткани, создавая наибольшие концентрации в печени, надпочечниках, сердце и почках. Выводится в неизмененном виде почками (70%) и печенью (30%).
ФЭ:
Регулирует жировой обмен. Входит в состав ацилпереносящего белка пальмитат-синтазного комплекса (обеспечивает синтез липидов). Необходим для активации жирных кислот при первом этапе их -окисления.
Обеспечивает процесс синтеза холестерина, стероидных гормонов, желчных кислот. Конденсация ацетил-КоА до мевалоновой кислоты – ключевая стадия синтеза всех этих соединений.
Обеспечивает синтез ацетилхолина в нейронах вегетативной и соматической нервной системы, облегчает передачу в холинергических синапсах.
Ацил-КоА переносит кислотные остатки на молекулы белков и жиров, модифицируя таким образом их функции:
Обеспечивает ацетилирование N-конца полипептидной цепи и регулирует, тем самым, посттрансляционный процессинг белков. Так, в гипофизе в процессе трансляции образуется-меланоцитстимулирующий гормон. Затем в средней доле гипофиза этот гормон ацетилируется и не разрушается, выполняя гормональную функцию. В передней доле гипофиза ацетилирования-МСГ не происходит и он быстро расщепляется протеазами до-эндорфина – гормона антиноцицептивной системы.
Обеспечивает ацетилирование аминокислот внутри полипептидной цепи (обычно это -аминогруппы остатков лизина). Так, например, микротрубочки клеток образованы димерами- и-молекул тубулина. Ацетилирование-тубулина усиливает процесс его полимеризации, а деацетилирование – усиливает процесс его деградации. Ацетилирование гистоновых белков Н4, Н3, Н2А и Н2В (которые образуют ядро нуклеосомы) вызывает дестабилизацию нуклеосом и раскручивание ДНК для последующей транскрипции.
КоА переносит на белки остатки жирных кислот (обычно это миристиковая кислота – С14класс и пальмитиновая кислота – С16класс). Миристоилированию подвергаются белки наN-конце которых расположен глицин: цитохромb5, цАМФ-зависимая протеинкиназа, кальцинейрин,-субъединицаG-белка. Без присоединения миристиковой кислоты все они не способны выполнять свою функцию. Миристоилированию подвергаются тяжелые цепи иммуноглобулинов в В-лимфоцитах – это обеспечивает их перенос в комплекс Гольджи и подготавливает к секреции из клетки. Пальмитоилированию подвергаются в процессе синтеза трансглютаминаза (белок кератиноцитов, который встроен в их мембрану и обеспечивает плотную адгезию клеток друг к другу), сурфактант легких, гликопротеин желудка.
В форме сукцинил-КоА принимает участие в синтезе протопорфириновых колец гема гемоглобина и цитохромов. Конденсация сукцинил-КоА с образование -аминолевулиновой кислоты – ключевая стадия синтеза гема.
Оказывает выраженное анаболическое действие. По величине анаболического эффекта превосходит все другие витамины. Полагают, что в основе анаболического действия пантотената лежат несколько механизмов:
Пантотенат оказывает «экономизирующее воздействие» на основной обмен, снижает процессы катаболизма, в первую очередь за счет уменьшения окисления белка. Фактически происходит перераспределение окислительных процессов: доля окисляемых белков снижается, а доля жиров возрастает.
Под влиянием пантотената потенцируются эффекты инсулина и снижается уровень глюкозы в крови. Это способствует синтезу и выбросу соматотропного гормона гипофизом. Под влиянием СТГ резко усиливаются процессы синтеза белка.
Пантотенат усиливает процессы стероидогенеза и образования эндогенных андрогенов – дигидроэпиандростерона и тестостерона, которые также усиливают синтез белка.
Пантотенат увеличивает абсорбцию ионов калия в кишечнике и его поступление в мышцы. Ионы калия участвуют в процессах реполяризации мышц и обеспечивают эффективные мышечные сокращения.
Установлено, что прием пантотената повышает общую переносимость физических нагрузок и выносливость, способствует приросту мышечной ткани.
Показания для применения. Несмотря на такое многообразие эффектов нет научно обоснованных показаний для применения пантотената: его дефицит у человека не описан, а у животных воспроизведен только экспериментально.
В настоящее время его применяют эмпирически при следующих состояниях:
Паралитическая форма кишечной непроходимости (например, у послеоперационных больных). Назначают по 300 мг каждые 6 часов внутрь или внутримышечно. Курс лечения до 2 месяцев.
Лечение хронической надпочечниковой недостаточности. Применяют внутрь по 200-400 мг 1-2 раза в день. Показано, что введение пантотената таким пациентам резко увеличивает количество в моче 17-кетостероидов (косвенный признак усиления функции коры надпочечников).
В спортивной медицине пантотенат применяют в период интенсивных тренировочных нагрузок (предсоревновательная подготовка и участие в соревнованиях) в дозах от 400 до 2000 мг/сут.
НЭ: Иногда при приеме пантотената возникает тошнота, рвота, изжога.
ФВ: порошок для приготовления растворов; таблетки по 100 мг; раствор 20% в ампулах по 2 мл.
Никотиновая кислота (Nicotinic acid, Niacin, Vitamin PP)Ниацин – генерический собирательный термин, который обозначает как саму никотиновую кислоту, так и никотинамид. В настоящее время рекомендуют пользоваться именно этим названием витамина РР, поскольку слова «никотиновая кислота» достаточно часто ассоциируются у пациентов с никотином, содержащимся в табаке. Такие ассоциации могут вызвать неадекватное отношение пациента к лечению, тем более, что на самом деле ничего общего между алкалоидом табака и никотиновой кислотой нет.
П ищевая
роль. В пище свободная форма ниацина
встречается в очень малых количествах.
Бóльшая часть ниацина находится в
составе НАД и НАДФ, а также в виде эфирных
комплексов с углеводами (ниацетин) и
пептидами (ниациногены), которые
содержатся в злаках и имеют крайне
низкую биодоступность. Наиболее важными
пищевыми источниками ниацина являются
мясо (печень), рыба, бобовые, некоторые
орехи (арахис) и злаковые. Кофе и чай
также содержат этот витамин в приемлемых
количествах. При обжаривании зеленый
кофейных зерен тригонеллин
(1-метил-никотиновая кислота) превращается
в никотиновую кислоту.
ищевая
роль. В пище свободная форма ниацина
встречается в очень малых количествах.
Бóльшая часть ниацина находится в
составе НАД и НАДФ, а также в виде эфирных
комплексов с углеводами (ниацетин) и
пептидами (ниациногены), которые
содержатся в злаках и имеют крайне
низкую биодоступность. Наиболее важными
пищевыми источниками ниацина являются
мясо (печень), рыба, бобовые, некоторые
орехи (арахис) и злаковые. Кофе и чай
также содержат этот витамин в приемлемых
количествах. При обжаривании зеленый
кофейных зерен тригонеллин
(1-метил-никотиновая кислота) превращается
в никотиновую кислоту.
В кукурузе и маисе ниацин содержится в достаточно большом количестве, но при этом он связан с углеводами в плохоусваиваемый ниацетин. Однако, в странах Центральной Америки, Мексике при изготовлении маисовых лепешек мука подвергается щелочной обработке (например, известковой водой), которая приводит к высвобождению ниацина и его биодоступность резко возрастает.
Суточная потребность в ниацине составляет 15-20 мг или 6,6 мг на 1000 ккал пищи (но не менее 13 мг/сут). Следует учитывать, что ниацин – витамин, который может самостоятельно синтезироваться в организме человека. Его предшественником является незаменимая аминокислота триптофан, которая при участии витамина В6трансформируется в хинолиновую кислоту, а затем, через ряд стадий в НАД (см. схему 3). Установлено, что 60 мг триптофана позволяют синтезировать 1 мг ниацина (т.н. ниациновый эквивалент). В связи с этим по мнению ряда экспертов можно питаться продуктами вообще лишенными ниацина, поскольку белок содержит1% триптофана и диета, включающая более 100 г белка позволит обеспечить организм 1000 мг триптофана или 16,6 мг ниацинового эквивалента.
МД: Витаминное действие ниацина связывают с образованием из него в организме НАД (никотинамидаденин динуклеотида) и НАДФ (никотинамидаденин динуклеотид фосфата).

Схема 3. Образование активных форм витамина РР. ФРПФ – фосфорибозил пирофосфат, ПФ – пирофосфат, глн – глутамин, глу – глутаминовая кислота.
ФК: Ниацин при введении внутрь быстро всасывается в желудке и начальных отделах двенадцатиперстной кишки. Ниацин единственный из витаминов, который всасывается одновременно двумя механизмами – облегченным транспортом при помощи переносчика и водной диффузией. После абсорбции в кровь ниацин быстро депонируется в печени и эритроцитах (эритроцитарное депо содержит запасы, обеспечивающие потребность организма в течение 30 сут, печень50-60 сут).
ФЭ:
В настоящее время известно более 200 ферментов, кроферментами которых являются НАД и НАДФ. В форме НАД ниацин обеспечивает катаболические реакции (распад гликогена, окисление глюкозы) и работу дыхательных цепей. В форме НАДФ ниацин обеспечивает анаболические процессы – синтез белка, липидов, холестерина и стероидных гормонов.
Обеспечивает работу фермента поли-АДФ-рибозил трансферазы, который принимает участие в репарации и репликации ДНК, дифференцировке клеток (особенно кроветворного ряда).
Ниацин оказывает антиагрегантное действие (тормозит агрегацию тромбоцитов за счет уменьшения продукции тромбоксана А2и выброса простациклина из эндотелия), повышает активность фибринолитической системы. При парентеральном введении он расширяет артериолы. Более подробно данный эффект ниацина охарактеризован в обзоре, посвященном средствам, влияющим на свертывание крови.
Ниацин участвует в реактивации родопсина после завершения акта фоторецепции. Он обеспечивает переход транс-формы ретинола в его цис-форму.
В больших (не витаминных) дозах ниацин оказывает гиполипидемическое действие – снижает синтез ЛПОНП и увеличивает включение холестерина в антиатерогенные ЛПВП. Более подробно данный эффект ниацина обсуждается в разделе, посвященном гиполипидемическим средствам.
Применение. Как витаминное средство ниацин следует применять только по следующим двум показаниям:
Лечение авитаминоза – пеллагры. Пеллагра представляет собой симптомокомлекс, который включает синдром «трех Д – деменции, диареи и дерматита»:
Деменциальный синдром – проявляется возникновением приступов необьяснимой тоски, ухудшения памяти, головных болей, бессонницы, онемения и парестезий конечностей. В последующем (через 2-3 года) появляются слуховые и обонятельные галлюцинации, эпилептиформные припадки.
Диарейный синдром – диарея, сопровождающаяся стоматитом, глосситом, слюнотечением, тошнотой и рвотой.
Дерматит – на коже рук, ног и лица появляются высыпания, которые напоминают солнечные ожоги, в последующем высыпания чернеют, подсыхают в виде корочек и трескаются.
Для лечения пеллагры ниацин применяют в дозе 200-500 мг/сут, разделенной на 2 приема внутрь или внутримышечно. Улучшение наступает через 24-48 часов (хотя дерматит может сохраняться в течение нескольких недель).
Лечение болезни Хартнупа – рецессивное наследственное заболевание, при котором нарушается абсорбция триптофана. Ниацин назначают в дозе 25-100 мг/сут внутрь.
Кроме этих показаний ниацин применяют для лечения следующих патологий в дозах, которые отличаются от физиологических витаминных доз:
Лечение дислипопротеинемий и атеросклероза – по 3,0-9,0 г/сут по специальной схеме.
Лечение облитерирующих заболеваний периферических сосудов (эндартериит, тромбангиит) и состояний, сопровождающихся повышенным риском тромбоза – вводят внутримышечно или внутривенно по специальной схеме. (Подробнее данные показания и режимы дозирования обсуждаются в соответствующих разделах.)
НЭ: Быстрая абсорбция ниацина из ЖКТ или его парентеральное введение вызывают выброс гистамина из депо и активацию кининовой системы плазмы. У 50% пациентов это приводит к появлению весьма неприятного симптомокомплекса:
Падение АД с появлением эпизодов головокружения;
Покраснение верхней половины туловища, крапивница, кожный зуд, зуд и жжение при мочеиспускании;
Увеличение секреции желудочного сока, боли в эпигастральной области, изжога.
Данных симптомов можно избежать, если начать прием ниацина с минимальных доз (12,5 мг/сут) и постепенно на 12,5 мг/сут повышать дозу до достижения желаемой. За 30 мин до приема ниацина можно назначить 250-300 мг ацетилсалициловой кислоты или Н1-гистаминоблокатор, которые также уменьшат выраженность данного симптомокомплекса.
При длительном применении высоких доз ниацина могут появиться следующие симптомы:
Со стороны ЖКТ: анорексия, рвота, язвенные поражения, диарея, нарушение функции печени (повышение уровня трансминаз). Полагают, что гепатотоксический эффект высоких доз ниацина связан с тем, что он обедняет гепатоциты метильными радикалами (происходит интенсивное включение метила в процессы биосинтеза и уровень его доноров в клетке падает, способствуя развитию жировой дистрофии). Чтобы предотвратить или ослабить нежелательное воздействие ниацина на печень при использовании его высоких доз рекомендуют одновременно назначать доноры метильных групп – метионин, холина хлорид, L-карнитин;
Со стороны сердечно-сосудистой системы: мерцательная аритмия;
Со стороны обмена веществ: гипергликемия, гиперурикемия;
Со стороны кожи: acantosisnigricans– появление на коже ног черных пятен, покрытых «бархатными» ворсинчатыми выростами.
ФВ: порошок, таблетки по 50, 100, 500 мг; раствор 0,1% в ампулах по 1 мл.
Никотинамид (Nicotinamide)Амид никотиновой кислоты (ее витамер). По механизму действия и витаминной активности полностью идентичен ниацину.
В отличие от никотиновой кислоты не
оказывает сосудорасширяющего действия,
не влияет на обмен холестерина и синтез
липопротеинов.
отличие от никотиновой кислоты не
оказывает сосудорасширяющего действия,
не влияет на обмен холестерина и синтез
липопротеинов.
Никотинамид переносится лучше, чем ниацин, поскольку он не вызывает рилизинга гистамина и активации кининовой системы. При его применении редко возникает падение артериального давления, появление кожной сыпи и зуда.
ФВ: таблетки по 15, 25 и 50 мг; раствор 1 и 2,5% в ампулах по 1 и 2 мл.
П иридоксина
гидрохлорид (Pyridoxine
hydrochloride, Vitamin
B6)Витамин В6существует в форме 3
витамеров, отличающихся заместителями
в 4-ом положении пиридинового кольца:
пиридоксин (С4гидроксиметил),
пиридоксаль (С4формил) и пиридоксамин
(С4метиламин). В печени человека
эти витамеры могут переходить один в
другой.
иридоксина
гидрохлорид (Pyridoxine
hydrochloride, Vitamin
B6)Витамин В6существует в форме 3
витамеров, отличающихся заместителями
в 4-ом положении пиридинового кольца:
пиридоксин (С4гидроксиметил),
пиридоксаль (С4формил) и пиридоксамин
(С4метиламин). В печени человека
эти витамеры могут переходить один в
другой.
Пищевая роль. Суточная потребность в витамине В6составляет 2 мг для мужчин и 1,6-2,2 мг для женщин. Поскольку биологическая роль витамина тесно связана с обменом белка, то рекомендуемое количество витамина составляет 0,016-0,032 мг/г белка пищи.
Витамин В6широко распространен в продуктах питания – животные продукты содержат пиридоксаль и пиридоксамин, растительные – пиридоксин. Наиболее богаты витамином В6следующие пищевые продукты:
-
Источник
Содержание мг/100 г массы
Семена подсолнечника
Пшеничные отруби
Куриная грудинка
Соевые бобы
Грецкие орехи
Авокадо
Картофель
0,997
0,903
0,700
0,627
0,535
0,443
0,394
МД: В печени все витамеры пиридоксина трансформируются в пиридоксаль, который подвергается фосфорилированию в коферментную форму – пиридоксаль фосфат. Присоединение кофермента к апобелку фермента происходит после того, как пиридоксаль фосфат образует основание Шиффа, которое фиксируется к -аминогруппам остатков лизина в белке ферменте.
ФК: Пиридоксин хорошо всасывается при введении внутрь или парентерально причем процесс абсорбции витамина в тонком кишечнике происходит путем пассивной диффузии и не является насыщаемым. Транспорт пиридоксина в крови протекает в связанном с альбуминами и гемоглобином эритроцитов состоянии. Основным депо пиридоксина в организме являются скелетные мышцы, которые содержат 80-90% всего пиридоксина организма.
Выведение пиридоксина происходит с мочой в форме неактивной пиридоксовой кислоты. Период полуэлиминации составляет 25-33 дня.
ФД: В настоящее время известно более 100 ферментов, использующих пиридоксаль фосфат в качестве кофермента. Основными являются трансаминазы, которые обеспечивают переаминирование -кетокислот и синтез заменимых аминокислот.
В мышцах пиридоксаль фосфат входит в состав гликогенфосфорилазы и обеспечивает гликогенолиз.
Пиридоксаль фосфат входит в состав кинурениназы – фермента, который обеспечивает синтез из триптофана витамина РР.
Пиридоксаль фосфат обеспечивает работу декарбоксилаз в периферических тканях и ЦНС. Под влиянием этих ферментов происходит синтез основных центральных медиаторов:
Глютаминовая кислота трансформируется в ГАМК;
Тирозин трансформируется в дофамин и норадреналин;
Триптофан переключается с кинуренинового пути метаболизма в ЦНС на серотониновый и трансформируется в серотонин (5-гидрокси-триптамин). Кинуренины являются возбуждающими медиаторами, тогда как серотонин выступает в роли тормозного.
Таким образом, витамин В6 принимает участие в регуляции возбудимости ЦНС.
Пиридоксаль фосфат стимулирует синтез -аминолевулиновой кислоты порфиринового кольца гема, увеличивает синтез сидерофиллина – железо-связывающего белка костного мозга.
Пиридоксаль фосфат связывается с -аминогруппами лизина на поверхности тромбоцитов и фибриногена, вызывая тем самым замедление свертываемости крови и агрегации тромбоцитов.
Пиридоксаль фосфат связывается с -аминогруппами лизина в аллостерических центрах рецепторов для стероидных гормонов (эстрогенов, андрогенов, гестагенов и кортикостероидов), препятствуя их транслокации в ядро клетки и реализации эффекта этих рецепторов.
Применение и режимы дозирования. Дефицит пиридоксина в изолированной форме практически не встречается: уживотных авитаминоз удавалось воспроизвести только экспериментальным путем, у человека описано всего 3 случая изолированного авитаминоза. В настоящее время пиридоксин применяют при следующих состояниях:
Лечение гипохромной сидероахристической анемии. При этой форме анемии имеется дефицит синтазы -аминолевулиновой кислоты и нарушается синтез протопорфиринового кольца гема. В результате, несмотря на высокий уровень железа в организме, оно не может включиться в гем и количество гемоглобина в эритроцитах падает (цветовой показатель крови снижается менее 0,8). Пиридоксин назначают по 50-200 мг/сут.
Лечение пиридоксин-зависимого судорожного синдрома у детей. Это наследственная патология, при которой нарушено декарбоксилирование глютаминовой кислоты в ГАМК (дефект декарбоксилазы глютаминовой кислоты). У таких детей через 2-4 часа после родов возникают тонико-клонические судороги, которые практически не устраняются обычными противосудорожными средствами. Пиридоксин назначают по 5-10 мг/сут длительно (до 3-5 лет).
При лечении изониазидом, гидралазином, циклосерином и D-пеницилламином часто возникают нейротоксические реакции, которые связывают со способностью этих лекарственных средств нейтрализовать витамин В6в нейронах ЦНС, образуя с ним неактивные комплексы. Для предупреждения нейротоксического эффекта этих лекарств пиридоксин назначают из расчета 10:1 (т.е. на каждые 100 мг этих лекарств требуется 10 мг пиридоксина в сутки).
Эмпирически пиридоксин применяют у женщин, которые плохо переносят оральные контрацептивы. Использование пиридоксина в дозе 50 мг/сут позволяет устранить нейротоксические эффекты контрацептивов: повышенную возбыдимость, головные боли, нарушения сна.
НЭ: В обычных дозах пиридоксин практически не вызывает нежелательных эффектов. Однако, следует помнить, что он усиливает синтез дофамина в ЦНС (который выполняет роль пролактостатина) и, поэтому, он может остановить лактацию у кормящих матерей.
Пиридоксин несовместим с приемом леводопы у больных синдромом Паркинсона. За счет активации декарбоксилаз ЖКТ и печени пиридоксин будет вызывать практически полное разрушение леводопы еще до того, как она проникнет в ЦНС.
Длительный прием больших доз пиридоксина может быть причиной двух весьма редких осложнений:
Развития «пиридоксиновой зависимости» - генетически обусловленного состояния, которое возникает при длительном введении пиридоксина в дозе 100-200 мг/сут. При этом организм теряет чувствительность к физиологическим дозам витамина и попытка отменить пиридоксин вызывает картину тяжелого авитаминоза (себорея, глоссит, спутанность сознания, задержка роста и развития, анемия, судороги). Описанные в медицинской литературе 3 случая В6авитаминоза как раз и являются примерами такой «зависимости». Они возникли у детей, матери которых принимали в течение беременности высокие дозы пиридоксина.
Введение пиридоксина в мега-дозах (200-2000 мг/сут) может вызвать тяжелую сенсорную нейропатию – онемение кистей и стоп, появление в них чувства сдавления.
ФВ: таблетки по 2, 5 и 10 мг; раствор 1 и 5% в ампулах по 1 мл.
Аскорбиновая кислота (Ascorbinic acid, Vitamin C)Интересно отметить, что аскорбиновая кислота выполняет роль витамина только у приматов, морских свинок, летучих мышей-крыланов, воробьев и краснобрюхих дроздов. Все другие животные способны синтезировать эту кислоту из глюкозы.
Пищевая роль. Аскорбиновая кислота содержится как в продуктах растительного, так и животного происхождения. Основными источниками витамина С являются:
-
Источник
Содержание мг/100 г массы
Черная смородина
Капуста брокколи
Брюссельская капуста
Цветная капуста
Земляника
Лимоны
Грейпфруты
Ананасы
200
70-163
90-150
50-90
40-90
50-80
28-48
20-40
С уточная
потребность в витамине С составляет
30-60 мг. Общее количество витамина С в
организме составляет 1500 мг (но при
чрезмерном поступлении витамина в
организм его депо может увеличиваться
до 2500 мг). Запасов депо хватает на 30-45
дней.
уточная
потребность в витамине С составляет
30-60 мг. Общее количество витамина С в
организме составляет 1500 мг (но при
чрезмерном поступлении витамина в
организм его депо может увеличиваться
до 2500 мг). Запасов депо хватает на 30-45
дней.
МД: В организме аскорбиновая кислота превращается частично в дигидроаскорбиновую кислоту и при этом образуется окислительно-восстановительная система, которая способна переносить водород в различных биохимических реакциях.
ФК: Аскорбиновую кислоту вводят внутрь, внутримышечно (лучше совместно с новокаином или лидокаином) и внутривенно. Всасывание аскорбиновой кислоты в полости рта происходит пассивно, в кишечнике – при помощи активного транспорта, сопряженного с переносом глюкозы. Если аскорбиновую кислоту вводят в физиологических дозах (30-60 мг/сут) ее биодоступность близка к 100%. В фармакологических дозах (75-180 мг/сут) биодоступность падает до 70-90%, а при дальнейшем повышении дозы уменьшается до 50%.
В крови аскорбиновая кислота транспортируется в связанном с лейкоцитами и тромбоцитами состоянии. Наибольшие количества аскорбиновой кислоты накапливаются в гипофизе, надпочечниках, хрусталике глаза и печени. Выводится аскорбиновая кислота почками, после превращения внеактивную дикетогулоновую, а затем щавелевую кислоту. Период полуэлиминации ее составляет 12,8-29,5 сут.
ФЭ:
Аскорбиновая кислота поддерживает в восстановленном состоянии металллы простетических групп металлоферментов, которые принимают участие в следующих процессах:
Синтез коллагена. Аскорбиновая кислота восстанавливает железо в активном центре пролилгидроксилазы и медь в активном центре лизилгидроксилазы. Эти ферменты гидроксилируют остатки пролина и лизина в молекулах протоколлагена и это обеспечивает посттрансляционную стабилизацию третичной структуры коллагеновой цепи.
Синтез L-карнитина. Аскорбиновая кислота обеспечивает гидроксилирование триметил-лизина в процессе синтезаL-карнитина – основного переносчика жирных кислот через митохондриальную мембрану для последующего их-окисления.
Синтез нейромедиаторов. Аскорбиновая кислота обеспечивает работу гидроксилаз, которые синтезируют норадреналин из дофамина и серотонин из триптамина в ЦНС.
Синтез стероидных гормонов. Аскорбиновая кислота обеспечивает работу цитохромов Р450, участвующих в биосинтезе стероидов (окисление в 7-положении).
Аскорбиновая кислота обеспечивает протекание следующих восстановительных реакций:
Восстановление Fe3+вFe2+в процессе абсорбции.
Восстановление фолиевой кислоты до активной тетрагидрофолиевой кислоты.
Показано, что аскорбиновая кислота стимулирует образование циклических нуклеотидов (цАМФ и цГМФ), простагландинов.
Под влиянием аскорбиновой кислоты усиливается синтез иммуноглобулинов, лизоцима и интерферонов.
Применение и режимы дозирования. Пожалуй ни один из витаминов не имеет столь широких и столь же, зачастую, необоснованных показаний для применения, как аскорбиновая кислота.
В 1973 г. L.Paulingпредложил использовать мега-дозы витамина С (3-4 г/сут) для лечения простудных заболеваний, вирусных инфекций и повышения иммунитета. Однако, на протяжении более чем 10 лет исследователи получали весьма противоречивые результаты в отношении влияния витамина С на течение простудных заболеваний. В 1979 г.было проведено двойное слепое исследование14применения витамина С в дозе 1-4 г/сут для повышения иммунитета. Было убедительно доказано, что эффект аскорбиновой кислоты не отличается от эффекта плацебо.
В 1989 г. G.BlockиM.Menkesопубликовали обзор, в котором привели данные о возможной роли витамина С в профилактике онкологических заболеваний за счет его способности подавлять перекисное окисление и повышать иммунитет. Кроме того, аскорбиновая кислота позволяет предотвратить образование нитрозаминов (сильных канцерогенов) в ЖКТ, стимулирует работу микросомальных ферментов, разрушающих ксенобиотики. Современные исследования, однако, весьма скромно оценивают роль витамина С в онкологии. В большинстве проведенных к настоящему времени исследований введение витамина С лицам из групп онкологического риска осуществлялось в виде коррекции рациона питания, поэтому до сих пор неясно, что же оказывало протективный эффект – введение витамина С или же нормализация рациона питания.
В 1982-1987 гг. появилась серия публикаций, пропагандировавших применение витамина С для профилактики и лечения атеросклероза и других сердечно-сосудистых заболеваний. Считалось, что за счет улучшения работы микросомальных систем печени избыток холестерина может быть преобразован в желчные кислоты и удален из организма, а структура сосудистой стенки, под влиянием витамина С, восстановится. Однако, параллельно с этими исследованиями был опубликован ряд работ, в которых авторы не обнаружили никакой связи между приемом витамина С и снижением риска сердечно-сосудистой патологии. В связи с этим, в настоящее время влияние витамина С на кардиоваскулярную патологию считается недоказанным.
В настоящее время доказанными можно считать только следующие показания для применения витамина С:
Лечение авитаминоза (цинга, скорбýт). Клинические проявления цинги возникают если уровень аскорбиновой кислоты в организме падает менее 300 мг. Основные проявления цинги включают повышенную склонность к кровотечениям и кровоизлияниям, вследствие дефицита коллагена сосудистой стенки – возникают подкожные, перифолликулярные (вокруг волосяных мешочков), межмышечные, околосуставные и поднадкостничные кровоизляния, кровоточивость десен, выпадение волос и зубов. Кровоизлияния в суставы и под надкостницу резко ограничивают подвижность больного, вызывают мучительные боли. Заболевание сопровождается общей слабостью, усталостью, депрессией. Смерть наступает от кровоизлияния в мозг. Аскорбиновую кислоту назначают в дозе 500-1500 мг/сут.
В послеоперационном периоде и при общирных разможженных ранах применение аскорбиновой кислоты в дозе 500-1000 мг/сут позволяет ускорить формирование рубца.
Аскорбиновая кислота в дозах 1-2 г/сут применяется у пациентов с хронической надпочечниковой недостаточностью для стимуляции синтеза кортикостероидов.
Аскорбиновая кислота в дозе 1,0 г 3-4 раза в сутки применяется для закисления мочи у пациентов с инфекциями нижних отделов мочевыводящих путей (при этом устраняются дизурические явления и повышается чувствительность возбудителей к химиотерапии).
НЭ: Аскорбиновая кислота – малотоксичное соединение, как правило хорошо переносится. Нежелательные эффекты возникают при ее применении в дозе более 1,0 г/сут и включают:
Гипергликемию – связанную с конкуренцией витамина С и глюкозы за транспортные механизмы, а также с подавлением секреции инсулина под влиянием дигидроаскорбиновой кислоты.
Оксалурию с образованием оксалатных кальциевых камней в почках.
Использование больших доз аскорбиновой кислоты во время применения оральных контрацептивов может привести к неэффективной контрацепции, если по каким-либо причинам прием витамина С будет внезапно прекращен. Это связано с тем, что прекратится дополнительный синтез эстрогенов, который ситмулировала аскорбиновая кислота и их уровень в крови женщины резко уменьшится.
ФВ: таблетки по 50, 100, 500 и 1000 мг; растворы 5 и 10% в ампулах по 1 и 2 мл.
Р утин
(Rutin, Rutoside)Представляет собой группу флавоноидов.
Естественными флавоноидами являются
рутин и пентаоксифлавон – кверцетин,
который представляет собой лишенный
сахаристой части рутин. Некоторые из
авторов рассматривают пентаоксифлавон
как витамин С2. В настоящее время
получены полусинтетические витамеры
рутина – венорутон (троксевазин).
утин
(Rutin, Rutoside)Представляет собой группу флавоноидов.
Естественными флавоноидами являются
рутин и пентаоксифлавон – кверцетин,
который представляет собой лишенный
сахаристой части рутин. Некоторые из
авторов рассматривают пентаоксифлавон
как витамин С2. В настоящее время
получены полусинтетические витамеры
рутина – венорутон (троксевазин).
Витаминная роль флавоноидов до настоящего времени вызывает занчительные сомнения. В 1986 г. AmericanMedicalAssociationв руководстве «DrugEvaluations» указывало, что«В препаратах поливитаминов включение компонентов, ценность которых не доказана – холина, метионина, лецитина, биофлавоноидов, инозитола – безосновательно.»Поэтому в настоящее время за рубежом биофлавоноиды рассматривают не как лекарственное средство, а как биологически активную добавку к пище.
МД и ФД: Рутин способствует восстановлению дигидроаскорбиновой кислоты в аскорбиновую кислоту и защищает ее от инактивации в дикетогулоновую кислоту.
Под влиянием рутина несколько улучшается синтез коллагена и тонус венозной стенки.
Рутин способен инактивировать супероксидный и гидроксидный радикалы в водной фазе. Полагают, также, что рутин снижает активность липоксигеназы и тормозит синтез лейкотриена В4 (хемоаттрактанта). Это приводит к снижению миграции нейтрофилов в очаг воспаления.
Применение и режим дозирования. Авитаминоз Р в клинической практике не описан, воспроизвести его у лабораторных животных изолированно (без цинги) невозможно.
Единственным применением витамина Р в настоящее время остается симптоматическое лечение варикозной болезни вен нижних конечностей, геморроя и хронической венозной недостаточности. Рутин назначают внутрь по 30-60 мг 1-2 раза в день и местно, на область варикозных узлов в виде геля 2 раза в день.
НЭ: не описаны.
ФВ: таблетки по 20 и 50 мг; гель 2% в тубах по 40,0.
