
- •1 Влияние температуры 300, 350, 400 к при давлении 0,1 мПа
- •1.1 Расчет изменения энергии Гиббса
- •1.1.1 Расчёт энергий Гиббса процесса гидратации пентена-1 при температуре 300 к
- •1.1.2 Расчёт энергий Гиббса процесса гидратации пентена-1 при температуре 350 к
- •1.1.3 Расчёт энергий Гиббса процесса гидратации пентена-1 при температуре 400 к
- •1.2 Расчёт константы равновесия процесса гидратации пентена-1
- •1.4.1 Расчёт равновесной степени превращения и равновесной мольной доли компонентов в смеси при температуре 300 к
- •1.4.2 Расчёт равновесной степени превращения и равновесной мольной доли компонентов в смеси при температуре 350 к
- •1.4.3 Расчёт равновесной степени превращения и равновесной мольной доли компонентов в смеси при температуре 400 к
- •3 Расчет селективности по «в» и «с»
- •5 Материальный баланс процесса получения 5 т н-пентанола в лучших условиях
- •6 Расходный коэффициент «а» в т/1 т смеси изомеров
- •Заключение
- •Список использованных источников
1.2 Расчёт константы равновесия процесса гидратации пентена-1
Константа равновесия может быть найдена расчетным методом по уравнению (1.3) [1]:
 ,
(1.3)
,
(1.3)
где Кр – константа равновесия химической реакции, атм-4;
R – универсальная газовая постоянная, ккал/(К · моль).
1.2.1 Расчёт константы равновесия процесса гидратации пентена-1 при температуре 300 К
1) Расчёт константы равновесия процесса гидратации пентена-1 с получением пентанола-1 (1.3)
ln Кр1 = -(-0,052)/(1,987 · 10-3 · 300) = 0,0973;
Кр1 = 1,102 атм-4.
2) Расчёт константы равновесия процесса гидратации пентена-1 с получением пентанола-2 (1.3)
ln Кр2 = -1,06/(1,987 · 10-3 · 300) = -1,768;
Кр2 = 0,1707 атм-4.
1.2.2 Расчёт константы равновесия процесса гидратации пентена-1 при температуре 350 К
1) Расчёт константы равновесия процесса гидратации пентена-1 с получением пентанола-1 (1.3)
ln Кр1 = -1,554/(1,987 · 10-3 · 350) = -2,2345;
Кр1 = 0,10704 атм-4.
2) Расчёт константы равновесия процесса гидратации пентена-1 с получением пентанола-2 (1.3)
ln Кр2 = -3,258)/(1,987 · 10-3 · 350) = -4,685;
Кр2 = 9,233 атм-4.
1.2.3 Расчёт константы равновесия процесса гидратации пентена-1 при температуре 400 К
1) Расчёт константы равновесия процесса гидратации пентена-1 с получением пентанола-1 (1.3)
ln Кр1 = -3,22/(1,987 · 10-3 · 400) = -3,976;
Кр1 = 0,01876 атм-4.
2) Расчёт константы равновесия процесса гидратации пентена-1 с получением пентанола-2 (1.3)
ln Кр2 = -5,574/(1,987 · 10-3 · 400) = -6,937;
Кр2 = 0,0009712 атм-4.
1.3 Мольный баланс процесса гидратации пентена-1
Таблица 1.13 – Мольный баланс процесса гидратации пентена-1
|
|
1–С5Н10 |
Н2О |
1-С5Н11ОН |
2-С5Н11ОН |
|
nio |
1 |
1 |
– |
– |
|
ni |
(1 – x1 – x2) |
(1 – x1 – x2) |
x1 |
x2 |
∑ ni = 1–x1 – x2 + 1–x1 – x2 + x1 + x2 = 2 – x1 – x2 = 2 – xА,
где хA – равновесная степень превращения.
1.4 Расчёт равновесной степени превращения и состав равновесной мольной доли компонентов в смеси для реакции гидратации пентена-1
 ,
(1.4)
,
(1.4)
 ,
(1.5)
,
(1.5)
где Робщ – общее давление системы, атм;
nB, nA, nY, nC – число молей соответствующего компонента.
 ,
(1.6)
,
(1.6)
 ,
(1.7)
,
(1.7)
Состав мольной доли компонентов в смеси рассчитывается по уравнению (1.8) [1]:
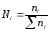 ,
(1.8)
,
(1.8)
где Ni – мольная доля i-го компонента.
1.4.1 Расчёт равновесной степени превращения и равновесной мольной доли компонентов в смеси при температуре 300 к


Далее средствами MS Excel с помощью надстройки “Поиск решения” нужно подобрать x2 при условии, что
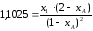
Получилось, что
x1 = 0,02916, x2 = 0,04517, xA = 0,02916 + 0,04517 = 0,3368
nA = 1 – хA = 1 – 0,3367 = 0,6632 моль;
nB = x1 = 0,2916 моль;
nС = x2 = 0,04517 моль;
nY = 1 – хA = 0,6632 моль;
∑ ni = 2 – хA = 1,6632 моль.
NA = 0,6632 / 1,6632 = 0,3988;
NB = 0,2916 / 1,6632 = 0,1753;
NC = 0,04517 / 1,6632 = 0,02716;
NУ = 0,6632 / 1,6632 = 0,3988.
