
- •Руды и минералы Au, Ag. Формы нахождения Au, Ag в рудах
- •Iтонкое измель флотация, обжиг
- •II. Плавка золотой головки
- •III. Гидрометаллургичесие методы
- •III. Влияние температуры
- •IV. Вязкость пульп
- •I. Метод перколяции
- •II. Метод кучного выщелачивания
- •III. Цианирование перемешиван
- •Au содовый раствор
- •Сжатый |оздах
- •1 Раствор
- •Сдира,н
- •Цианирование
- •Поведение примесей Au
- •III. Цианирование перемешиван
Поведение примесей Au
Содержание в анодном сплаве до 20% Au не нарушает процесса (ф 0 au/au3+ = +1,58 В).
При содержании > 20%, образует на аноде плотную корку, пассивирует его и вызывает побочные реакции на электродах.
Pd
ф °pt/Pd2+ = + 0,987 В. Близок к Ag. Возможно частичное растворение Pt и при накоплении в электролите частичное осаждение на К. При повышенном содержании Pt электролиз ведут при пониженной кислотности и плотности тока( i =300-400 А/м2).
Содержание Pt в растворе не должно превышать 0,1 - 0,2 г/л.
Pt
ф °Pt/Pd2+ = +1,2 В.
Возможен частичный переход в раствор и соосаждение на К. Максимальное содержание в электролите 0,025 г/л.
Си.
ф °pt/Pd2+ = +0,337 В.
Легко растворяется на аноде и не осаждается на К. При высоких содержаниях приводит к нежелательным явлениям. В прикатодном пространстве возможно накопление Си , что приводит к выделению ее на катоде вместе с Ag. Поэтому необходимо интенсивное перемешивание электролита и невысокая плотность тока.
Предельное содержание Си- 100 г/л (обычно 30- 60 г/л), при этом Ag должно быть более 110- 120 г/л. При содержании Си в аноде >7,5%, электролитическое рафинирование экономически не выгодно(необходимо часто менять электролит).
Bi, Pt
Переходят в электролит, но могут частично гидролизоваться и уходить в шлам. При попадании на катод, Bi и Pt легко удаляются при промывке катодов слабой HN03.
Fe,Zn
Переходят в электролит и выводятся из него при регенерации.
Se
Растворяется на аноде и переходит в шлам в виде Ag2SeC>4.
Те
Очень вредная примесь! При содержании > 0,2% электролиз нарушается.
Ag2Te - 2е —Те + 2Ag+;
Ag2Te + ЗН20 - бе —► Те03 2" + 2Ag+ + 8Н+;
Ag2Te + 4Н20 - 8е * ТеО/~ + 2Ag' + 8Н+.
Концентрация Те в растворе не велика, так как он образует с Ag труднорастворимые соединения и переходит в шлам. В катодный металл Те может попасть при восстановлении, либо механически. При содержании Те в анодном металле >0,2% начинают выделяться оксиды озота и образуются серые губчатые осадки (при содержании 16- 30 мг/л Те). Поэтому Те необходимо удалять на предыдующих стадиях.
На практике установлено, что анодный сплав должен содержать более 750 проб Ag,
200- Au, 75 проб лигатуры, менее 2 проб Те.
Аппаратурное оформление
Ванны изготовлены из винипласта, заключенного в деревянный каркас V=300- 600л. Рисунок 63.
Катод - на всю ширину ванны из Al, Ti, стали или Ag.
■* ►
1225
Катод
Катодная
штанга Анод
Рис. 63
Аноды растворяются двое- трое суток. Они обычно книзу утолщены, так как нижняя часть растворяется быстрее.
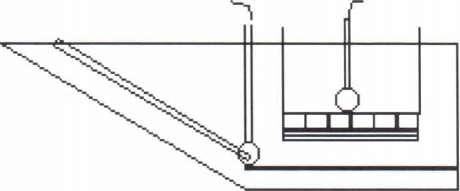
Ag осаждается на катоде в виде крупнокристаллического осадка. Кристаллы Ag растут от К к А, что может привести к замыканию. Поэтому их периодически счищают. Электролит перемешивают с помощью сжатого воздуха. Кристаллы серебра, упавшие на дно периодически извлекают дырчатым совком из алюминия. Иногда одну из боковых стен делают наклонной и по ней выгребают катодное Ag. Рисунок. 64.
|
|
|
|
|
|
|
|
|
|
С |
3 |
| |||
|
|
|
|
| |||
|
|
|
| ||||
Рис.
64.
Аноды помещают в чехлы из хлорвиниловой ткани. Шлам периодически извлекают из чехлов. Электролит обедняется по Ag, его выводят из ванны и заменяя новым.
I = 200- 600 А/м2, чем грязнее аноды, тем i меньше; t = 30- 50°С.
Выход по току - 94- 96%; U = 1,0 - 2,5 В;
Расход эл.энергии - 0,3 - 0,6 кВт*ч/1кг Ag. Ag выгружают из ванны, промывают раствором HNO3, затем горячей водой, прессуют, для удаления влаги и плавят.
Чистота Ag 999,7 - 999,9 проб.
Ванны с горизонтальным расположением электродов
Ванны прямоугольной формы, одна из боковых стенок наклонная. Катод выполнен из стали или графита и расположен на дне ванны.
VBaHHbi= 150 л;
Я!анодов- 50 кг,
h= 100- 120 мм (между К и А);
i = 400- 500 А/м2;
U= 3,5-5,0 В;
i
О
Рис.
65.
Фильтровальная
ткань(капрон)
Токоподвод
к
^Токоподвод
к аноду
Аноды
Ложное
днище
Преимущества:
Полное срабатывание анодов,
Простота устройства,
Удобство обслуживания. Недостатки:
высокий расход эл.энергии,
громозкость.
Эти
ванны часто применяют для перерабатывания
анодного скрапа
( « 15% ванн).
Отработанный электролит направляют :
1. В ванны предварительного электролиза для понижени
я
содержания
(CAg понижают до 10 г/л).
серебра
Аи
(катод)
Электролитическое рафинирование Аи
Анод отливают из рафинируемого сплава, содержащего Ag, платиновые металлы и некоторые цветные металлы.
НАиСЦ, НС1, Аи
Н20, примеси, с примесями электролит (анод)
Золотохлористоводородная кислота (НАиС14).
HAuCU —► Ащ + 4Н+ +АиС14 (полностью диссоциирует). АиСЦ Аи3+ + 4СГ , но
![]()
то есть равновесие смещено влево. Возможен гидролиз АиСЦ" в водном растворе
:
[AuCh(OH)]- + Н+ + СГ.
Но!! в кислом растворе гидролиз практически невозможен. То есть Аи в электролите находится в форме АиСЦ". Основной катодный процесс:
АиСЦ" + Зе < Аи + 4С1".
ф° = + 0,99 В.
Восстановление Н2 невозможно, так как ф°н+/н2 = 0. На аноде:
Аи + 4СГ - Зе—*• А1СЦ",
так как стандартный ф() хлора и кислорода более электроположителен,
о
чем ф au3+/au •
2СГ - 2е " С12(газ), q>° = + 1,36 В.
2НгО -4е —*4¥t + 02(газ), (р° = 1,23 В.
То есть их выделение в данном случае невозможно.
!!!Однако, Аи склонно к пассивированию, что приводит к
прекращению растворения золота,
о
ф смещается в положительную сторону и становится возможным выделение С1.
Это явление весьма нежелательно и далее опасно для работающих
(С12).
Во избежание этого явления необходимо поддерживать повышенную кислотность, высокую температуру.
Повышение кислотности (свободной НС1) приводит к увеличению электропроводности электролита и, как следствие, к уменьшению расхода электроэнергии.
!! Другой особенностью электролиза Аи является то, что на аноде кроме АиСЦ" образуется АиСЦ:
Аи + СГ-е > АиСЦ"; ф°=+1,11В.
Так как электрохимический эквивалент Аи' > электрохимического эквивалента Аи3' , то г|А в расчете на AuJ оказывается > 100°С. За счет реакции диспропорционирования:
А
и CI4
+ И20
.
Часть Au выпадает в шлам. Извлечение Аи из шлама требует затрат, поэтому стремятся предотвратить образование порошкового Аи. Это возможно с увеличением i.
!!! Третья особенность электрохимического рафинирования Аи- это проведение электорлиза при переменном ассиметричном токе (процесс Вольвиля). Для этого последовательно с постоянным током включают генератор переменного тока с ЭДС, превышающей ЭДС постоянного тока. Рисунок 65.

Необходимость применения ассиметричного тока вызвана специфическим поведением Ag при растворении анодного сплава.
Так как (p°Ag (+ 0,799) < электроотрицателен, чем ф°Аи(+0,99) , Ag легко окисляется на аноде, образуя AgCl :
Ag + СГ-е > AgCL ф° = +0,22В.
Если процесс ведут при постоянном токе, AgCl покроет анод толстой коркой, что приведет к прекращению растворения Аи и выделению СЬ. При использовании ассиметричного тока на аноде чередуются полупериоды (+) знака (ti) с более короткими (-)(ti).
При анодной поляризации происходит растворение сплава и пленки AgCl. Во время катодной поляризации AgCl теряет сцепление с анодом и опадает на дно ванны (анодный шлам). Использование ассиметричного тока позволяет вести электролитное рафинирование Аи с 20% Ag.
При этом Uпер: ип0ст должно быть тем >, чем >Ag в сплаве.
Если содержание Ag менее 5 -е- 6 %, электролиз можно вести при постоянном токе. AgCl не образует плотной пленки и опадает в шлам.
В анодном сплаве содержатся примеси: Си, Pb, Bi, Те, Fe, Sn, As, Sb,
Pt, Pd.
Поведение примесей
Си
Более электроотрицателен чем Au. Переходит в раствор. При содержании Си в аноде >2% необходимо часто менять электролит. ССи=90г/л.
РЬ
Еще более электроотрицателен. Растворяется на аноде в первую очередь, его концентрация в растворе(РЬСЬ) определяется растворимостью РЬСЬ. При насыщении раствора РЬСЬ, на аноде может образоваться нерастворимая пленка, которая вместе с AgCl может вызвать пассивицию анода. Если содержание РЬ и Ag менее 13%, пассивации не происходит.
Bi
Легко растворяется. При содержании в сплаве до 0,3% затруднений не вызывает.
При совместном присутствии: 0,6%Bi; 0,9%Pb; 12%Ag - анод пассивируется.
В присутствии S даже небольшое количество Bi и РЬ вызвают пассивацию. При содержании в сплаве BiS и PbS необходимо предварительно окислить сплав в присутствии Мп02(300- 500% от теоретически необходимого для окисления S).
Те
Растворяется на аноде и накапливается в электролите. При высоком содержании в электролите ухудшает качество катодного Au.
Fe
Вредная примесь. Переходя в раствор в виде Fe~ восстанавливает Au из электролита (в шлам).
Sn, Sb, As
До 0,05% легко растворяются и трудностей не вызывают.
Pt, Pd
Растворяются на аноде и могут при повышенном содер- жании в растворе (Cpt=50rAi, Ср<]=15г/л) соосаждаться на катоде совместно с золотом.
Ru, Os, Ir, Rh
Переходят в шлам.
Аппаратура
Электролизные ванны из фарфора или винипласта V=20 + 65 л. Катоды из Аи жести толщиной 0,1 4- 0,25мм.(из электролитного Аи).
Для придания жесткости катоды рифленые (на прессе жести придают рифление).
В ванны подвешивают 18 катодов(по 3 в ряд)и 15 анодов (по 3 в ряд ).
Масса 1 анода- 2 кг.
Для поддержания t°, ванны устанавливают в водяных банях. Электролит перемешивают сжатым воздухом, подаваемым через стеклянные трубки. Так как выделяется С12, ванны устанавливают в вытяжном шкафу.
Электролит содержит: 70 + 200 г/л Аи; 40 + 100 г/л НС1.
t°= 50 -г- 60°С. Электролиз ведут ассиметричным током i=600 + 1500
А/м2.
Сила переменного тока на 10% больше силы постоянного тока. Una ванне 0,5 — 1,0В.
Катод выгружают 3-4 раза в сутки. Катодное Аи промывают горячей водой, очищают щетками, обрабатывают НС1 или NH4OH (для растворения AgCI), снова- водой, сушат, прокаливают и плавят в индукционных печах.
Проба Аи- 999,8- 999,9. Основные примеси : Ag, Fe, Си.
Анодный шлам промывают водой. Шлам загружают в барабан, помещенный в наполненную водой ванну. При вращении барабана AgCI через отверстия в барабане смывается водой в ванну, а более крупные частицы Аи остаются в барабане. Остаток сушат и направляют на плавку на аноды.
Выход скрапа =10 + 20% от массы анодов.
Его тоже промывают в барабане и отправляют на плавку анодов.
Электролит в процессе электролиза обедняется по Аи и обогащается примесями. При работе на грязном электролите Его тоже промывают в барабане и отправляют на плавку анодов.
Электролит в процессе электролиза обедняется по Аи и обогащается примесями.
При работе на грязном электролите возможно:
Загрязнение катодного Аи;
Рост дендритов на катоде, что приводит к катодным замыканиям;
Пассивация анодов за счет кристаллизации солей.
Электролит не пригоден для электролиза, если: Аи<100 г/л; Си>90 г/л; Pd>50 г/л; Pt>15 г/л; РЬ>1.5 г/л; Те>4 г/л; Fe>2 г/л.
Отработанный электролит перерабатывают различными методами:
Электролизом с нерастворимыми анодами;
Ионообменными смолами.
Свежий электролит готовят электрохимическим растворением относительно чистых сплавов Аи (например, полученных при обработке анодных шламов Ag электролиза).
Растворение ведут в ваннах круглой формы, снабженных диафрагмой из пористых материалов (пористый фарфор, глина, ионообменные материалы).
В диафрагму завешивают 6 + 8 анодов и заливают раствор НС1 (разбавленный 3:1). По обе стороны диафрагмы подвешивают катоды из тонких пластин Аи или графита.
В катодное пространство заливают расствор 1:3. На аноде растворяется Аи, на катоде |Н2.
2Ли + 6Н + 8СГ = 2АиС14 + ЗН2.
Раствор содержит 200 -е- ЗООг/л Аи и 45 -н 80 г/л НС1. Его разбавляют водой и заливают в ванны для основного электролиза.
Достоинство метода электролитического рафинирования
получают высокочистый Me;
возможно выделение Pt.
Производство вторичных Аи и Ag
Особенность вторичной металлургии благородных металлов(БМ) - многообразие физических форм и химических составов отходов, содержащих БМ. Обычно это отходы изделий из БМ с более высоким содержанием металлов, чем руды. Характеристика вторичного Аи- содержащего сырья
Основные поставщики сырья БМ:
металлургия,
приборостроение,
электронная промышленность.
Сырье делят на несколько видов:
Аи- содержащие сплавы (50 -т- 60%Аи);
Детали электронной и электротехнической промышленности
(0,3 до 20%Au).Au в них в виде тонкого поверхностного слоя на металлической, керамической, пластмассовой или смешанной (металло- керамической) основе;
-Порошкообразные (сыпучие) отходы: зола фарфорового производства (25 -т- 35% Au); шламы электролиза Си (15 4- 25%Аи); отходы шлифовально- полировальных отделений ювелирных производств (5 н- 10% Au).
Характеристика вторичного Ag- содержащего сырья
Основные поставщики:
Фото- и кинопромышленность;
Химическая;
Электротехническая,
Радиопромышленность;
Зеркальное;
Ювелирное;
Часовое производство;
Лечебные учреждения.
Состав поступающего на переработку сырья
Ag бромистое (35-66%), Ag сернистое (45-65%);
Зола кинопромышленности (45 -ь 52%);
Зола фотобумаги (1,2 н- 7%);
- Зола фотоотпечатков(до 0,5%);
-Отходы химической промышленности в виде: отработанных контактов (20 -ь 80%Ag), катализаторов (>80%),шламов (60 4- 80%), лома аппаратуры (20 + 25 %Ag);
Отходы зеркальной промышленности в виде зеркального боя (0,05 0,2%Ag);6ofi елочных украшений ( до 0,5%); лом серебрильных кувшинов (10 -ь 25%); сукно серебрильных столов (в золе 40 ч- 50%); и другие отходы серебрильных установок (до 60% Ag).
Отходы полиграфической промышленности;
Отходы ювелирных заводов и мастерских в виде сора (0,05-10%);
часовое np0H3B0flCTB0(Ag контакты, припои, опилки, стружка) - до70% Ag и ...
Все отходы делят на 2 вида сырья:Переработка сплавов
Сплав подвергают плавке в тигельных индукционных печах. Содержание Аи обычно >50%, поэтому количество флюсов составляет 20- 30% от массы шихты.
Флюсы: Na2C03 и Si02.
Материал плавят при t° = 1200 + 1250°С, т = 0,57час.
Расплавленный металл гранулируют, вливая медленно в воду.
Гранулы промывают и растворяют царской водкой в фарфоровой емкости при t° =80 + 90°С, при периодическом перемешивании до полного прекращения реакции:
Au+4HCl+HN03 = HAuC14+N0+2H20.
Раствор декантируют и отстаивают (х 4 т 6 часов) для коагуляции AgCI. Осадок отделяют от раствора фильтрацией и направляют на плавку. Из осветленного раствора Аи выделяют солянокислым гидразином или сернокислым закисным железом:
4НАыС14 + 3N2H2(HCl)2 = 4Аи + 3N2 + 22НС1.
П отмыв олученный шлам промывают водой, затем 10% раствором NH4OH для ки AgCI:
AgCl+2NH40H=Ag(NH3)2Cl+H20.
Осадок промывают 5 -г 10% раствором H2S04 для отмывки от Fe и Си. Отмывку от Ag, Си и Fe проводят дважды. Шлам сушат при t ' =150 -н 200 С, плавят с селитрой (NaN03) при 1250°С и разливают в слитки. Слитки поступают на аффинаж электролизом.
Переработка шлифовальных Аи- содержащих порошков
Шлифопорошки после опробования загружают в реакторы для растворения Аи. Сырье смачивают водой (чтобы не было разбрызгивания), добавляют раствор HNO3 и НС1 в соотношении 1:5.
Траст =3 + 4 ч., t° = 80 + 100°С.
По окончании растворения пульпу фильтруют на нутч- фильтрах. Раствор после фильтрации поступает на осаждение Au [ N2H2(HC1)2 ] с добавкой медного порошка (для уменьшения кислотности, удаления HN03 и предотвращения обратного растворения Аи).
Си + 4HN03 = Cu(N03)2 + 2N02 + 2Н20.
ТосаждИ т отстаивания составляет 5 часов. Далее пульпу фильтруют.
Осадок 3 + 4 раза промывают водой, сушат в электрических печах при t° =100 -г- 200°С и плавят в индукционных печах. Слитки отправляют на аффинаж, шлам - на медный завод.
Переработка изделий, покрытых золотом
Отходы радиотехнической промышленности представлены деталями из вольфрама или молибдена, покрытыми Аи.
Толщина золотой пленки 0,1-24 мкм, с содержанием в ней Аи ^20%.
Для растворения Аи могут быть использованы растворители, инертные к материалу основы, то есть растворы тиомочевины, йода, роданистого аммония.
При использовании иодистых растворов применяют раствор йода в водном растворе KI. При этом образуется комплекс KfAuU] или К[АиЬ].
Обычно раствор для снятия Аи- покрытия содержит 180 + 250 г/л KI и 200 г/л 12. Процесс ведут при воздействии электрического тока. Анодное и катодное пространство разделяют диафрагмой из пористого материала (например, керамики с порами величиной 0,0001 -=- 0,001мм при толщине стенок 8 мм).
На катоде выделяется Аи:
Аи + е > Аи.
Диафрагма разделяет продукты электродных реакций и предотвращает растворение губчатого Аи, выделившегося на катоде в травильном растворе.
Процесс электролитического выделения Аи ведут при U= 4 -н 5 В;
г = 20 -н 30 А/дм2; т=2 +3ч.
Расход электроэнергии составляет 0,2 0,4 кВт*ч/1г Аи. ЕАи= 99 + 99,8%.
Обеззолоченные отходы идут на выделение ЦМ. Аи- на плавку и аффинаж, осветленный раствор католита- в процесс электролиза.
Переработка отходов осуществляется по схемам. Рисунок 66,67.
Технологическая схема переработки вторичного Ag- содержащего сырья
Металлические отходы Неметаллические отходы
Приемная^плавка Флюсы Опробование
Плавка в электродуговых печах
Черновые слитки Шлак, пыль
4 Флюсы |
| На^медеплавильный завод
Плавка в индукционных печах
I I
Медный
порошок
I
Цементация
Ад (2 стадия)
Отработанный электролит Ад НЫОз О2
РастворениеИсходный порошкообразный материал
Опробование и анализ
I
Царсководочное растворение ФильтрацияОсадок Промывка
JC
Осадок
I
Сушка
I
Опробование и анализ
4
Осадок
Сушка
Черновое
30JJ0T0
Анализ
I
На
аффинажный завод
Ш|1ак
Раствор
Осаждение
Аи Фильтрация
Промывная
вода
Осадок
I
Промывка
'аствор
Осадок
Сушка
Плавка
Промывная
вода i
Нейтрализация
и коагуляция
Раствор
Отстаивание
В
канализацию
з
Технологическая схема переработки вторичного Аи- содержащего сырья
При плавке сырья на Ag (металл) добавляют флюсы: NaCC>3, Fe, буру (Н3ВО3), NaN03, СаСОз, Si02. Состав шихты для плавки зависит от состава сырья.
Ag- содержащее сырье в основном представлено AgBr, Ag2S, AgCl. При плавке бромистого и хлористого Ag в качестве флюса добавляют Na2C03:
2AgBr + Na2C03 > Ag2C03 + 2NaBr;
2AgCl + Na2C03 > AgC03 + 2NaCl;
Далее происходит термическая диссоциация AgCC>3
:
При плавке Ag2S:
2Ag2S + 4Na2C03 > 8Ag + 3[Na2S*Ag2S] + Na2S04 + 4C02.
Для восстановления Ag из Na2S*Ag2S вводят Fe:
Na2S*Ag2S+Fe > FeS*Na2S+2Ag.
Для связывания избытка Fe добавляют S (порошок). В AgCl, AgBr, Ag2S обычно не содержится неблагородных металлов. В отходах таких как зола, сплавы и другие неблагородные металлы содержатся в различных количествах. Для окисления этих металлов добавляют Na2NC>3, а для ошлакования Н3ВЮ3 (буру), Si02, стекло.
Вначале окисляется Ag:
2Ag + I/2O2 > Ag20;
Ag:0 + Me ^ Ag + MeO.
Примеси не благородных металлов переходят в шлак и накапливаются
AgC03
2Ag:0
Ag20
+
C02;
—►
4Ag
+ 021.
Аи Чернов.
(75-95% Аи)
I
Сорбент Десорбция Аи
Раствop N aO Н
awn
ДсЪербиия Zri. CN~. SO/'. SiO
Сорбент р-Р щелочи на
| нейтрал изайцию
Промывка Н 2° в отвал
1
Регенерированный
сорбент
У 2 1 где
d2 7,-Г
d-диаметр частиц, у - плотность, г см3.
1 г Au - 0,49г NaCN
Для снижения протекания данной реакции в раствор вводят защитную щелочь(СаО, Са(ОН)2) или NaOH - сдвиг равновесия реакции влево). Без защитной щелочи стадия гидролиза 3-16%. Использование защитной щелочи снижает до 0.1-0.3%.
Концентрация защитной щелочи: Ссао = 0.001 0.02%. Чаще применяют СаО как более дешевую, кроме того СаО выполняет роль коагумента.
4. Потери цианида за счет химического взаимодействия с минералами Руда содержит инертную породу: Si02, А1203, MgO, оксиды Fe(IH, II), и содержит оксиды, сульфиды, арсениды ЦМ и Fe, которые активно взаимодействуют с цианидом.
Соединения Fe :
Присутствуют в виде : Fe203, Fe304, FeOOH, FeC03, FeS2, FeS и другие. Окисленные соединения Fe203, Fe304, FeOOH, FeC03 не взаимодейст-вуют с NaCN. Поведение сульфидов зависит от их структуры и типа. Их различают: плотные и рыхлые, пористые.
Рис. 13.
Метод считается перспективным для переработки старых отвалов, бедных по Аи руд. Число установок кучного выщелачивания возрастает.
