
- •Розрахунки в середовищі excel Розділ 1. Розрахунок кінетичних параметрів топохімічних реакцій
- •Індивідуальна самостійна робота
- •Розділ 2. Статистична обробка результатів експерименту
- •2.1. Кореляційний аналіз
- •2.2. Довірчий інтервал
- •Контрольні питання
- •Література
- •Розділ 3. Розрахунок кінетичних параметрів хімічних реакцій
- •Література
- •Розділ 4. Оптимізація об'єктів досліджень за моделями другого порядку
- •Література
- •Розділ 5. Розрахунки математичних моделей "склад - властивість"
- •Література
- •Розділ 6. Розрахунок кінетичних параметрів за дериватографічними даними
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 7. Розрахунок очищення коксового газу від сірководню
- •Алгоритм розрахунку
- •Розділ 8. Розрахунок виробництва водню мембранним методом
- •Алгоритм розрахунку [1]
- •Контрольні питання
- •Розділ 9. Розрахунок паро – повітряної конверсії метану
- •Вихідні дані (додаткові)
- •Контрольні питання
- •Розділ 10. Розрахунок двоступеневої
- •Розділ 11. Розрахунок матеріального балансу синтезу метанолу
- •Розділ 12. Розрахунок матеріального балансу синтезу аміаку
- •Алгоритм розрахунку
- •Контрольні питання
- •Розділ 13. Розрахунок очищення газу від co2 розчином моноетаноламіну
- •Алгоритм розрахунку Розрахунок матеріального балансу виробництва
- •Стадія «тонкого» очищення
- •Стадія «тонкого» очищення
- •Концентрації компонентів суміші с(і)2відповідають даним таблиці 3.
- •2 Розрахунок теплового балансу виробництва
- •Де ∑m(mea)р-ну - сума витрат розчину меа на «грубе» та «тонке» очищення, кг меа/год.
- •3 Розрахунок насадкового абсорбера верхня частина абсорбера («тонке» очищення)
- •Алгоритм розрахунку
- •Швидкість захлинання абсорбера у верхній частині [3]:
- •Робоча швидкість газу у верхній частині абсорбера:
- •Нижня частина абсорбера («грубе» очищення)
- •Алгоритм розрахунку
- •Швидкість захлинання абсорбера у нижній частині [3]:
- •Робоча швидкість газу у нижній частині абсорбера:
- •4 Розрахунок тарілчастого абсорбера
- •Верхня частина абсорбера
- •Алгоритм розрахунку
- •Нижня частина абсорбера
- •Алгоритм розрахунку
- •Промисловий абсорбер має 15 тарілок: 9 в нижній частині і 6 у верхній.
- •Розділ 14. Аналіз статики іонного обміну однозарядних (рівнозарядних) іонів
- •Рівновага іонного обміну рівновалентних іонів
- •Алгоритм розрахунку
- •Контрольні питання
- •Література
- •Розділ 15. Аналіз статики іонного обміну різнозарядних іонів
- •Алгоритм розрахунку
- •Контрольні питання
- •Література
- •Розділ 16. Розрахунок очищення газу від оксиду карбону (IV) гарячим розчином поташу
- •1 Матеріальний розрахунок
- •Алгоритм розрахунку
- •1.1 Розрахунок грубого очищення
- •1.2 Розрахунок тонкого очищення
- •2 Тепловий баланс поташного очищення конвертованого газу
- •Алгоритм розрахунку
- •3 Конструктивні розрахунки насадкового абсорберу
- •3.1 Розрахунок діаметру абсорберу Нижня зона
- •Алгоритм розрахунку
- •Верхня зона
- •Алгоритм розрахунку
- •3.2 Розрахунок висоти насадки
- •Верхня зона
- •Алгоритм розрахунку
- •Нижня зона
- •Алгоритм розрахунку
- •1. Розрахувати реальний вміст компонентів k2co3,kнco3і н2о в розчинах згідно даних таблиці 10. Врахувати стехіометрію реакції
- •Розрахунок матеріального балансу
- •Розрахунок теплового балансу
- •Алгоритм розрахунку
- •Конструктивний розрахунок
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розрахунки в середовищіmathcad розділ 18. Розрахунок рівноваги оборотних реакцій
- •Розділ 19. Розрахунок трубчатого реактора конверсії природного газу
- •Алгоритм розрахунку
- •Розділ 20. Розрахунок рівноваги пароповітряної конверсії метану
- •Розділ 21. Розрахунок окиснення оксиду сульфуру (IV)
- •Контрольні питання
- •Література
- •Розділ 22. Альтернативний розрахунок матеріального балансу синтезу аміаку
- •Контрольні питання
- •Розділ 23. Альтернативний розрахунок матеріального балансу синтезу метанолу
- •Розділ 24. Розрахунок паро-вуглекислотної конверсії природного газу
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 25. Розрахунок вуглекислотної рівноваги у водних розчинах
- •Алгоритм розрахунку
- •Значення рН буде приймати значення 4, 5, 6, 7, ..... До значення –log(Kw). Важливо! Отримані числові значення параметра не утворюють матрицю, тому з ними не можливі дії, що застосовуються до матриці.
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Розділ 26. Аналіз динаміки іонного обміну однозарядних іонів
- •2 Хвильове рівняння для концентрації
- •3 Рівняння збереження в безрозмірній формі [1]
- •4 Рівняння ізотерми іонного обміну
- •5 Рішення хвильового рівняння методом характеристик [1]
- •6 Розрахунок обміну однозарядних іонів[1]
- •Алгоритм розрахунку
- •Вихідні дані для 1-ої ступені водопідготовки
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Література
- •Розділ 27. Термодинамічний та матеріальний розрахунки газифікації вугілля
- •Розділ 28. Термодинамічний розрахунок газифікації (конверсії) вуглеводнів
- •Алгоритм розрахунку
- •.Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розділ 29. Розрахунок концентрацiй iонiв у вапнованiй та коагульованiй воді
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Розділ 30. Аналіз динаміки іонного обміну різнозарядних іонів
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Література
- •Розділ 31. Термодинамічний розрахунок газифікації рідких палив невідомої формули
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Розділ 32.Розрахунок поличних колон синтезу аміаку
- •Алгоритм розрахунку
- •Індивідуальна самостійна робота
- •Контрольні питання
- •Література
- •Методичні рекомендації до виконання розрахункової роботи
- •Розрахунок матеріального балансу виробництва
- •Розрахунок енергетичного (теплового) балансу виробництва
- •Розрахунок основних реакторів
- •Захист розрахункової роботи
- •Завдання на розрахункову роботу з дисципліни
Контрольні питання
Коефіцієнт кореляції (ryx). Математичне очікування випадкової величини. Дисперсія випадкової величини (2). Стандартне відхилення. Паралельні (дубльовані) виміри. Рівень значимості q. Довірчий інтервал випадкової величини. Відсів грубих вимірювань.
Література
1. Методичні вказівки до комп‘ютерних та практичних занять з дисципліни “Методологія наукових досліджень” для студентів спеціальності 7.091602 “Хімічна технологія неорганічних речовин”. Укладачі : А.Л. Концевой, І.М. Астрелін, С.А. Концевой - НТУУ “КПІ”, 2006. – 80 с.
Розділ 3. Розрахунок кінетичних параметрів хімічних реакцій
Для необоротної реакції А + В продукти
кінетичне рівняння згідно з законом діючих мас матиме вид :
![]() (1)
(1)
де V -
швидкість реакції;
![]() -
час перебування в зоні реакції; k -
константа швидкості; СA
та
СB
– концентрації речовин А і В, відповідно,
мол частки; nA,
nB
– порядки реакції за компонентами А і
В. Сумарний порядок кінетичного рівняння
-
час перебування в зоні реакції; k -
константа швидкості; СA
та
СB
– концентрації речовин А і В, відповідно,
мол частки; nA,
nB
– порядки реакції за компонентами А і
В. Сумарний порядок кінетичного рівняння
![]() .
.
Якщо знехтувати зміною об’єму в процесі реакції, концентрація речовини А в рівнянні (1) може бути виражена у вигляді:
![]() ;
;
![]() ,
тому що
,
тому що![]() ,
,
де
![]() іx
– початкова концентрація і ступінь
перетворення речовини А. Концентрація
речовини В дорівнює:
іx
– початкова концентрація і ступінь
перетворення речовини А. Концентрація
речовини В дорівнює:

де b=
 - концентраційний параметр. Тоді
швидкість реакції:
- концентраційний параметр. Тоді
швидкість реакції:
![]() ,
де
,
де
![]() .
.
Для подальших розрахунків застосовуємо рівняння:
![]() .
(2)
.
(2)
.Значення порядків реакції nА, nВ і константи швидкості k* знаходять після логарифмування з метою лінеаризації рівняння (2):
ln(Vx
![]()
![]() )
= nB
)
= nB
![]() ln(
ln(![]()
![]() (b-x))+nA
(b-x))+nA
![]() ln(
ln(![]()
![]() (1-x))+lnk,
(3)
(1-x))+lnk,
(3)
де
Vx
=
![]() /
/![]() -
ще один вираз для швидкості реакції.
-
ще один вираз для швидкості реакції.
З врахуванням впливу температури за законом Ареніуса на швидкість реакції рівняння (2) змінюється на наступне:
![]() ,
(4)
,
(4)
що після логарифмування має лінійний вид:
ln(Vx*![]() )
= nB
)
= nB![]() ln(
ln(![]()
![]() (b-x))+nA
(b-x))+nA![]() ln(
ln(![]()
![]() (1-x))
+ E/R
(1-x))
+ E/R
![]() (1/Т)+lnkо.
(5)
(1/Т)+lnkо.
(5)
Значення nВ, nА, (-E/R), lnkо розраховуються за рівнянням (5)
Мета роботи: розрахунок в середовищі Excel порядків реакції і
енергії активації рівняння швидкості хімічної реакції в потоці.
Вихідні дані
Залежність
ступеня перетворення х
(частки) від часу перебування в зоні
реакції
![]() ,(c)
для 3 кінетичних кривих при температурі
Т=298+5·N,
К (N
– номер варіанту, дорівнює останній
цифрі залікової книжки студента):
,(c)
для 3 кінетичних кривих при температурі
Т=298+5·N,
К (N
– номер варіанту, дорівнює останній
цифрі залікової книжки студента):
|
№ точки |
х |
|
|
|
|
1 |
0,2 |
1,6/N |
0,4/N |
0,93/N |
|
2 |
0,3 |
2,68/N |
0,67/N |
1,53/N |
|
3 |
0,4 |
4,01/N |
1,0/N |
2,2/N |
|
4 |
0,5 |
5,7/N |
1,43/N |
3,13/N |
|
5 |
0,6 |
8,0/N |
2,0/N |
4,4/N |
|
6 |
0,7 |
10,5/N |
2,63/N |
5,83/N |
|
Концентрація А |
CА0 |
0,1 |
0,4 |
0,1 |
|
Конц. параметр |
b |
1,5 |
1,5 |
2,5 |
Алгоритм розрахунку
1. Розрахунок швидкості реакції при постійній температурі.
Побудувати для 3 кривих діаграму залежності ступеня перетворення x (функція) від часу
 (аргумент) (Увага!
Не навпаки!)
і апроксимувати кожну
криву рівнянням третього порядку:
(аргумент) (Увага!
Не навпаки!)
і апроксимувати кожну
криву рівнянням третього порядку:
 ,
,
де z1, z2, z3, z4 – коефіцієнти рівняння апроксимації
1.2 Розрахувати
швидкість реакції для 6 точок кожної
кривої при відповідному часі перебування:
![]()
Якщо швидкість в останній точці х=0,7 збільшується в порівнянні з попередньою або стає від‘ємною, для підвищення точності розрахунку останню точку необхідно відкинути і подальші розрахунки проводити для перших 5 точок.
2. Розрахунок кінетичних параметрів за рівнянням (3):
розрахувати значення ln(
 ·
(1-x)), ln(
·
(1-x)), ln( ·
(b-x)), ln(Vх·САо)
для кожної кривої, групувати колонки
значень в єдину таблицю без розривів
та заголовків між строками і колонками,
при цьому отримують матрицю з 3-х
колонок ln(
·
(b-x)), ln(Vх·САо)
для кожної кривої, групувати колонки
значень в єдину таблицю без розривів
та заголовків між строками і колонками,
при цьому отримують матрицю з 3-х
колонок ln( ·
(1-x)), ln(
·
(1-x)), ln( ·
(b-x)), ln(Vх·САо)
і
15 строк
(з урахуванням відкидання шостої точки
кожної кривої);
·
(b-x)), ln(Vх·САо)
і
15 строк
(з урахуванням відкидання шостої точки
кожної кривої);розрахувати значення nВ, nА, lnk* з використанням функції
ЛИНЕЙН, яка базується на методі найменьших квадратів.
Увага! Перед використанням функції ЛИНЕЙН необхідно зберегти (записати) файл програми тому, що при некоректному використанні цієї функції можливо «зависання» комп‘ютера. Функція ЛИНЕЙН може бути знайдена за допомогою меню: Вставка/Функции/Категория: Статистические. З можливостями функції ЛИНЕЙН необхідно ознайомитися за допомогою довідки.
У вікні, що з‘являється після вибору функції ЛИНЕЙН, необхідно ввести:
відомі значення y - колонка ln(Vх·САо), що містить значення для всіх 3 кривих;
відомі значення х - масив ln(
 ·
(1 - x)), ln(
·
(1 - x)), ln( ·
(b - x)) для всіх
3 кривих;
·
(b - x)) для всіх
3 кривих;конст - логичне значення, необхідно ввести 1;
статистика - необхідно ввести 0. Натиснути OK.
У комірці, що активована, з‘являється одне значення. Формулу необхідно вивести як формулу масиву. Для цього виділити вправо (в рядок) діапазон, що містить 3 комірки. Нажати клавишу F2, а потім одночасно клавиші CTRL+SHIFT+ENTER. Розраховані значення повертаються в порядку nВ, nА, lnk.
Розрахувати в окремих комірках значення n, k.
Зміна значень масиву, його копіювання або зміщення приводить до необхідності очистки усіх комірок, що містять формулу ЛИНЕЙН.
3. Оцінка адекватності рівняння швидкості реакції
Розрахувати за отриманим кінетичним рівнянням
![]()
значення шидкості для 5 точок кожної кривої. Розрахувати відносне відхілення, %, експериментальних Vx і розрахункових Vp значень швидкості. Визначити максимальне відхілення, зробити висновок щодо адекватності опису експериментальних даних отриманим кінетичним рівнянням (в кінетиці допускається максимальне відхілення до 15%)
3. Розрахунок кінетичних параметрів за рівнянням (4):
Матрицю
(таблицю), що отримано при виконання
п.2, необхідно розширити за рахунок
колонки 1/Т, при цьому отримують матрицю
з 4-х
колонок
1/Т, ln(![]() ·
(1-x)), ln(
·
(1-x)), ln(![]() ·
(b-x)), ln(Vх·САо)
і 30
строк.
Строки з 16 по 30 отримати за даними іншого
варіанту (при іншій температурі). Для
цього значення таблиці іншого студента
при іншій температурі копіювати у буфер
обміну і вставити з використанням правої
кнопки миші:
Специальная вставка
/Вставить/Значения
вниз
існуючої таблиці.
·
(b-x)), ln(Vх·САо)
і 30
строк.
Строки з 16 по 30 отримати за даними іншого
варіанту (при іншій температурі). Для
цього значення таблиці іншого студента
при іншій температурі копіювати у буфер
обміну і вставити з використанням правої
кнопки миші:
Специальная вставка
/Вставить/Значения
вниз
існуючої таблиці.
Послідовність операцій при використанні функції ЛИНЕЙН визначено в п.2 - виділити діапазон з 4 комірок в рядок для виводу значень nВ, nА, E/R, lnkо. Розрахувати в окремих комірках значення n, Е, k0. Розрахувати за рівнянням Арреніуса k для обох температур.
Індивідуальна самостійна робота
Округлити отримані порядки і константу швидкості рівняння (2) до цілих значень, аналітично інтегрувати отримане рівняння (по
 від
від
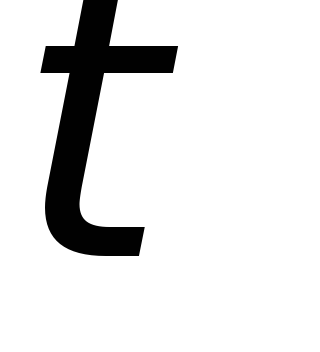 =0
до
=0
до =
= ;
пох
від х=0
до х=х),
розрахувати значення часу перебування
;
пох
від х=0
до х=х),
розрахувати значення часу перебування
 для
кожної точки 3-х кривих. Розрахувати
відносне відхилення (%) експериментальних
і розрахункових значень
для
кожної точки 3-х кривих. Розрахувати
відносне відхилення (%) експериментальних
і розрахункових значень
 .
.
Провести розрахунки за пунктами 1, 2 і 3 алгоритму з врахуванням початкової точки
 =0,
х=0для
3 кривих.
=0,
х=0для
3 кривих.
Контрольні питання
Визначення швидкості хімічної реакції. Закон діючих мас. Молекулярність реакції і порядок кінетичного рівняння. Рівняння Ареніуса. Фізико-хімічний сенс енергії активації і передекспоненційного множника. Інтегрування кінетичних рівнянь нульового, першого і другого порядків.
