
- •Лекция n 20-23. Растворы электролитов
- •1. Растворы электролитов. Слабые электролиты. Закон разбавления Оствальда
- •Растворы слабых электролитов
- •2. Сильные электролиты. Активность. Ионная сила раствора
- •3. Электролитическая диссоциация воды, рН раствора. Расчет рН растворов сильных и слабых электролитов..
- •Расчет рН растворов сильных и слабых электролитов.
- •4. Буферные растворы. Буферные системы живых организмов.
- •Типы буферных систем.
- •Расчет рН буферных растворов.
- •Механизм действия буферных систем
- •Буферные системы живого организма
- •3.Белковые буферные системы.
- •5. Гидролиз солей
- •Влияние различных факторов на гидролиз.
- •6. Равновесие в системе осадок – раствор электролита
- •Условия растворения и осаждения труднорастворимых электролитов
- •7. Равновесия в растворах комплексных соединений
- •Токсичность солей тяжелых металлов
Токсичность солей тяжелых металлов
Хорошо известно, что загрязнение окружающей среды соединениями токсичных элементов — тяжелых металлов: ртути, свинца, кадмия, хрома, никеля — может приводить к отравлениям. Токсичность таких соединений основана на вытеснении ионами тяжелых металлов биогенных элементов (Mn, Fe, Zn, Co) из бионеорганических комплексов, что может быть обусловлено как большей прочностью вновь образующихся комплексов, так и более высокой концентрацией токсичных ионов. В результате нормальная жизнедеятельность нарушается и начинается токсикоз.
Свойство ионов тяжелых металлов образовывать прочные связи с серусодержащими лигандами используется при подборе лекарств, применяемых для лечения при таких отравлениях. Такие лекарства имеют общее название — антидоты.
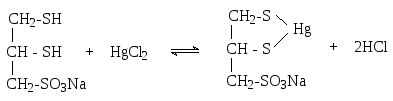
Например, в нашей стране с успехом используется отечественный препарат унитиол. Это хорошо растворимая соль, в молекулу которой входят две сульфгидрильные группы. Благодаря их присутствию унитиол обладает высокими антидотными свойствами и успешно применяется при отравлениях мышьяком, ртутью, кадмием, свинцом, хромом, кобальтом и некоторыми радиоактивными элементами. Как пример приведем реакцию с сулемой:
В качестве антидотов при отравлении Zn, Сu и Нg применяют также комплексоны. В медицинской практике наиболее широко используют комплексон (ЭДТА) — этилендиаминтетрауксусную кислоту, которая известна еще как трилон А, а ее динатриевая соль Na2ЭДТА — трилон Б.
Соли комплексонов называются комплексонатами, образуются они за счет взаимодействия ионов металлов и протонов СООН-групп, а также за счет донорно-акцепторного взаимодействия азота комплексона и ионов металла. Образующиеся комплексонаты, как правило, хорошо растворимы и характеризуются низкими константами нестойкости. В лечебной практике применение комплексонов основывается именно на том, что они, выступая в роли лигандов, образуют более прочные комплексы с ионами металлов, чем комплексы этих же ионов с серосодержащими группами белков, ферментов, аминокислот.
Комплексонат СаNа2ЭДТА (или CaNa2Y), известный в медицинской практике как тетацин, широко используется в лечебных целях как антидот при отравлениях ионами тяжелых металлов. Ионы ртути и кадмия вытесняют кальций из тетацина, так как образуют более прочные связи с кислородом и азотом комплексона:
СaY2- + Hg2+ = HgY2- + Ca2+
![]()
Комплексонаты ртути и кадмия с тетацином малотоксичны, имеют низкие константы нестойкости, в организме не разрушаются, легко выводятся через почки.
