
- •КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- •Сложные вещества, полученные взаимодействием соединений первого порядка, но не путем простого замещения в
- •Координационная теория Вернера
- •Виды комплексов
- •Внутренняя сфера состоит из центрального атома (комплексообразователя), а вокруг него находятся (координируются) лиганды.
- •Характеристики центрального атома: 1)степень окисления (заряд атома)
- •2) Координационное число (КЧ) - количество химических связей, которые комплексообразователь образует с лигандами.
- •Координационное число зависит от природы, степени окисления комплексообразователя, природы лиганда и условий реакции.
- •Лиганды не связаны друг с другом, и между ними действуют силы отталкивания.
- •3) По координационной емкости
- •В комплексном соединении [Co(NH3)4CO3]NO3 бидентатный лиганд – ион CO32- образует две связи с
- •Лиганды, способные образовывать две и более связи называются полидентантными.
- •Если в комплексе содержатся два и более комплексообразователя, то этот комплекс называется
- •2) Если атомы комплексообразователя связаны между
- •Номенклатура комплексных соединений
- •Комплексные соединения с комплексным анионом.
- •Комплексные соединения с комплексным катионом.
- •Нейтральные комплексы
- •Многоядерные комплексы
- •Геометрические изомеры
- •Строение комплексных соединений
- •Изомерия комплексных соединений
- •2) Геометрическая изомерия
- •3) Оптическая изомерия (зеркальная изомерия).
- •4) Сольватная (гидратная) изомерия
- •5) Ионная изомерия
- •Устойчивость комплексных соединений
- •Диссоциация имеет два этапа:
- •Процесс комплексообразования завершается, когда у комплексообразователя исчерпаны все валентные возможности.
- •Процесс диссоциации характеризуется величиной константой нестойкости.
- •Примеры образования и разрушения комплексов
- •3) Реакция:
- •Теория валентных связей
- •Ион [MnCl4]2- содержит пять не спаренных электронов на 3d-орбитали и вакантные 4s- и
- •Гибридизация орбиталей и структура комплексов
- •При объединении двух электронов 3d-подуровня в пару и высвобождение одной из квантовых ячеек
- •Если в гибридизации участвуют атомные орбитали внешнего d-подуровня, то комплекс парамагнитен и называется
- •Гексафтороферрат(II)-ион [FeF6]4- - парамагнитный
- •Гексацианоферрат(II)-ион [Fe(CN)6]4- - диамагнитный
- •Теория кристаллического поля
- •Октаэдрическое расположение лигандов
- •Атомные орбитали, вытянутые вдоль осей координат, ближе всего подходят к лигандам. Между ними
- •Три d-АО, расположенные между осями координат и между лигандами, находятся на значительном расстоянии
- •Пять одинаковых d-АО комплексообразователя, попадая в поле лигандов, подвергаются расщеплению на две группы
- •Разность энергий двух новых подуровней d и d – это
- •Выигрыш энергии за счет заселения электронами d - атомных орбиталей называют энергией стабилизации
- •Заселение d - и d
- •При низком значении параметра расщепления (слабое поле лигандов) электроны преодолевают энергетический барьер, разделяющий
- •При сильном поле лигандов и высоком значении 0 заселение четвертым и пятым электроном
- •Шестой, седьмой и восьмой электроны в случае слабого поля оказываются снова на d
- •В случае сильного поля лигандов шестой электрон заселяет d -АО, приводя к диамагнетизму
- •Заселение орбиталей девятым и десятым электроном также не различается для комплексов обоих типов:
- •Строение октаэдрического комплексного ионов [CoF6]3-. Фторид-ион F- – лиганд слабого поля.
- •Цветность комплексных соединений
- •Избирательность поглощения света зависит: 1)от степени окисления комплексообразователя; 2)от вида лигандов.

В комплексном соединении [Co(NH3)4CO3]NO3 бидентатный лиганд – ион CO32- образует две связи с комплексообразователем – условным ионом Co(III), а каждая молекула лиганда NH3 – только одну связь.

Лиганды, способные образовывать две и более связи называются полидентантными.
Пример гексадентатного лиганда - анион этилендиаминтетрауксусной кислоты:
Этот тип лигандов способен несколькими связями, пространственно отдаленными друг от друга, вцепляться в центральный атом и называются хелатными, ''клешнеобразными''.
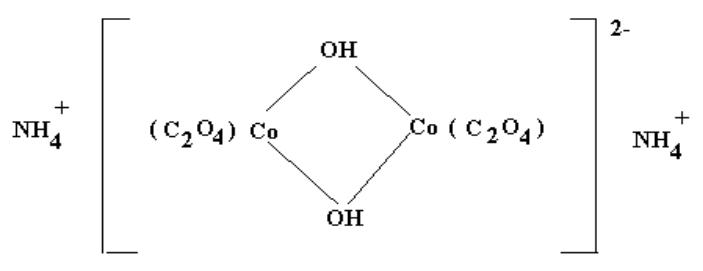
Если в комплексе содержатся два и более комплексообразователя, то этот комплекс называется
многоядерным.
Делятся на мостиковые, кластерные и смешанного типа.
1) В мостиковых комплексах полидентантные лиганды связывают частицы комплексообразователя.

2) Если атомы комплексообразователя связаны между
собой непосредственно, то комплекс относят к кластерному типу.
Например, [Re2Cl8]2-:
3) Многоядерные комплексы смешанного типа содержат как связь комплексообразователь– комплексообразователь, так и мостиковые лиганды.

Номенклатура комплексных соединений
Лиганд |
Название |
Лиганд |
Название |
|
CH COO- |
ацетато |
NO- |
нитрозо |
|
3 |
|
|
|
|
CN- |
циано |
NO - |
нитро |
|
|
|
|
2 |
|
CO 2- |
карбонато |
O 2- |
пероксо |
|
|
3 |
|
2 |
|
C O 2- |
оксалато |
OH- |
гидроксо |
|
2 |
4 |
|
|
|
Cl- |
хлоро |
SO32- |
сульфито |
|
H- |
гидридо |
SO S2- |
тиосульфато |
|
|
|
|
3 |
|
H2O |
аква |
NH3 |
аммин |
|
NO |
нитрозил |
CO |
карбонил |
|
SO2 |
диоксосера |
PF3 |
трифторофосфор |
|
NH2(CH2)2NH2 |
этилендиамин |
N2H5+ |
гидразиний |
|
(NH2)2CO |
карбамид |
NO+ |
нитрозилий |
|
Комплексные соединения с комплексным анионом.
Указывается число и название лиганда, комплексообразователь по латински с окончанием -ат (феррат, никелат, хромат, купрат). Число
лигандов в комплексе обозначают греческими приставками ди, три, тетра, пента, гекса и т.д.
Степень окисления металла в комплексе указывается в скобках после названия комплекса:
Na[Al(OH)4] – Тетрагидроксоалюминат натрия K2[PtCl6] – Гексахлороплатинат (IV) калия
Ag - аргент- ; Au - аур- ; Cu - купр- ; Fe - ферр- ; Hg - меркур- ; Mn - манган- ; Ni - никкол- ; Pb - плюмб- ; Sb - стиб- ; Sn - станн-.
Комплексные соединения с комплексным катионом.
Сначала указывается название аниона, затем число и названия лиганда и
комплексообразователя |
по-русски |
в |
родительном падеже |
(для многоядерных |
|
комплексов – с указанием их числа). Обозначение степени окисления комплексообразователя дают римскими цифрами в скобках после названия:
[Zn(NH3)4]Cl2 – хлорид тетраамминоцинка. [Сu(H2O)6]SO4– сульфат гексааквомеди(II)
Нейтральные комплексы
Названия состоят из одного слова.
Указывается число и названия лигандов (для лигандов каждого вида отдельно), затем название центрального атома в именительном падеже (в случае многоядерных комплексов – с указанием числа центральных атомов).
Например:
[СоС13(Н2О)3] – триакватрихлорокобальт (III) [Cr2(CO)8] – октакарбонилдихром
Многоядерные комплексы
Названию мостиковых групп предшествует греческая буква , которая повторяется перед названием мостикового лиганда каждого вида.
Сначала называют мостиковые в порядке их усложнения, затем не мостиковые, а после этого – комплексообразователи с указанием их числа.
Например:
[(NH3)5Co – NH – Co(NH3)5]Cl5
хлорид ( -амидо)-декаамминодикобальта(III) или
хлорид ( -амидо)-бис{пентаамминокобальта(III)}

Геометрические изомеры
Приставка цис-, если одинаковые по составу лиганды занимают соседнее положение по отношению к комплексообразователю.
Транс-, когда лиганды находятся в противоположных положениях.
Например, дихлородиамминоплатина(II) [Pt(NH3)2Cl2]0 имеет два геометрических изомера:
В случае оптических изомеров к названию добавляется латинская буква L в случае левовращающих изомеров или D
– для правовращающих
