
- •Химия и биохимия липидов Методические указания к выполнению лабораторных работ для студентов специальностей
- •Учебное издание
- •Введение
- •1 Классификация липидов и природных жиров
- •Стериды
- •Глицерофосфолипиды
- •Гликолипиды
- •Сфингофосфолипиды
- •Биологическая роль липидов
- •Жирные кислоты
- •Номенклатура
- •Изомерия
- •Обмен липидов
- •Определение содержания сырого жира в аппарате Сокслета
- •Определение общих липидов по цветной реакции с сульфофосфованилиновым реактивом
- •Качественное определение ненасыщенности жиров пробой с раствором брома
- •Прогоркание жиров
- •Гидролитическое прогоркание жиров
- •Определение активности триацилглицерол-липазы
- •Кинетика действия липазы
- •Гидролитическое расщепление жира под действием липазы
- •Определение числа омыления
- •Определение кислотного числа
- •Определение эфирного числа
- •Окислительное прогоркание жиров
- •Определение активности липоксигеназы
- •Определение йодного числа жиров
- •Определение перекисного числа
- •Анализ карбонильных соединений
- •Фосфолипиды
- •Выделение лецитинов из яичного желтка
- •Гидролиз лецитина и определение продуктов гидролиза
- •Список использованной литературы
Определение перекисного числа
Указанное число показывает суммарное количество перекисей, образовавшихся при окислении как ненасыщенных, так и насыщенных жирных кислот. Образование гидроперекисей в случае насыщенных жирных кислот происходит с меньшей скоростью в сравнении с ненасыщенными. Однако и в этом случае образуется свободный перекисный радикал:
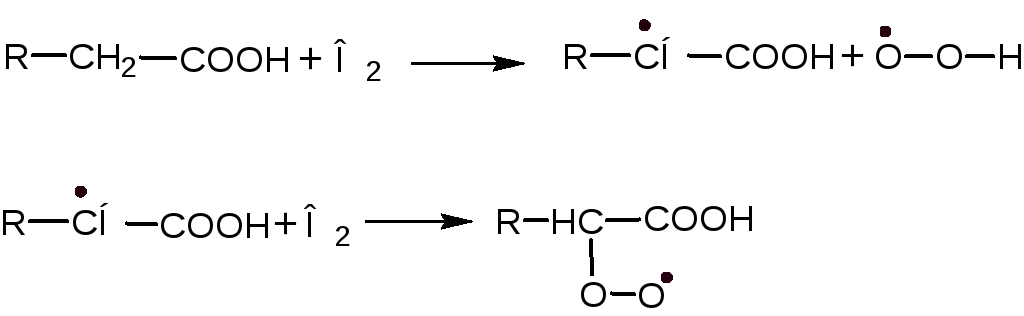
При взаимодействии с другими жирными кислотами свободный перекисный радикал стабилизируется, «отрывая» от них атом водорода:

Образовавшийся новый радикал взаимодействует с кислородом по прежней схеме:
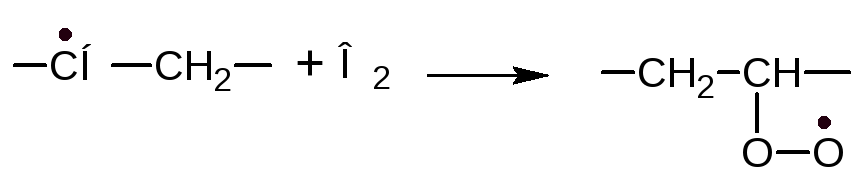
Свободный перекисный радикал может превратиться в альдегиды путем его изомеризации с образованием нестойкой диалкилперекиси:

Образующиеся гидроперекиси могут также активно превращаться в кетоны:

Доказано также, что гидроперекиси могут взаимодействовать с двойными связями ненасыщенных жирных кислот с образованием эпоксидов:

Именно набор всех вышеуказанных соединений с различной молекулярной массой и обуславливает наличие в хранящемся молочном жире таких пороков вкуса как «салистый», «олеистый», «рыбный», «грибной» и т.д.
Сильнейшими активаторами окисления являются ионы металла.
Принцип метода: количественное определение перекисей в масле основано на реакции выделения йода перекисями из йодата калия в кислой среде (пример циклической перекиси):

Выделившийся йод оттитровывают раствором тиосульфата.
Техника определения: в конической колбе или склянке с притертой пробкой емкостью 200 см3 отвешивают на аналитических весах около 2-3 г масла. Навеску растворяют в 20 см3 смеси ледяной уксусной кислоты и хлороформа (2:1), прибавляют 5 см3 насыщенного раствора йодистого калия, сосуд закрывают пробкой и ставят в темное место на 10 минут, после чего добавляют 50 см3 дистиллированной воды и оттитровывают выделившийся йод 0,002 н. раствором тиосульфата (индикатор-крахмал). Одновременно проводят также контрольное определение (без масла). Перекисное число (ПЧ) (количество граммов йода, выделенного перекисями, содержащимися в масле) рассчитывают по формуле
![]() ,
,
где Vк – количество 0,002 н. раствора тиосульфата, израсходованное при титровании контрольного образца, см3;
V0 – количество 0,002 н. раствора тиосульфата, израсходованное при титровании опытного образца, см3;
k – поправочный коэффициент раствора тиосульфата;
0,0002538 – титр 0,002 н. раствора тиосульфата по йоду (1 см3 раствора соответствует 0,0002538 г йода);
m – навеска масла, г.
Анализ карбонильных соединений
К вторичным продуктам окисления относятся спирты, карбонильные соединения, эфиры, кислоты, а также соединения со смешанными функциями, такие как оксикислоты, эпоксисоединения и др. Все вторичные продукты окисления появляются в результате тех или иных превращений гидроперекисей, причем часть вторичных продуктов образуется непосредственно при распаде гидроперекисей, а часть – в результате дальнейших реакций.
Принцип метода: анализ карбонильных соединений проводят фотоколориметрированием щелочных растворов 2,4-динитрофенилгидразонов, поглощающих при 430 и 460 нм.
Техника определения: в мерную колбу на 25 см3 помещают 1,5 см3 4,3 %-го раствора трихлоруксусной кислоты (ТХУ), добавляют 2,5 см3 0,05 %-го раствора 2,4-динитрофенил-гидразина в бензоле и 2,5 см3 раствора липидов в бензоле. Смесь нагревают 30 минут при температуре 60 0С, после охлаждения добавляют 5 см3 4 %-го раствора КОН в этаноле и измеряют оптическую плотность растворов при 430-460 нм. Контролем служит смесь реагентов без липидов. Рассчитывают концентрацию насыщенных С1 (в ммоль/кг) и мононенасыщенных С2 (в ммоль/кг) карбонильных соединений по формулам:
![]() ,
,
![]()
![]() ,
,
где m – навеска липидов, г.
Используют растворители, свободные от карбонильных соединений.
Для исключения ошибки, за счет карбонильных соединений, образующихся в процессе анализа при распаде пероксидов, в оксидатах предварительно удаляют пероксиды путем добавления к пробе уксусной кислоты и йодата калия, выдерживают в течение 20 минут в темноте, разбавляют водой и титруют тиосульфатом.
Материала, реактивы и оборудование: 4,3 %-й раствор трихлоруксусной кислоты (ТХУ); 0,05 %-й раствор 2,4-динитрофенилгидразина в бензоле; 4 %-й раствор КОН в этаноле; раствор липидов в бензоле; этанол, масло; смесь уксусной кислоты с хлороформом (2:1); йодистый калий, спиртовой раствор; тиосульфат, 0,002 н. раствор; крахмал 0,5 %-й раствор; конические колбы с притертыми пробками на 250 см3; мерные цилиндры; пипетки; бюретка; аналитические весы, фотоэлектроколориметр, баня, мерные колбы.
