
Контрольные задания-2009
.pdfМинистерство образования Республики Беларусь
Учреждение образования «МОГИЛЕВСКИЙГОСУДАРСТВЕННЫЙУНИВЕРСИТЕТПРОДОВОЛЬСТВИЯ»
Кафедра химической технологии высокомолекулярных соединений
МЕТОДИЧЕСКИЕ УКАЗАНИЯ И КОНТРОЛЬНЫЕ ЗАДАНИЯ
ПО КУРСУ «ОРГАНИЧЕСКАЯ ХИМИЯ»
для студентов специальностей технологии продовольственных продуктов заочной формы обучения
Могилев 2009

2
УДК 547 (07)
Рассмотрены и рекомендованы к изданию на заседании кафедры ХТВМС
Протокол № 8 от 30 июня 2009 г.
Составители:
профессор, д.х.н. Роганов Г.Н., доцент, к.х.н. А.Я. Гузиков, ст. преподаватель Писарев П.Н.
Рецензент кандидат химических наук, доцент УО МГУП
Баранов О.М.
Аннотация. Настоящее методическое пособие содержит тексты задач и упражнений по органической химии, охватывающих все разделы изучаемого курса. В соответствии с учебным планом для специальностей технологии продовольственных продуктов задания входят в состав двух контрольных работ. Каждая контрольная работа содержит по девять задач как теоретического, так и практического плана. Выбор варианта каждого номера задачи проводят по двум последним цифрам шифра зачетной книжки.
УО «Могилевский государственный университет продовольствия», 2009
3
Содержание
Введение |
4 |
Общие методические указания………………………………...................... |
5 |
Контрольная работа №1………………………………............................... |
20 |
1.Углеводороды…………………………………………………………….. 20
2.Гидроксисоединения…………………………………………………….. 23
3. |
Карбонильные соединения……………………………………………… |
27 |
4. |
Карбоновые кислоты и их производные.………………………………. |
31 |
Контрольная работа №2………………………………………………….. |
35 |
|
5. |
Гидроксикислоты, оптическая изомерия …………................................ |
35 |
6.Амины. Аминокислоты……………………………….............................. 39
7.Углеводы………………………………………………………………….. 43
8.Жиры, терпены.…………………………………………………………... 46
9. Гетероциклические соединения………………………………………… 48
4
ВВЕДЕНИЕ
Органическая химия является одной из основополагающих теоретических дисциплин при подготовке инженеров – технологов для пищевой промышленности и общественного питания. Она является базой для глубокого понимания процессов, происходящих в продуктах растительного и животного происхождения во время их заготовки, хранения и переработки. Современная технология хранения и переработки сельскохозяйственного сырья, получение из него пищевых продуктов требуют соответствующих знаний, химических и биохимических процессов, протекающих на всех этапах производства продуктов питания. Без глубокого знания закономерностей изучаемых органической химией, невозможно в дальнейшем полноценное изучение биологической химии, микробиологии, физиологии животных и растений, других специальных технологических дисциплин.
В преподавании органической химии (современные теоретические представления, общие закономерности и в то же время свойства наиболее важных органических соединений и др.) значительное внимание уделяется упражнениям проводимым параллельно лекционному курсу, что является одной из эффективных форм самостоятельной работы студентов. Особое значение этот вид работы имеет для студентов заочной формы обучения, где он представлен в виде самостоятельных контрольных заданий.
Студенты – заочники специальностей технологии продовольственных продуктов выполняют две контрольные работы по органической химии. Студенты, выполнившие контрольные работы, а также лабораторный практикум в соответствии с рабочей программой допускаются к экзамену по органической химии.
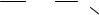
5
ОБЩИЕ МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Настоящие контрольные задания содержат тексты задач и упражнений по органической химии, охватывающих все основные разделы изучаемого курса «Органическая химия».
Учитывая особую важность усвоения отдельных разделов органической химии для студентов пищевых специальностей (в частности, гидроксисоединения, оксосоединения, карбоновые кислоты и их функциональные производные, гидрокси– и аминокислоты, углеводы) количество задач в этих разделах удвоено и они имеют несколько больший объем и повышенную трудность по сравнению с другими разделами.
При составлении ответов на вопросы контрольной работы необходимо, прежде всего, отобрать наиболее существенное, касающееся данного вопроса и дать исчерпывающий, лаконичный, непосредственно относящийся к данному вопросу ответ. Следует избегать длинных описаний и дополнительных объяснений, пере-
писанных из учебников. Нужно сопровождать свои ответы химическими
уравнениями, структурными и проекционными формулами, необходимыми пояснениями. Совершенно недопустимо изображение органических соединений с помощью молекулярных формул, формула органического соединения должна давать представление не только о составе, но и о том к какому классу относится данное соединение (спирты, альдегиды, кетоны, кислоты и др.). Например, формулу пропионовой кислоты не следует писать С3Н6О2; необходимо дать структурную формулу:
 O H3C СН2 С
O H3C СН2 С
OH
Под приведенной структурной формулой следует писать названия соединений по предложенной номенклатуре: заместительной (ИЮПАК), тривиальной, рациональной.
При изучении органической химии студент сталкивается с наличием огромного фактического материала, поэтому необходимо уметь выделить в нем главное, найти взаимную связь различных классов соединений; это достигается только систематическим, последовательным и вдумчивым изучением материала. Приступая к изучению каждого раздела, в первую очередь следует уяснить строение и свойства функциональной группы, т.е. группы определяющей в основном химические свойства данного класса соединений, в особенности качественные реакции.
Знание свойств различных классов соединений позволяет найти естественную связь между отдельными классами, т.е. дает возможность уяснить систему органической химии в целом. Изучение курса органической химии рекомендуется вести по темам (классам соединений) в следующей последовательности:
1)общая формула;
2)изомерия, номенклатура;
3)источники и способы получения (промышленные, лабораторные);

6
4)строение функциональной группы, определяющей основные физические и химические свойства данного класса соединений;
5)химические свойства;
6)отдельные представители, их получение, применение.
Усвоению материала способствует краткий конспект.
После изучения каждой темы можно приступать к выполнению задания по данной теме.
Оформление контрольной работы должно отвечать следующим требованиям: a) работа должна быть написана в тетради, разборчиво и аккуратно;
б) на обложке тетради указываются фамилия, имя и отчество, номер контрольной работы, номер группы и шифр студенческого билета и зачетной книжки;
в) на первой странице следует указать номер варианта и номера всех задач соответствующих данному варианту (из таблицы 1.)
г) на каждой странице следует оставлять свободные поля для указаний рецензента;
д) отвечать на вопросы и решать задачи необходимо в той последовательности, в какой они приводятся в контрольных заданиях;
е) необходимо записывать номер задачи и полностью ее содержание; ж) в конце работы приводится список использованной литературы, простав-
ляется дата и подпись.
Если работа не будет удовлетворять этим требованиям, то она будет возвращена без проверки.
Выбор варианта контрольного задания проводится по двум последним цифрам шифра студенческого билета и зачетной книжки. Например, если последние две цифры шифра 5 и 2, то решайте задачи 52-го варианта. Номера задач каждого варианта указаны в таблице 1.
В качестве примеров выполнения контрольных заданий приведены решения нескольких задач из двух контрольных работ.
Задача 1. Получите вторичный и третичный бутиловые спирты по методу Гриньяра и напишите для них уравнения реакций : а)внутри- и межмолекулярной дегидратации; б) с пятихлористым фосфором.
Решение: Получение втор-бутилового спирта:
|
|
|
|
|
|
|
|
|
|
О |
|
эфир |
H C |
|
|
CH |
|
|
|
CH |
|
CH |
|
|
|
|||||||||
H C |
|
СН |
|
|
|
|
|
+ CH MgI |
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
2 |
|
|
С |
|
|
|
3 |
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
3 |
|
|||||||||
3 |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
H+ |
|
|
|
|
|
|
|
|
|
OMgI |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
H C |
|
|
|
CH |
|
|
|
CH |
|
CH |
+ |
H O |
|
|
H3C |
|
|
|
CH2 |
|
|
|
|
CH |
|
CH3 + Mg(OH)I |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
3 |
|
|
|
|
|
2 |
|
|
|
3 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
OMgI |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
втор-бутиловый спирт |
|||||||||||||||
Получение трет-бутилового спирта:

7
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
OMgI |
|
|
||||||
|
|
|
|
|
|
|
|
|
эфир |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
СН |
3 |
|
С |
|
+ CH3MgI |
|
|
|
|
СН3 |
|
|
С |
|
|
|
CH3 |
|
||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|||||||
|
|
|
|
OMgI |
|
|
|
H+ |
|
OH |
|
|
||||||||||||
СН |
|
|
|
|
|
|
|
|
+ H O |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
С |
|
|
CH |
|
|
|
СН |
|
|
С |
|
CH |
+ Mg(OH)I |
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
3 |
|
|
|
|
|
3 |
2 |
|
3 |
|
|
|
|
|
|
|
3 |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
трет-бутиловый спирт |
|||||||
Внутримолекулярная дегидратация спиртов (протекает по правилу Зайцева):
t1
H3C |
|
|
|
СH2 |
|
|
|
CH |
|
|
CH3 |
|
|
|
|
|
H3C |
|
|
CH |
|
CH |
|
CH3 |
+ H O |
|||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2SO4 (к) |
|
|
|
|
|
|
|
|
|
|
2 |
||||
|
|
|
|
OH |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
t2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
C |
|
|
CH2 |
|
|||||||
H C |
|
|
C |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
3 |
|
|
|
|
|
|
|
|
|
|
3 H SO |
4 (к) |
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
||||||||||
Межмолекулярная дегидратация спиртов идет с хорошими выходами с первичными спиртами. В случае вторичных и особенно третичных спиртов в продуктах преобладают алкены (т.е. дегидратация протекает внутримолекулярно).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
t ' |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
H3C |
|
|
СH2 |
|
|
|
CH O HC |
|
|
CH2 CH3 + H2O |
||||||||
H3C |
|
|
|
СH2 |
|
|
|
CH |
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
H SO |
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 4 (к) |
|
|
|
|
|
|
|
|
СH3 |
CH3 |
||||||||||
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
CH |
|
CH3 |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
t |
' |
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H3C |
|
|
C |
|
|
CH3 |
2 |
|
H3C |
|
|
|
C |
|
|
O |
|
|
C |
|
CH3 |
+ H O |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
H2SO4 (к) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|||||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
CH3 |
|
CH3 |
|
|
|
|
||||||||||||||||
Последняя реакция даёт незначительные выходы продукта из-за стерических препятствий при протекании реакции, поэтому дегидратация трет-бутилового спирта протекает преимущественно внутримолекулярно.
Следует отметить, что t1 > t'1; t2. > t'2.
б) Реакции спиртов с пятихлористым фосфором: при действии неорганических галогенангидридов на третичные и вторичные спирты происходит в основном обмен гидроксила на галоген:
8
H3C |
|
|
CH2 |
|
|
CH |
|
CH3 + PCl5 |
|
|
H3C |
|
|
CH2 |
CH |
|
CH3 + HCl + POCl3 |
||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
||||||||||||||||||||||
|
|
|
OH |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|||||||
H3C |
|
|
|
|
|
|
|
|
|
+ PCl5 |
|
|
|
|
|
|
|
|
|
CH3 + HCl + POCl3 |
|||||
|
|
C |
|
CH3 |
|
|
H3C |
|
C |
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
||||||
Задача 2 Из толуола получите бензиловый спирт и пара-крезол. Какое из этих соединений реагирует со щелочью? Почему? Напишите уравнения реакций.
Получение пара-крезола:
NaOH
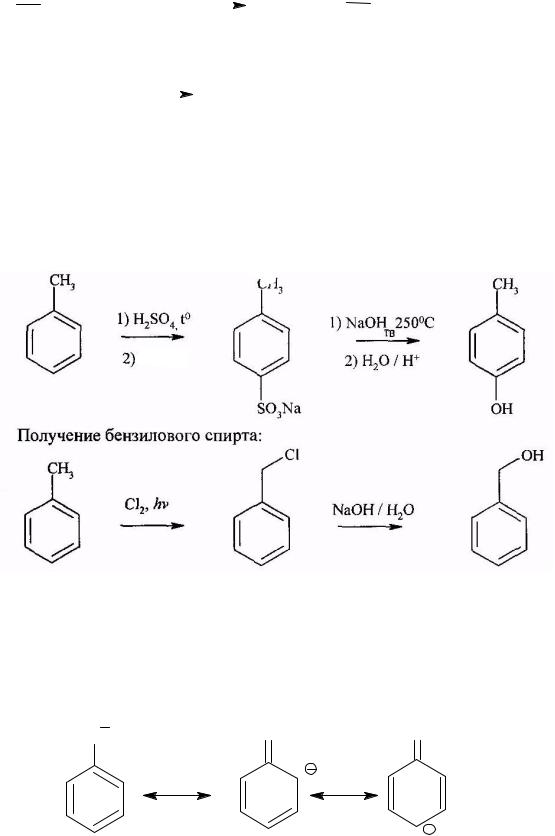
Из этих двух веществ со щелочью реагирует пара-крезол, т.к. в нем гидроксильная группа присоединяется непосредственно к ароматическому кольцу, вследствие чего неподеленные пары кислорода могут участвовать в сопряжении ароматического кольца. Поэтому крезолят-анион гораздо более устойчив, это можно проиллюстрировать набором резонансных структур для него:
O O O
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||
|
CH |
CH3 |
|||||
3 |
|
|
|
|
|
|
|
Для бензилового спирта подобного не наблюдается, по своим свойствам он схож с обычными спиртами и не реагирует со щелочами:

9
Задача 3.Получите масляную кислоту из бромистого пропила всеми известными Вам способами Получите изопропиловый эфир масляной кислоты тремя способами
Решение: Получение масляной кислоты из бромистого пропила;
1) CH3CH2CH2Br + КCN → CH3CH2CH2CN + KBr; t
CH3CH2CH2CN + 2H2O → CH3CH2CH2COONH4;
CH3CH2CH2COONH4 + HCl → CH3CH2CH2COOH + NH4Cl.
эфир
2) CH3CH2CH2Br + Mg → CH3CH2CH2MgBr;
эфир
CH3CH2CH2MgBr + CO2 → CH3CH2CH2COOMgBr;
CH3CH2CH2COOMgBr + HBr → CH3CH2CH2COOH + MgBr2.
t
3) CH3CH2CH2Br + КOH → CH3CH = CH2+ KBr + H2O;
спирт
t,p
CH3CH = CH2 + СO + H2O → CH3CH2CH2COOH.
H2SO4
Получение изопропилового эфира масляной кислоты:
I способ:
|
|
|
|
|
|
|
|
t |
O |
||||
CH CH CH COOH +H3C |
|
|
|
|
|
|
+ H2O |
||||||
|
CH |
|
CH3 |
|
|
H3C |
|
CH2 CH2 C |
|
||||
|
|
|
|
|
|
||||||||
|
|
|
|||||||||||
|
|
|
|
|
|
||||||||
3 |
2 |
2 |
|
|
|
|
H2SO4 (к) |
O |
CH CH3 |
||||
|
|
|
HO |
||||||||||
|
|
|
|
|
|
|
|
CH3 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||
10
II способ:
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|||
H3C |
|
CH2 CH2 C |
+ H3C |
|
HC |
|
CH3 |
|
H3C |
|
CH2 CH2 C |
|
|
|
+ HCl |
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
Cl |
|
|
OH |
|
|
|
|
O |
|
|
CH CH3 |
||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
III способ:
|
|
|
|
|
|
|
|
|
|
O |
|
|
+ NaBr |
CH CH CH COONa + H3C |
|
CH |
|
CH3 |
|
H3C |
|
CH2 CH2 C |
|
|
|||
|
|
|
|
|
|
||||||||
3 |
2 |
2 |
|
|
|
|
|
|
|
O |
CH |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|||
Br
H3C
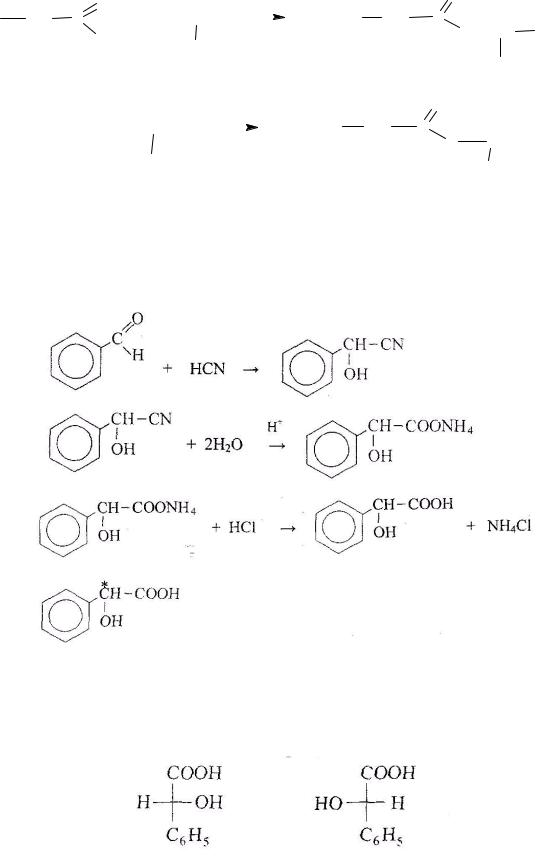
Задача 4. Получите миндальную кислоту (фенилоксиуксусную) из бензальдегида. Будет ли это соединение оптически деятельным и в скольких стереоизомерных формах оно существует?
Решение:
Миндальная кислота содержит один асимметрический атом углерода( помечен звездочкой) поэтому имеет два оптических изомера: N=2 n (N-число оптических изомеров; n- число асимметрических атомов углерода). Для данного случая: n =1; N=21=2:
Д-изомер L -изомер
