
- •Билет №2
- •2) В инфекционное отделение больницы был доставлен пациент, проработавший геодезистом-картографом на вырубленных территориях тайги. Ему был поставлен диагноз – весенне-летний энцефалит.
- •Билет №3
- •1. Что такое сцепленное с полом наследование? Объясните сцепленное с х-хромосомой наследование.
- •Классификация типов наследования признаков при моногенном наследовании.
- •Классификация типов наследования признаков при полигенном наследовании.
- •1. В середине 40-х годов χχ века было установлено, что обеспечение свойств наследственности и изменчивости связано с молекулой днк.
- •2. Наиболее частый порок сосудов у человека – персистирование Ботталова протока.
- •4. Практический навык: составьте родословную семьи с ахондроплазией.
- •1. У прокариот установлена оперонная модель регуляции экспрессии генов, что было доказано в 1961 году французскими микробиологами Жакобом и Моно на примере лактозного оперона у кишечной палочки.
- •4. Практический навык:
- •1. В природе существ. Знач. Разнообразие клеток. Число же главных типов клеточн. Организации ограничено 2-мя.
- •1.Перечислить типы клет. Организации. Назовите представителей клеток каждого типа?
- •2.Основные черты строения про- и эукариотических клеток?
- •3. Особенности организации генетического материала у про- и эукариот?
- •4. Биоконцентрирование или Биоаккумуляция. Примеры?
- •5. Ксенобиотики. Превращение ксенобиотиков в организме человека?
- •1. Назовите этапы формирования жевательной поверхности зубов млекопитающих и человека
- •2. Охарактеризуйте типы прикрепления зубов к челюсти.
- •3. Из каких зародышевых листков развиваются эмаль, дентин, и пульпа зуба?
- •4. Какие эволюционные преобразования зубной системы отмечаются у человека?
- •5. Происхождение онто-филогенетических пороков зубной системы человека:
- •4. Поперечный срез аскариды. Локализация в теле человека, заболевание?
- •Билет16
- •3) Гипоплазия эмали (тонкая зернистая эмаль, зубы светло-бурого цвета) наследуется как сцепленный с х-хромосомой доминантный признак.
- •II Проверка практических навыков
- •3. Синтез днк идет только в направлении 5¢ - 3¢, а так как две матричные цепи днк антипараллельны, то и образование дочерних цепей идет в противоположных направлениях.
- •3. В практике стоматолога встречаются пороки зубо-челюстной системы: сверхкомплектные зубы, наличием трем и диастем, конические зубы.
- •4. Практический навык: составьте родословную семьи с ахондроплазией.
- •1.Назовите стадии овогенеза и объясните уменьшение числа овоцитов.
- •Эволюция двух первых жаберных (висцеральных) дуг в ряду позвоночных:
- •1.Перечислите основные элементы челюстной и подъязычных дуг.
- •2.Чем характеризуется каждый тип сочленения?
- •3.Для каких классов позвоночных характерны данные типы сочленения. С какими эволюционными событиями связан переход от одного типа сочленения к другому?
- •4.В состав каких структур включаются элементы челюстной и подъязычной висцеральных дуг?
- •5.Назовите онто-филогенетически обусловленные пороки развития у человека, связанные с эволюционными преобразованиями висцеральных дуг.
- •- Отсутствие слухового прохода и евстахиевой трубы
- •1)У человека при оплодотворении к яйцеклетке приближается большое кол-во сперматозоидов, но сливается с ней только один. Это явление получило название моноспермия.
- •1. Какие процессы препятствуют проникновению других сперматозоидов в клетку?
- •2.Назовите стадии оплодотворения и охарактеризуйте их.
- •3.Объясните роль гамонов в оплодотворении.
- •Билет17
- •3)В практике стоматолога встречаются пороки зубо-челюстной системы: сверхкомплектные зубы, наличие трем и диастем, конические зубы.
- •I. Используя знания теории оперона Жакоба-Моно, какие механизмы регуляции экспрессии генов реализуются в бактериальных клетках.
- •5.Назовите онто-филогенетически обусловленные пороки развития у человека, связанные с эволюционными преобразованиями висцеральных дуг.
- •4. Анализ кариограммы
- •2. Каков жизненный цикл данного паразита? Жизненный цикл:
- •3. Является ли данное заболевание природно-очаговым?
- •4.Почему термич. Обработка мяса не предотвратила инвазию?
- •5.Какие основные меры профилактики против заражения данным паразитом?
- •3.) Во время медосмотра у пациента был обнаружен шейный свищ.
- •4) Всуд поступило заявление о взыскании алиментов с предполагаемого отца. Мать и ребёнок имеют 1-ю группу крови, а отец 4-ю. Какое заключение даст судебная экспертиза?
- •1. Какие органы в эмбриогенезе позвоночных обеспечивают жизненно важные ф-ции?
- •2. Что лежит в основе деления позв. На 2-е группы: Анамнии и Амниоты, Представители?
- •3. Зародышевые оболочки плацентарных млекопит. И человека. Функции?
- •4. Какие функции выполняет плацента? Чем образована материнская и зародышевая часть плаценты?
- •5. Типы плацент? Какой тип у человека?
- •3) В процессе развития висцерального черепа человека можно проследить повторение этапов филогенетических преобразований висцеральных дуг в ряду челюстноротых.
- •4). Практический навык
- •1. В процессе ряда последовательных митотических делений зиготы образуется многоклеточный организм.
- •2. В мазке из выделений мочепол. Путей мужчины были обнаружены одноклет. Паразиты грушевидной ф-мы с 4-мя жгутиками, ундулирующей мембраной и опорным стержнем- аксостилем.
- •5. Укажите меры общественной и личной профилактики.
- •5. Объясните происхождение онто-филогенетических пороков зубной системы человека: сверхкомплектные зубы, тремы, диастемы, конические зубы, сильное развитие клыков.
- •4. Составить и проанализировать родословную. Генотип пробанда, его сына и дочери?
- •Билет26
- •1)В основе дробления зародыша лежит деление клеток митозом, приводящее к увеличению количества клеток. Однако, в объеме зародыш не увеличивается.
- •3) Гипоплазия эмали (тонкая зернистая эмаль, зубы светло-бурого цвета) наследуется как сцепленный с х-хромосомой доминантный признак.
- •4) Фасциолез (фасциола обыкновенная)
- •Экзаменационное задание №28
- •I ситуационные задачи
- •I I . Проверка проктических навыков.
- •Экзаменационное задание №29
- •I ситуационные задачи
- •I I . Проверка проктических навыков.
- •Билет 38
- •Билет№30
- •Билет№31
- •1.Каков хар-р прикрепления челюстного аппарата к мозговому черепу у млекопитающих и человека?
- •Кзаменационное задание №37
- •1.Перечислите основные элементы челюстной и подъязычных дуг.
- •2.Чем характеризуется каждый тип сочленения?
- •3.Для каких классов позвоночных характерны данные типы сочленения. С какими эволюционными событиями связан переход от одного типа сочленения к другому?
- •4.В состав каких структур включаются элементы челюстной и подъязычной висцеральных дуг?
- •5.Назовите онто-филогенетически обусловленные пороки развития у человека, связанные с эволюционными преобразованиями висцеральных дуг.
- •II. Практические навыки.
- •Билет № 39
- •Билет № 41
- •Часть 2
- •Билет 40
- •Часть 2
- •I. Молекула днк, явл. Носителем наследственной информации, кот. Реализуется в процессе синтеза белка.
- •Какова молекулярная структура днк?
- •Что такое генетический код, свойства ген.Кода?
- •3. Процессы в период транскрипции (кратко)?
- •4. Процессинг (посттранскрипция)?
- •5. Трансляция?
- •II. При раскопках в Южн. Африке были обнаружены костные останки древних гоминид. Возраст 2,8-1,5 млн. Лет, прямоходящие, объем мозга 700 см3.
- •5. Как происходит эволюция чел на 1-м этапе антропогенеза?
- •III. В стомат. Клинику обрат пац. Со сверхкомплектными зубами
- •1.Основные направления эволюции зубов у позвоночных?
- •2.Что такое полифиодонтизм и дифиодонтизм?
- •Билет № 45
- •3. Гипоплазия эмали наследуется, как сцепленный с х-хромосомой доминантный признак.
- •2) Какой закон отражает связь индивидуального и исторического развития организма?
- •3) Основные эволюционные преобразования зубочелюстной системы позвоночных?
- •4) Гомологами каких структур низших позвоночных явл. Зубы?
- •5) Эвол. Преобразования зубочелюстной сист. Человека?
- •1. У здоровых родителей родился сын с тяжелыми наследственными заболеваниями миодистрофия Дюшена (рецессивный сцепленный с х-хромосомой признак)
- •1. Причина рождения больного ребенка?
- •2.Какой вид изменчивости проявился в этом случае? Возможные мех-мы возникновения такой изменчивости?
- •3. В практике стоматолога встречаются пороки зубочелюстной системы (Сверхкомплектные зубы, диастемы, конические зубы)
- •2) Какой закон отражает связь индивидуального и исторического развития организма?
- •3) Основные эволюционные преобразования зубочелюстной системы позвоночных?
- •4) Гомологами каких структур низших позвоночных явл. Зубы?
- •5) Эвол. Преобразования зубочелюстной сист. Человека?
- •4. Таежный клещ
- •Билет № 48
- •Экзаменационное задание № 49
- •1. Назовите стадии гаметогенеза и дайте их характеристику.
- •2. На какой стадии происходит редукция числа хромосом?
- •3. Какаие процессы в гаметогенезе обуславливают генетическое разнообразие гамет?
- •4. Назовите отличительные особенности овогенеза и сперматогенеза у человека.
- •5. Укажите возможные механизмы нарушения числа хромосом в половых клетках. К чему приводят эти нарушения?
- •1. Какие области значений экологического фактора называют биоинтервалом или диапазоном выживания?
- •2. В чем сущность понятий экологического оптиума, зон адаптаций, пределов выносливости, биологической нормы, зон летальности?
- •3. Что такое экологическая пластичность организмов, какие виды организмов различают по отношению к ней?
- •4. Какой экологический фактор называют лимитирующим? Представления к. Либиха, закон биологичской стойкости в. Шелфорда и ю. Одума.
- •5. Какова экологическая пластичность человека как индивидуума и как представителя социума?
- •1. Что такое сцепленное с полом наследование? Объясните сцепленное с х-хромосомой наследование.
- •2. Назовите другие типы наследования. Чем они характеризуются?
- •Экзаменационное задание №50
- •1. Перечислите основные механизмы онтогенеза.
- •2. Какие клеточные процессы лежат в основе роста и морфогенеза?
- •3. Что такое дифференцировка клеток, ее цитогенетические основы?
- •4. В чем заключено явление эмбриональной индукции?
- •5. Приведите примеры индукционных изменений.
- •1. Инвазию каким паразитом можно предположить?
- •1.Каков хар-р прикрепления челюстного аппарата к мозговому черепу у млекопитающих и человека?
Билет № 41
Каким образом могут делиться соматические клетки?
Соматические клетки (др.-греч. σῶμα — тело) — клетки, формирующие тело организма. К соматическим клеткам относятся все клетки тела, за исключением гамет.
Мито́з (греч. μιτος — нить) — непрямое деление клетки, кариокинез, наиболее распространенный способ репродукции эукариотических клеток. Биологическое значение митоза состоит в строго одинаковом распределении хромосом между дочерними ядрами, что обеспечивает образование генетически идентичных дочерних клеток и сохраняет преемственность в ряду клеточных поколений.
Митоз — один из фундаментальных процессов онтогенеза. Митотическое деление обеспечивает рост многоклеточных эукариот за счёт увеличения популяции тканевых клеток. В результате митотического деления клеток меристем увеличиваются тканевые популяции растительных клеток. Дробление оплодотворённого яйца и рост большинства тканей у животных также происходит путём митотических делений.[2]
На
основании морфологических особенностей
митоз условно подразделяется на стадии:
профазу
![]() ,
прометафазу
,
прометафазу
![]() ,
метафазу
,
метафазу
![]() ,
анафазу, телофазу. Первые описания
митотических фаз и установление их
последовательности были предприняты
в 70—80-х годах XIX
века.
В конце 1870-х —
начале 1880-х
годов немецкий гистолог Вальтер
Флемминг
для обозначения процесса непрямого
деления клетки ввёл термин «митоз».
,
анафазу, телофазу. Первые описания
митотических фаз и установление их
последовательности были предприняты
в 70—80-х годах XIX
века.
В конце 1870-х —
начале 1880-х
годов немецкий гистолог Вальтер
Флемминг
для обозначения процесса непрямого
деления клетки ввёл термин «митоз».
Продолжительность митоза в среднем составляет 1—2 часа. В клетках животных митоз, как правило, длится 30—60 минут, а в растительных — 2—3 часа. Клетки человека за 70 лет суммарно претерпевают порядка 1014 клеточных делений.
Охарактеризуйте типы тканей по характеру пролиферативной активности? Быстро обновл, медленно обновл, стабильные, растущие
Какие периоды включает митотический цикл клетки? Назовите процессы, происходящие в каждом периоде.
Одним из основных свойств живой клетки является ее способность к делению. В настоящее время остается неясным, что ограничивает этот процесс и почему во многих органах, когда они достигают в процессе развития определенного объема, процесс деления прекращается. Неясно также, за счет чего деление клеток возобновляется, например, в фазе регенерации после резекции части печени. Многие гормоны вместе с тем являются стимуляторами митотического цикла клетки.
В течение митотического цикла клетка проходит ряд фаз, в которых чувствительность к различным воздействиям значительно меняется. Клеточный цикл в соответствии с современной моделью делится на следующих четыре периода: период митоза или фаза «М»; период «S» (период синтеза), в котором происходит синтез ДНК, РНК и белка; период G1 (от «gap»-интервал) между М и S, или период покоя клетки, и период G2 между S и М (премитотический период).
Продолжительность фазы S обычно составляет около 6-8 часов. Те воздействия, которые обладают способностью вмешиваться в синтез ДНК, оказывают повреждающее действие в этот период. В конечном итоге митоз может не наступить или могут возникнуть генетические дефекты, нарушающие жизнеспособность клетки.
Продолжительность фазы G2 в среднем 0,5-1,5 часа. Синтез РНК и белка продолжается в этой фазе, что, как видно, необходимо для обеспечения клетки энергией во время митоза. Длительность митоза (фаза М) определяется для тканей млекопитающих в пределах 0,5-2,5 часа. В течение фазы М синтез белка находится на низком уровне, а синтез РНК ограничен ранней профазой и поздней гелофазой. Фаза G1 является главной переменной в длительности клеточного цикла.
В дальнейшем был выделен дополнительно период, характеризующий выход из митотического цикла — G0. Так, «дремлющие» опухолевые клетки, не претерпевающие митозов, нередко в течение многих лет находятся в фазе G0, будучи рефрактерными ко многим воздействиям. Но затем они могут вновь включиться в митотический цикл. Поэтому отношение числа пролиферирующих клеток к общему числу клеток популяции получило наименование пролиферативного пула.
Механизм, который переключает клетки на путь синтеза ДНК и митоза, во многих отношениях остается неясным. Однако многие гормоны играют в этом механизме существенную роль. Хотя механизм, поддерживающий постоянный размер популяции нормальных клеток, невыяснен, имеется ряд доказательств, что этот эффект в значительной степени достигается за счет действия так называемых келонов. Если концентрация келонов уменьшается, то митотическая активность возрастает, и, наоборот, показано, что активность келонов некоторых тканей усиливается гормонами, например адреналином.
В этом отношении представляет интерес, что концентрация адреналина уменьшается во время сна, тогда как количество митозов в этот период возрастает.
Секреция гормона роста, напротив, увеличивается в ночные часы, причем существует «ночной пик» его концентрации в крови. Возможно, увеличение концентрации гормона роста в ночные часы имеет отношение к механизму стимуляции митозов.
Суточный ритм секреции глюкокортикоидов также, вероятно, имеет отношение к митотической активности, что несомненно, по крайней мере, для лимфоидной ткани. Наконец, большая группа гормонов — ФСГ, АКТГ, меланотропин, пролактин, тиреотропин, эстрогены, андрогены, эритропоэтин — обладает способностью стимулировать митозы в специализированных тканях-мишенях.
Очень важно отметить, что в доброкачественных опухолях, по крайней мере, в некоторых из них, сохраняется циркадный (суточный) митотический ритм. Поэтому было высказано предположение, что уменьшение концентрации келонов или снижение чувствительности клеток к их ингибирующему действию происходит при прогрессии опухоли.
Вместе с тем и некоторые злокачественные опухоли сохраняют чувствительность как к митотическому, так и антимитотическому действию тропных гормонов, что имеет много примеров, относящихся, в частности, к раку молочной железы, эндометрия и щитовидной железы.
Существуют также данные и о других факторах, определяющих митотическую активность, причем гормоны, как видно, участвуют в механизмах регуляции и этих систем поддержания размеров нормальной клеточной популяции. Одной из кардинальных систем ограничения клеточной популяции является контактное торможение клеток, происходящее на уровне клеточных мембран.
Существенное значение в осуществлении контактного торможения имеет концентрация в клеточных (плазматических) мембранах кислых мукополисахаридов, сиаловой кислоты, холестерина, определяющих физико-химический ионный эффект на поверхности клеток, а также уровень цАМФ, цГМФ и кальция.
Так как действие большинства гормонов также осуществляется на уровне клеточных мембран, то нельзя исключить, что некоторые гормоны могут существенно изменять их ионный потенциал, в частности путем регуляции утилизации глюкозы.
Активность лизосомального аппарата также принимает участие в регуляции размеров клеточной популяции, энзиматически разрушая клетки собственной популяции. Роль глюкокортикоидов, которые ингибируют активирующее действие некоторых веществ на лизосомы, например витамина А, хорошо известна. Предполагается, что стимуляция пролиферации в специфических тканях под влиянием эстрогенов и андрогенов также регулируется путем освобождения гидролаз из лизосом.
В опухолевой ткани различные факторы, влияющие на скорость гибели клеток, играют очень существенную роль, в конечном итоге определяя реальную скорость роста опухоли. Так, в частности, показано, что клетки лимфомы Бэркита имеют потенциальное время удвоения (т. е. время удвоения при отсутствии потери клеток), равное 24-48 часам, тогда как удвоение объема опухоли происходит за несколько недель.
Среди ряда факторов, вызывающих гибель клеток, определенное значение имеют и взаимоотношения между опухолью и организмом-хозяином, в значительных пределах регулируемые гормонами. Так, например, при избытке в организме глюкокортикоидов создаются условия для пролиферации опухолевых клеток. Этот эффект обеспечивается различными влияниями, в частности, за счет иммунодепрессивного действия глюкокортикоидов с усилением лизиса лимфоцитов, что приводит к увеличеню пула глюкогенных аминокислот и тем самым возникновению относительной гипергликемии.
Что такое жизненный цикл клеток?
Клеточный цикл — это период существования клетки от момента её образования путем деления материнской клетки до собственного деления.
Длительность клеточного цикла у разных клеток варьируется. Быстро размножающиеся клетки взрослых организмов, такие как кроветворные или базальные клетки эпидермиса и тонкой кишки, могут входить в клеточный цикл каждые 12—36 ч. Короткие клеточные циклы (около 30 мин) наблюдаются при быстром дроблении яиц иглокожих, земноводных и других животных. В экспериментальных условиях короткий клеточный цикл (около 20 ч) имеют многие линии клеточных культур. У большинства активно делящихся клеток длительность периода между митозами составляет примерно 10—24 ч.
Фазы клеточного цикла эукариот
Клеточный цикл эукариотсостоит из двух периодов:
Период клеточного роста, называемый «интерфаза», во время которого идет синтез ДНКибелкови осуществляется подготовка к делению клетки.
Периода клеточного деления, называемый «фаза М» (от слова mitosis — митоз).
Интерфаза состоит из нескольких периодов:
G1-фазы (от англ.gap — промежуток), или фазы начального роста, во время которой идет синтез мРНК,белков, других клеточных компонентов;
S-фазы (от англ.synthesis — синтетическая), во время которой идет репликация ДНКклеточного ядра, также происходит удвоениецентриолей(если они, конечно, есть).
G2-фазы, во время которой идет подготовка к митозу.
У дифференцировавшихся клеток, которые более не делятся, в клеточном цикле может отсутствовать G1 фаза. Такие клетки находятся в фазе покоя G0.
Период клеточного деления(фаза М) включает две стадии:
кариокинез(деление клеточного ядра);
цитокинез(деление цитоплазмы).
В свою очередь, митозделится на пять стадий,in vivo эти шесть стадий образуют динамическую последовательность.
Описание клеточного деления базируется на данных световой микроскопии в сочетании с микрокиносъемкой и на результатах световойиэлектронноймикроскопиификсированных и окрашенных клеток.
Регуляция клеточного цикла
Закономерная последовательность смены периодов клеточного цикла осуществляется при взаимодействии таких белков, какциклин-зависимые киназыициклины.Клетки, находящиеся в G0 фазе, могут вступать в клеточный цикл при действии на них факторов роста. Разные факторы роста, такие кактромбоцитарный, эпидермальный, фактор роста нервов, связываясь со своимирецепторами, запускают внутриклеточный сигнальный каскад, приводящий в итоге ктранскрипциигеновциклиновициклин-зависимых киназ.Циклин-зависимые киназыстановятся активными лишь при взаимодействии с соответствующимициклинами. Содержание различныхциклиноввклеткеменяется на протяжении всего клеточного цикла.Циклинявляется регуляторной компонентой комплекса циклин-циклин-зависимая киназа.Киназаже является каталитическим компонентом этого комплекса.Киназыне активны безциклинов. На разных стадиях клеточного цикласинтезируютсяразныециклины. Так, содержаниециклинаB вооцитахлягушкидостигает максимума к моментумитоза, когда запускается весь каскад реакцийфосфорилирования, катализируемых комплексом циклин-В/циклин-зависимая киназа. К окончанию митоза циклин быстро разрушается протеиназами.
Контрольные точки клеточного цикла
Для определения завершения каждой фазы клеточного цикла необходимо наличие в нем контрольных точек. Если клетка «проходит» контрольную точку, то она продолжается «двигаться» по клеточному циклу. Если же какие-либо обстоятельства, например повреждение ДНК, мешают клетке пройти через контрольную точку, которую можно сравнить со своего рода контрольным пунктом, то клетка останавливается и другой фазы клеточного цикла не наступает по крайней мере до тех пор, пока не будут устранены препятствия, не позволявшие клетке пройти через контрольный пункт. Существует как минимум четыре контрольных точки клеточного цикла: точка в G1, где проверяется интактность ДНК, перед вхождением в S-фазу, сверочная точка в S-фазе, в которой проверяется правильность репликации ДНК, сверочная точка в G2, в которой проверяются повреждения, пропущенные при прохождении предыдущих сверочных точек, либо полученные на последующих стадиях клеточного цикла. В G2 фазе детектируется полнота репликации ДНК и клетки, в которых ДНК недореплицирована, не входят в митоз. В контрольной точке сборки веретена деления проверяется, все ли кинетохоры прикреплены к микротрубочкам.
Нарушения клеточного цикла и образование опухолей
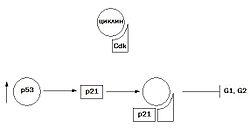
![]()
Увеличение синтеза белка p53 ведет к индукции синтеза белка p21 — ингибитора клеточного цикла
Нарушение нормальной регуляции клеточного цикла является причиной появления большинства твердых опухолей. В клеточном цикле, как уже говорилось, прохождение контрольных пунктов его возможно только в случае нормального завершения предыдущих этапов и отсутствия поломок. Для опухолевых клеток характерны изменения компонентов сверочных точек клеточного цикла. При инактивации сверочных точек клеточного цикла наблюдается дисфункция некоторых опухолевых супрессоров и протоонкогенов, в частности p53, pRb, Myc и Ras. Белок p53 является одним из факторов транскрипции, который инициирует синтез белка p21, являющегося ингибитором комплекса CDK-циклин, что приводит к остановке клеточного цикла в G1 и G2 периоде. Таким образом клетка, у которой повреждена ДНК, не вступает в S-фазу. При мутациях, приводящих к потере генов белка p53, или при их изменениях, блокады клеточного цикла не происходит, клетки вступают в митоз, что приводит к появлению мутантных клеток, большая часть из которых нежизнеспособна, другая — дает начало злокачественным клеткам.
Приведите примеры жизненных циклов клеток, относящихся к равным по характеру пролиферативной активности типам тканей.
