
- •А.М.Даниленко
- •Глава 2. Химическая термодинамика.
- •Внешняя среда
- •I закон термодинамики.
- •Глава 3. Химическая кинетика и равновесие.
- •Глава 4. Растворы
- •Поскольку растворение - процесс самопроизвольный, то
- •Глава 5. Электрохимия.
- •Возникновение скачка потенциала на границе металл - раствор электролита.
- •Активный металл Пассивный металл
- •Глава 6. Дисперсные системы
- •Классификация диперсных систем
- •Методы получения дисперсных систем.
- •Строение частиц лиофобных золей.
- •Глава 7. Жесткость природных вод.
- •Методы осаждения Методы ионного обмена
- •Метод методы
- •Метод известкования Содово-известковый метод
Методы осаждения Методы ионного обмена

Термический Реагентные
Метод методы
Метод известкования Содово-известковый метод
Термический метод.
Предусматривает нагревание воды до 95-98 0С. Карбонатную жесткость легче устранить при умягчении воды. Гидрокарбонат кальция существует только в водных растворах и обладает малой термической устойчивостью. Равновесие, устанавливающееся в воде выражается уравнением:
Ca(HCO3)2 CaCO3+ CO2+ H2O
При повышении температуры растворимость углекислого газа в воде значительно уменьшается, равновесие реакции смещается вправо и CaCO 3 выпадает в осадок. Магний при нагревании воды осаждается в виде гидроксида или основного карбоната (вследствие гидролиза):
Mg(HCO3)2 = MgCO3 + CO2 + H2O
2MgCO3 + 2H2O = (MgOH)2CO3 + CO2 + H2O
MgCO3+ 2H2O = Mg(OH)2 + CO2 + H2O
Таким образом, при кипячении воды жесткость, вызываемая присутствием гидрокарбонатов кальция и магния, устраняется и поэтому называется временной – Жв. Некарбонатная жесткость не устраняется при кипячении, поэтому ее еще называют постоянной жесткостью – Жп. Нетрудно видеть, что
Жо = Жв + Жп
Так как нагрев воды требует больших затрат энергии, то этот метод применим только в тех случаях, когда вода должна нагреваться по условиям своего применения.
Реагентные методы.
Связаны с удалением ионов кальция и магния в результате образования малорастворимых соединений под действием химических реагентов. Кальций при этом удаляется в виде карбоната, а магний в виде гидроксида. Выделяются следующие разновидности реагентных методов:
1. Метод известкования – обработка воды гидроксидом кальция – Са(ОН)2. В результате протекают следующие реакции:
Ca(HCO3)2 + Са(ОН)2 = 2CaCO3 + 2H2O
Mg(HCO3)2 + 2Са(ОН)2 = Mg(OH)2 + 2CaCO3 + 2H2O
При этом также происходит удаление растворенного СО2:
СО2 + Са(ОН)2 = CaCO3 + H2O
Метод известкования применим только для воды с очень большой карбонатной жесткостью. При известковании в воду дополнительно вводятся ионы кальция, поэтому применение избытка Са(ОН)2 недопустимо. Количество вводимой извести должно соответствовать предварительно определенному содержанию гидрокарбонатов кальция и магния. Методом известкования также не не удаляется постоянная (некарбонатная) жесткость.
2. Содово–известковый метод – обработка воды смесью Са(ОН)2 и Na2CO3. Применяется для одновременного удаления карбонатной и некарбонатной жесткости. Карбонатная жесткость удаляется известью, как показано выше, а некарбонатная удаляется содой:
CaSO4 + Na2CO3 = CaCO3 + Na2SO4
CaCl2 + Na2CO3 = CaCO3+ NaCl
Образующийся по аналогичным реакциям карбонат магния реагирует с известью:
MgCO3+ Ca(OH)2 = Mg(OH)2 + CaCO3
Количество остающейся жесткости составляет всего 0,3 ммоль-экв/л. Еще лучшие результаты дает сочетание содово-известкового и термического методов. Такой метод применяют для умягчения воды, используемой в котлах низкого давления (до 15 атм).
Методы ионного обмена.
Применяют для умягчения воды или ее полного обессоливания. Твердые материалы, способные к ионному обмену с окружающей средой, получили название ионитов . Сюда относятся различные вещества природного и синтетического происхождения. В настоящее время наибольшее значение приобрели различные ионообменные смолы, вырабатываемые на основе синтетических полимеров. Иониты представляют собой твердые электролиты, у которых один поливалентный ион является нерастворимым, а ионы противоположного знака способны к обмену на ионы, находящиеся в окружающем растворе. В зависимости от того, какие ионы в этих смолах обмениваются - катионы или анионы,- различают
катиониты
–
![]() (Х = Н+
или Na+)
(Х = Н+
или Na+)
аниониты
–
![]() (Y
= OH–)
(Y
= OH–)
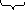
поливалентный обменивающиеся
нерастворимый ион ионы
По виду обмениваемых ионов катиониты подразделяются на Na-катиониты (используются для умягчения воды) и Н-катиониты (используются при обессоливании). Основной характеристикой ионитов является величина обменной емкости - количество ммоль-экв/л ионов, поглощенных определенным объемом набухшего ионита.
Сущность работы Na-катионита состоит в том, что при пропускании воды через колонну, заполненную катионитом (зерна 0,2-3 мм), протекают реакции, в ходе которых удаляется и временная и постоянная жесткости:
![]() +
+![]() Ca(HCO3)2
=
Ca(HCO3)2
=
![]() +nNaHCO3
+nNaHCO3
![]() +
+![]() Mg(HCO3)2=
Mg(HCO3)2=
![]() +nNaHCO3
+nNaHCO3
![]() +
+
![]() CaCl2
=
CaCl2
=
![]() + nNaCl
+ nNaCl
Для регенерации катионита, т.е. восстановления его работоспособности, через ту же колонну пропускают 5-10% раствор NaCl, что приводит к образованию хорошо растворимых хлоридов кальция и магния и удалению их их катионита:
![]() +
nNaCl
=
+
nNaCl
=
![]() +
+
![]() CaCl2
CaCl2
![]() +
nNaCl =
+
nNaCl =
![]() +
+
![]() MgCl2
MgCl2
Н–катиониты работают по аналогичным реакциям с образованием соответствующих кислот (H2CO3, HCl, H2SO4). Для удаления образовавшейся кислоты необходимо пропустить раствор через анионит:
![]() +
+
![]() H2SO4
=
H2SO4
=
![]() +mH2O
+mH2O
Пропуская воду последовательно через Н-катионит и анионит, можно полностью удалить из нее все содержащиеся электролиты.
Регенерацию анионита осуществляют пропусканием раствора едкого натра:
![]() +
mNaOH
=
+
mNaOH
=
![]() +
+
![]() Na2SO4
Na2SO4
Кроме перечисленных методов в практике водоподготовки начинают использовать магнитные, ультразвуковые, электрохимические методы. Воду специального технологического назначения очищают от соединений железа, марганца, кремния, растворенного воздуха и др. Вода для питьевых нужд очищается от взвесей коагуляцией и обеззараживанию при помощи хлора, хлорной извести или озонированием.
Пример 6.1. К 200 л воды с Ж0в = 2,8 ммоль-экв/л добавили 150 л воды с Ж0п = 3 ммоль-экв/л. Определите Жк, Жп, Жо после смешения?
Решение.
1. nэк(врем.) = Ж0в•V1/1000 = 2,8•200/1000 = 0,56 моль-экв.
2. nэк(пост.) = Ж0п•V2/1000 = 3•150/1000 = 0,45 моль-экв
3. После смешения V(р–ра) = V1 + V2 = 150 + 200 = 350 л.
4. Жв = 1000 • nэк(врем.)/V(р–ра) = 1000•0,56/350 =
= 1,6 ммоль-экв.
5. Жп = 1000 • nэк(пост.)/V(р–ра) = 1000•0,45/350 =
= 1,3 ммоль-экв.
6. Жо = Жв + Жп = 1,6 + 1,3 = 2,9 ммоль-экв.
Пример 6.2. Жп = 6 ммоль-экв/л обусловлена содержанием CaCl2. Сколько г К2CO3 требуется для полного умягчения 100 л воды?
Решение.
Расчет количества реагента (К2CO3), требующегося для удаления ионов жесткости осуществляют на основе закона эквивалентов:
![]() =
=
nЭК
(К2CO3).
Отсюда
=
=
nЭК
(К2CO3).
Отсюда
m
(К2CO3)
![]() =
40,8 г.
=
40,8 г.
.
