- •Предисловие
- •Введение
- •1. Хроматографические методы
- •1.1. Характеристики хроматографического разделения компонентов анализируемой смеси
- •Изотермы адсорбции
- •Изотермы адсорбции и форма фронтов зон
- •1.3 Теория теоретических тарелок
- •6.2. Оценка параметров эффективности и селективности хроматографической колонки
- •6.5. Степень разделения и ее связь с параметрами
- •Влияние условий анализа на эффективность разделения
- •7.3. Влияние скорости потока газа-носителя на эффективность капиллярных колонок
- •8. Влияние температуры на параметры процесса разделения
- •1.5. Газовая хроматография
- •3.2. Газовый хроматограф. Принципиальная схема
- •Устройства ввода пробы в хроматограф
- •Ввод пробы
- •9.2. Чувствительность детектора. Предел обнаружения
- •9.3. Линейность детектора
- •9.4. Селективность детектора
- •1.3.5.1. Детекторы по теплопроводности
- •1.3.5.3. Пламенно-ионизационный детектор
- •Значения инкрементов функциональных групп и связей
- •Величины относительных молярных поправочных коэффициентов
- •1.3.5.4. Детектор электронного захвата
- •1.3.5.5. Детектор ионизационно-резонансный
- •1.5.5.6. Термоионный детектор
- •1.3.5.9.Фотоионизационный детектор (дфи)
- •3.1. Варианты метода газовой хроматографии
- •Силы дисперсионного взаимодействия
- •Силы индукционного взаимодействия
- •Силы ориентационного взаимодействия
- •Силы полухимического и химического взаимодействий
- •12.2. Классификация разделяемых соединений по их способности к различным типам межмолекулярных взаимодействий
- •Классификация адсорбентов по способности к различным типам межмолекулярных взаимодействий
- •Классификация адсорбентов по особенностям внутренней геометрической структуры
- •12.4. Важнейшие адсорбенты и характеристика их свойств
- •Углеродные адсорбенты
- •Адсорбенты с большим содержанием кремниевой кислоты
- •Оксид алюминия
- •Органические сорбенты
- •12.5. Приложение теории адсорбции к газовой хроматографии
- •12.6. Основные преимущества и недостатки газо-адсорбционной хроматографии
- •13.2. Классификация основных носителей неподвижных жидких фаз Диатомовые носители
- •Стеклянные микрошарики
- •Силикагель
- •Оксид алюминия
- •Политетрафторэтилен
- •13.3. Неподвижные жидкие фазы
- •Химическая активность
- •Давление паров и термостойкость
- •Размеры молекул
- •Вязкость
- •Способность к растворению разделяемых соединений
- •Разделительные свойства
- •13.4. Классификация неподвижных жидких фаз
- •Шкала относительной полярности неподвижных жидких фаз
- •Классификация неподвижных жидких фаз по индексам удерживания Ковача
- •Классификация неподвижных жидких фаз по веществам-стандартам
- •Классификация неподвижных жидких фаз Мак-Рейнольдса
- •13.5. Важнейшие неподвижные жидкие фазы
- •Неароматические углеводороды
- •Ароматические углеводороды
- •Силиконы
- •Фенилсиликоны
- •Спирты, эфиры и производные углеводов
- •Полигликоли
- •Ароматические простые эфиры
- •Сложные эфиры
- •7.2. Влияние количества неподвижной жидкой фазы на свойства насадки
- •7.4. Влияние толщины пленки неподвижной жидкой фазы на эффективность капиллярной колонки
- •4.4. Основные преимущества и недостатки газо-жидкостной хроматографии
- •3. Жидкостная хроматография
- •Основное оборудование для тсх
- •Техника эксперимента в тсх
- •Сверхкритическая флюидная хроматография
- •Критические величины для подвижных фаз в сфх
- •2. Свойства сверхкритических флюидов, используемые
- •4. Приборное оформление
- •5. Современные задачи сфх с насадочными колонками
- •6. Заключение
- •6. Капиллярный электрофорез Введение
- •Принятые термины и сокращения
- •Физико-химические основы метода капиллярного электрофореза
- •Основные варианты капиллярного электрофореза
- •Аппаратура Общее устройство систем кэ
- •Капилляры
- •Источники высокого напряжения
- •Ввод пробы
- •Детекторы
- •Системы термостабилизации. Сбор и обработка данных
- •Эффективность разделения
- •Чувствительность метода
- •Разрешение и селективность разделения
- •Обработка результатов в капиллярном электрофорезе. Качественный и количественный анализ
- •Количественная обработка результатов анализа
- •Объекты для анализа методом кэ. Подготовка пробы
- •Электрофореза и примеры использования Анализ объектов окружающей среды.
- •Анализ неорганических анионов с обращением эоп (рис. 9)
- •Анализ неорганических анионов без обращения эоп (рис. 9)
- •Анализ неорганических катионов в яблочном соке (рис. 9)
- •Анализ ионного состава воды. Определение неорганических
- •Особенности методики, практические рекомендации
- •В присутствии (а) и в отсутствие (б) Br в составе ведущего электролита.
- •1.9. Качественный хроматографический анализ
- •5. Количественный анализ
- •11.1. Параметры пика как характеристика количества вещества
- •Параметр h
- •Параметр hl
- •Параметр а
- •Величины допустимых погрешностей задания параметров разделения
- •5.3.1 Методы триангуляции
- •7. Практическое использование хроматографии в контроле качества продукции
1. Хроматографические методы
Абсолютое большинство веществ живой и неживой природы и синтетических веществ, используемых в производстве самых разнообразных продуктов питания и непродовольственных товаров, представляют собой не индивидуальные химические соединения, а сложные многокомпонентные смеси веществ. В процессе получения готовой продукции чаще всего состав исходного сырья изменяется: в результате технологических воздействий некоторые компоненты частично или полностью исчезают, появляются новые вещества.
Должное
качество продукции достигается, как
правило, при достаточно строгом
компонентном составе получаемой
продукции. К сожалению, большинство
современных физических и физико-химических
методов анализа, используемых для
контроля компонентного состава вещества,
дает аддитивную величину измеряемого
аналитического сигнала, которая слагается
из его величин, образуемых отдельными
компонентами смеси, зачастую имеющими
различную химическую природу и различное
влияние на качество продукции.Это
ограничивает использование таких
методов для строгого контроля компонентного
состава продукции и приводит к
необходимости использовать те или иные
методы разделения смесей веществ.
Особенно большие трудности возникают, если все компоненты разделяемой смеси образуют одну фазу. В этом случае необходимо или изменять агрегатное состояние части компонентов смеси, или добиваться изменения фазового равновесия или кинетики процесса разделения. Например, в таких методах разделения, как экстракция и ректификация, вещества, входящие в смесь, переходят через границу раздела фаз в обоих направлениях, стремясь к установлению равновесия. Эффективность разделения значительно повышается, если процесс перехода вещества из одной фазы в другую с установлением равновесия многократно повторяется.
Цвет М.С. (1872-1919 г.г.)
Еще более эффективно смеси веществ разделяются, если разделение смеси производить так, чтобы одна из фаз была подвижной и перемещалась отностельно другой – неподвижной. В этом случае, как и при установлении фазового равновесия, молекулы веществ, входящих в смесь, на выходе из неподвижной фазы возвращаются в нее, однако вследствие движения подвижной фазы попадают не в прежний участок объема неподвижной фазы, а в новый, ближайший по направлению движения подвижной фазы, объем. Многократное повторение элементарных актов фазовых переходов, большая поверхность раздела фаз и относительно малая толщина взаимодействующих слоев фаз обеспечивает высокую эффективность разделения многокомпонентных смесей веществ, часто обладающих близкими свойствами.
Эти условия в большей мере выполняются в методе разделения смеси веществ, получившего название хроматографического и в настоящее время широко используемого на практике не только в качестве метода разделения, но и метода анализа сложных многокомпонентных смесей веществ.
Основы хроматографического метода были сформулированы в 1903 году ботаником М. . Цветом. Разработанный метод предназначалcя для разделения окрашенных биохимических объектов. Первые опыты по хроматографии, проведенные М. Цветом на смесях растительных пигментовхлорофиллинов и ксантофиллинов, состояли в использовании стеклянных колонок, заполненных мелом. При вымывании пигментов петролейным эфиром они перемещались вдоль колонки, разделяясь при этом на кольца разного цвета. Результаты этих экспериментов были опубликованы М. Цветом в статье «О новой категории адсорбционных явлений и о применении их к биохимическому анализу».
Характеризуя
принципы предложенного им метода,
М. Цвет писал: «При
фильтрации смешанного раствора через
столб адсорбента пигменты расслаиваются
в виде отдельных различно окрашенных
зон. Подобно световым лучам в спектре,
различные компоненты сложного пигмента
закономерно распределяются друг за
другом в столбе адсорбента и становятся
доступными качественному определению.
Такой расцвеченный препарат я назвал
хроматограммой, а соответствующий метод
анализахроматографическим методом».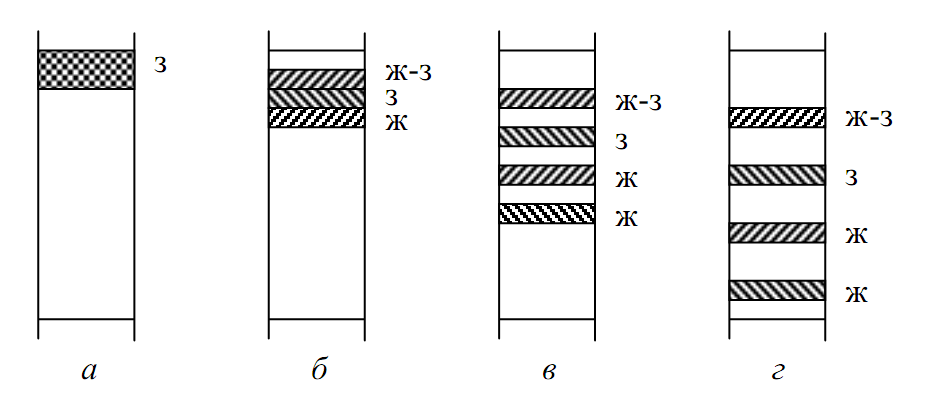
В этой формулировке М. Цвет дал достаточно четкое определение адсорбционной хроматографии, основанной на различии компонентов анализируемой смеси по сродству к выбранному адсорбенту. Он высказал идею о возможности применения для хроматографического разделения смеси веществ различий и в других свойствах компонентов, в частности в растворимости труднорастворимых осадков. Однако предложенный М. Цветом метод его современниками не был оценен и длительное время не находил использования.
Расцвет
и бурное развитие хроматографии начались
с 1931 г., когда уже были разработаны основы
теории адсорбции и ионного обмена и
синтезированы новые неорганические и
органические сорбенты. Развитие
хроматографии связано с именами Р. Куна,
Е. Ледерера, А. Винтерштейна,
А. Измайлова. Усилиями этих и многих
других ученых были разработаны
разнообразные варианты хроматографического
анализа: тонкослойная (1938 г., Н. Измайлов),
бумажная (1941 г., А. Мартин, Р. Синдж),
газоадсорбционная (1940), газожидкостная
(1952 г., А. Мартин), капиллярная (1957 г.,
М. Голей), высокоэффективная жидкостная
(60-е г. XIXв.), эксклюзионная
(60-е г.XIXв.), ионная
хроматография (1970 г., Х. Смолл,
Т. Стивенс).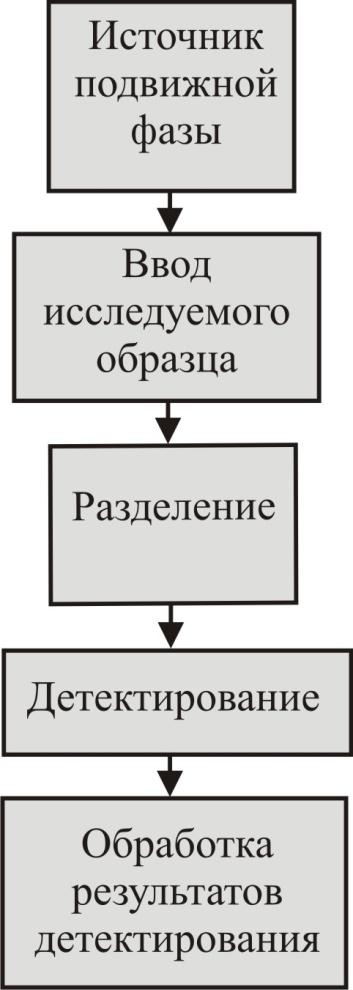
Однако любые варианты хроматографии, как бы далеки друг от друга они не были по внешним признакам, основываются на одном общем принципе, состоящем в распределении компонентов разделяемой смеси между двумя фазами, одна из которых неподвижна и имеет развитую поверхность, а вторая – подвижная – представляет собой поток, проходящий через слой неподвижной фазы.
Неподвижной (стационарной) фазой служит твердое вещество (сорбент), пленка жидкости, нанесенная на твердое вещество (носитель), гелеобразное вещество, вещество, способное к реакциям ионного обмена или обмена другого типа. Подвижная фаза представляет собой жидкость или газ, протекающий через неподвижную фазу.
Подвижная фаза (газ-носитель или жидкость) непрерывно пропускается через неподвижную фазу (колонка, сорбент и.т.д.). В этот поток дозирующим устройством вводится импульсно анализируемая смесь, которая должна быть газообразной или испаряться в дозаторе в случае газовой хроматографии, или растворяться в подвижной фазе в случае жидкостной.
В процессе хроматографирования вещества, которые входят в анализируемую смесь и помещаются в большинстве случаев в заполненную неподвижной (стационарной) фазой стеклянную, металлическую или пластиковую трубку, называемую хроматографической колонкой, подвергаются одновременному воздействию двух факторов: поток подвижной фазы перемещает их по колонке, а неподвижная фаза тормозит это движение. Торможение (удерживание) каждого компонента различное и пропорционально силе его взаимодействия с неподвижной фазой. В результате этого входящие в анализируемую пробу индивидуальные вещества, слабее взаимодействующие с неподвижной фазой, перемещаются по колонке быстрее, чем более сильно взаимодействующие вещества, и в конечном итоге при подборе оптимальных условий разделения каждый компонент анализируемой смеси концентрируется в колонке в чистом виде, отдельно от других компонентов, перемещается и выходит из колонки отдельно.
Основные
элементы хроматографического процесса
рассмотрим на примере разделения
бинарной смеси в условиях колоночной
жидкостной адсорбционной хроматографии.
Представим себе трубку, заполненную
простым адсорбентом (колонку), через
которую непрерывно течет растворитель
(рис. 1.)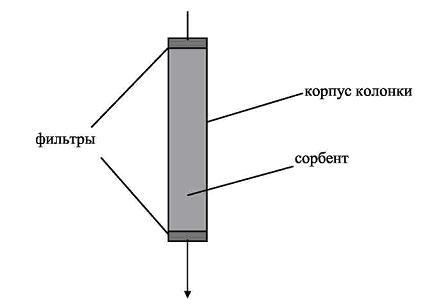
Адсорбент
(сорбент, наполнитель колонки) удерживается
в колонке фильтрами, он неподвижен и
поэтому называется неподвижной фазой.
Растворитель, перемещающийся относительно
сорбента, называется подвижной фазой
(в некоторых случаях элюентом). Введем
в верхнюю часть колонки по одной молекуле
соединений - сорбатов, обозначенных
далее Х и У (рис. 2). При движении вдоль
колонки эти молекулы будут диффундировать
внутри пор сорбента и, в результате
межмолекулярных взаимодействий того
или иного типа, адсорбироваться на
поверхности неподвижной фазы. Естественно,
что на практике в колонку не вводят
единичные молекулы и поэтому данная
картинка предельно упрощает реальную
ситуацию. Если в колонку введены хотя
бы несколько молекул разного вида, то
обнаружим, что средние скорости
перемещения молекул X и У по-прежнему
различны. Помимо этого, скорости
перемещения отдельных молекул каждого
вида отклоняются в ту или иную сторону
от среднего для данного вида значения.
Молекулы сорбатов , первоначально
введенные в колонку в виде мгновенного
импульса, выходят из нее более
продолжительно, это объясняется тем,
что в ходе хроматографической миграции
каждое индивидуальное вещество
перемещается в направляющей системе в
ограниченном (постепенно изменяющемся)
объеме. Эти объемы и соответствующие
им участки длины колонки, равно как
пятна и полосы на хроматографической
пластинке, будем ниже именовать.
хроматографическими зонами, или просто
зонами. Неидентичность скоростей
перемещения одинаковых молекул в
хроматографии называется размываниемОно
связано с рядом явлений в колонке,
которые подробнее рассмотрим позднее.
Это нежелательное явление приводит к
тому, что среди молекул У могут находиться
также молекулы Х, скорость которых
близка к скорости наиболее "быстрых"
молекул У. В результате зоны Х и У могут
частично наложиться одна на другую и
разделение окажется неполным.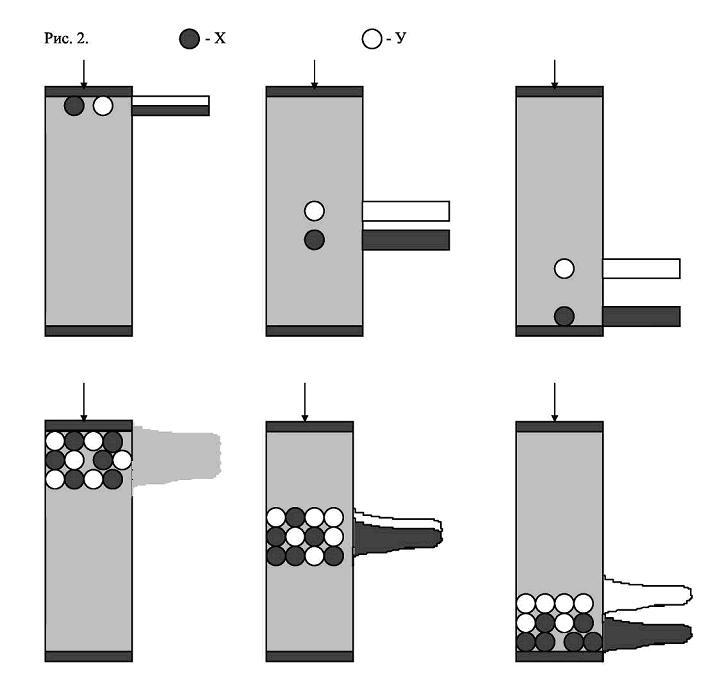
С помощью хроматографии могут быть решены следующие задачи:
1) разделены сложные смеси веществ на отдельные компоненты;
2) установлена идентичность и однородность химических соединений;
3) определен количественный состав сложных смесей или количественное содержание отдельных компонентов;
4) установлена молекулярная структура соединений.
В отличие от других методов, основанных на распределении компонентов между фазами, таких как экстракция и сорбция, хроматографияэто динамический процесс, состоящий из многократных актов сорбции-десорбции компонентов, так как он происходит в потоке подвижной фазы. Такой динамический характер обеспечивает достижение значительно более высокой эффективности хроматографии по сравнению с сорбцией и экстракцией в статических условиях.
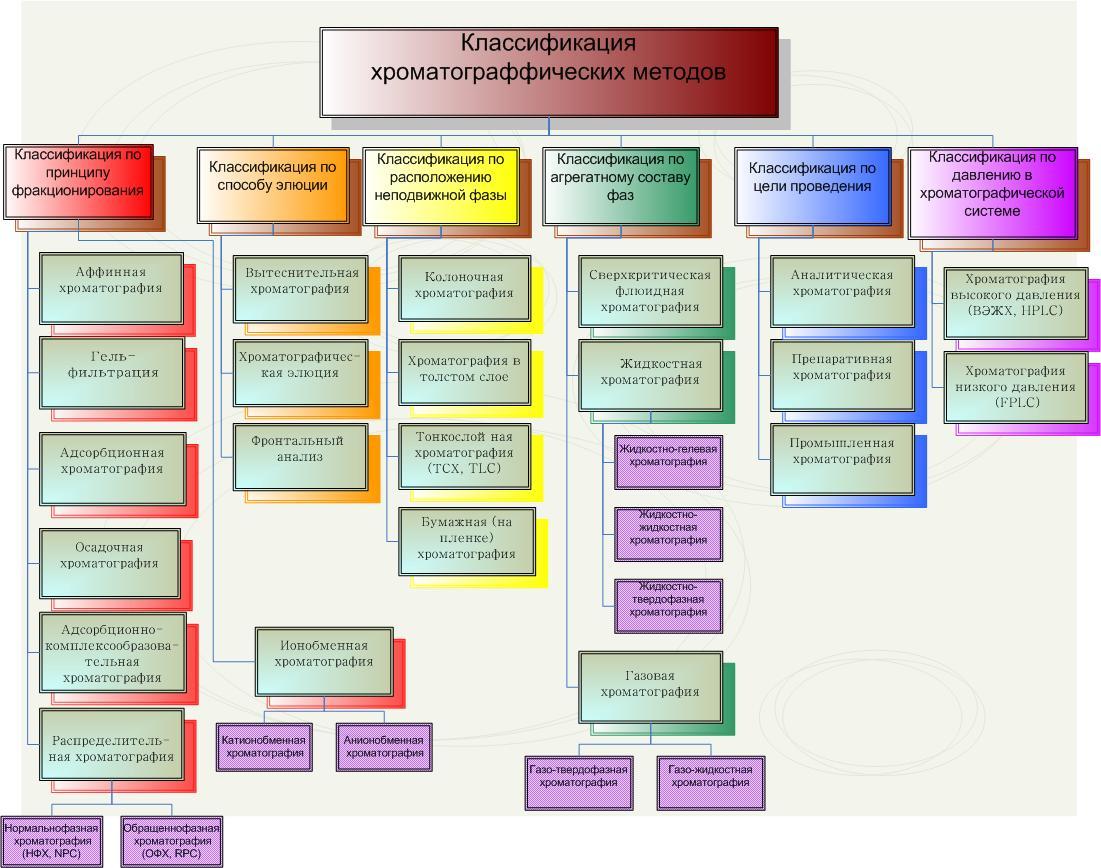
В основу классификации многочисленных хроматографических методов положены следующие признаки: агрегатное состояние подвижной и неподвижной фаз, механизм взаимодействия сорбент – сорбат, форма слоя сорбента (техника выполнения), цель хроматографирования.
В зависимости от агрегатного состояния подвижной фазы выделяют:
По
механизму взаимодействия сорбента и
сорбата различают несколько видов
хроматографии: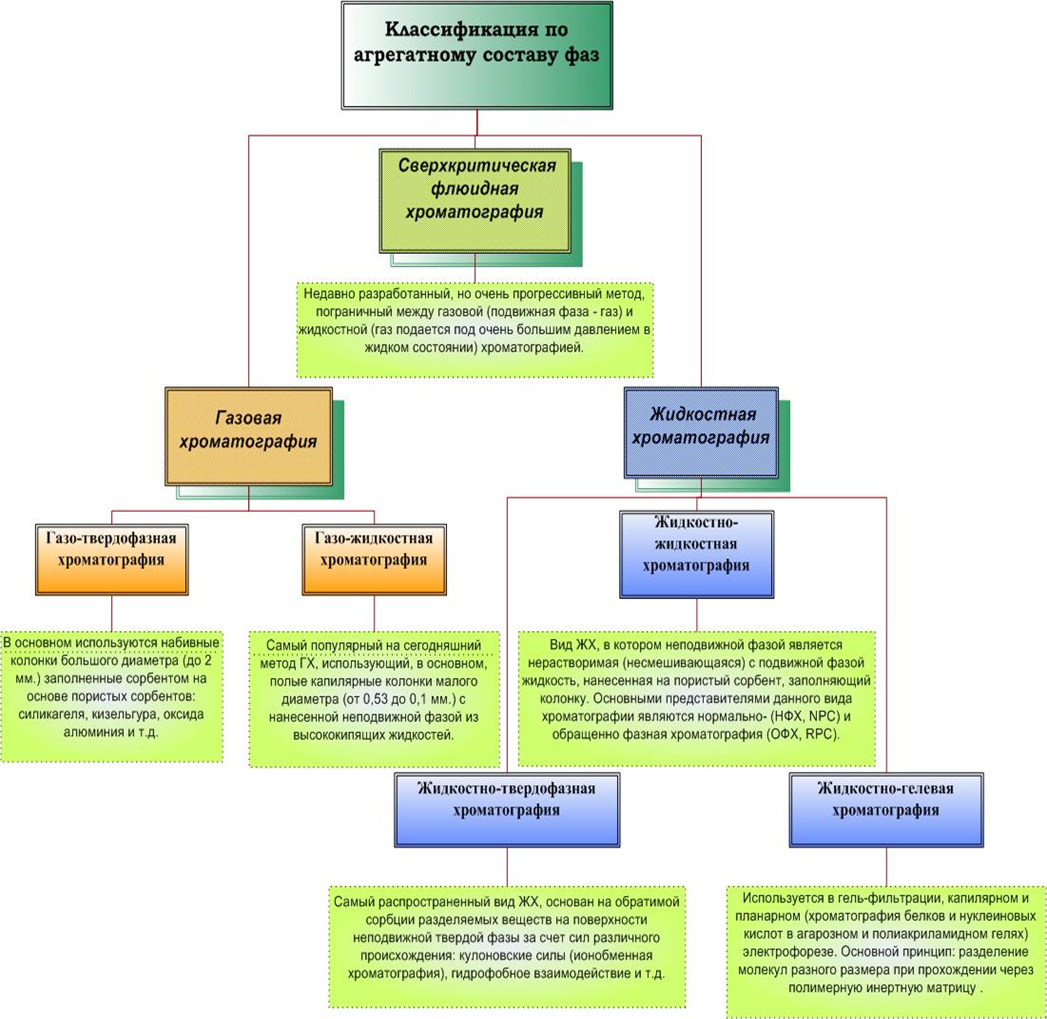
адсорбционная хроматография основана на различной способности компонентов анализируемой смеси адсорбироваться твердым сорбентом;
распределительная хроматография – на различии в растворимости разделяемых веществ в неподвижной фазе (газовая хроматография) или на различии в растворимости веществ в подвижной и неподвижной жидких фазах;
ионообменная хроматография – на разной способности веществ к ионному обмену;
эксклюзионная (ситовая) хроматография – на различии в размерах и форме молекул разделяемых веществ;
аффинная хроматография – на специфических взаимодействиях, характерных для некоторых биологических и биохимических объектов (антитело и антиген, фермент и его субстрат или ингибитор, гормон и соответствующий рецептор);
осадочная хроматография – на образовании отличающихся по растворимости осадков разделяемых веществ с сорбентом;
адсорбционно-комплексообразовательная хроматография – на возникновении координационных соединений разной устойчивости в фазе или на поверхности сорбента.
– хемосорбционная хроматография – за счет образования водородной связи, проявления химического сродства и др.
Следует подчеркнуть, что классификация хроматографических методов по механизму разделения весьма условна: часто процесс разделения протекает сразу по нескольким механизмам.
Таблица 3
Варианты хроматографии, различающиеся по способу проведения
|
Способ проведения процесса разделения |
Название варианта |
|
в цилиндрическом слое сорбента |
колоночная хроматография |
|
в слое сорбента на плоской поверхности |
хроматография в тонких слоях |
|
в пленке жидкости, содержащейся в полоске бумаги |
хроматография на бумаге |
|
в пленке жидкости или тонком слое адсорбента, размещенном на внутренней стенке капилляра |
капиллярная хроматография |
|
в полях электрических, магнитных, центробежных и других сил |
хроматография в полях сил |
В зависимости от цели хроматографирования выделяют:
– аналитическую;
– препаративную (для получения чистых веществ, концентрирования и выделения микропримесей);
– промышленную (производственную) хроматографию, применяемую для автоматического управления производственным процессом.
По способу получения хроматограмм различают элюентную (проявительную), фронтальную хроматографию и вытеснительную.
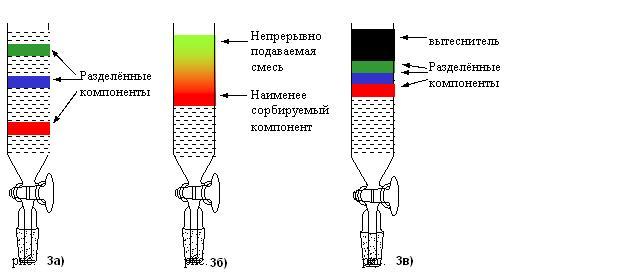
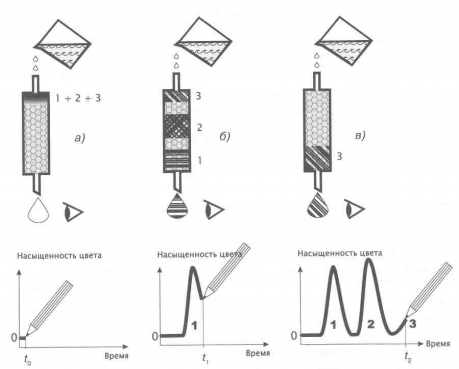
Проявительный (элюационный) метод заключается в том, что сорбаты переносятся через сорбционный слой потоком вещества (элюента), сорбирующегося хуже любого из сорбатов. В ходе проявительного анализа разделенные компоненты анализируемой смеси выходят из хроматографической колонки в потоке элюента отдельными зонами, между которыми (при достаточно четком разделении) из колонки выходит чистый элюент. Вид хроматограммы при осуществлении элюентного разделения представлен на рис. 1.1.
Основные
преимущества проявительного метода
заключаются в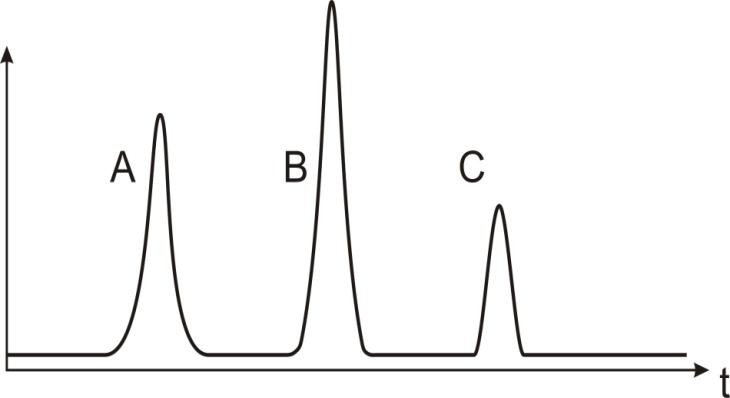
следующем:
1) при выборе соответствующих условий компоненты могут быть, практически полностью, изолированы друг от друга и будут находиться лишь в смеси с элюентом;
2) сорбент непрерывно регенерируется элюентом, поэтому после выхода наиболее сильно сорбирующегося компонента пробы может быть немедленно начато исследование следующей смеси;
3) если концентрация исследуемого компонента соответствует линейному участку изотермы сорбции, то время элюирования компонента при заданных условиях является постоянной величиной, которая может быть использована для целей идентификации.
К недостаткам метода относится необходимость использования значительных количеств элюента.
Проявительный анализ можно проводить как при постоянной температуре (изотермическая хроматография), так и при изменении температуры сорбента в процессе анализа по заданной программе (хроматография с программированием температуры). В последнем случае изменяется сорбционная емкость сорбента.
Фронтальный
метод
заключается в непрерывном пропускании
исследуемой смеси через слой сорбента.
При этом на сорбенте образуются зоны,
содержащие последовательно увеличивающееся
число компонентов, а из колонки вначале
выходит порция наименее сорбирующегося
вещества, а в конце анализа из кологнки
выходит исходная смесь. Фронтальный
анализ применялся на ранних стадиях
развития хроматографии, когда еще не
были достаточно разработаны методы
детектирования. В настоящее время он
используется редко и практически совсем
не применяется для целей количественного
анализа. Это объясняется тем, что при
фронтальном анализе ни один из компонентов
смеси не отделяется полностью от
остальных. Если после полного проявления
концентрационного профиля при фронтальном
анализе прекратить подачу пробы и начать
промывку колонки чистой подвижной
фазой, то фронтальный анализ превратится
в вариант проявительной хроматографии
с очень большой пробой.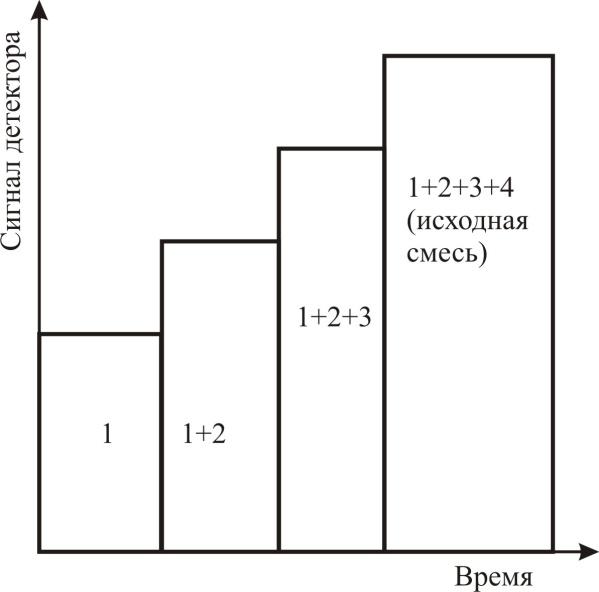
Кривая элюирования будет повторять в обратном порядке кривую фронтального анализа; последняя ступень будет соответствовать относительно чистому последнему (наиболее сильно удерживаемому) компоненту.
К недостанткам фронтального метода можно отнести необходимость регенерации сорбента после каждого анализа и в результате хроматографирования возможно получить в относительно чистом виде только первый компонент.
Вытеснительный
метод
заключается в переносе разделяемой
смеси потоком вещества (вытеснителя),
сорбирующегося сильнее любого из
компонентов смеси. В ходе вытеснительного
анализа образуются отдельные примыкающие
друг к другу зоны компонентов, которые
располагаются в порядке увеличения их
сорбируемости. Порядок элюирования
компонентов характеризует их
физико-химические свойства, а ширина
полосы (не высота!) пропорциональна
концентрации данного компонента.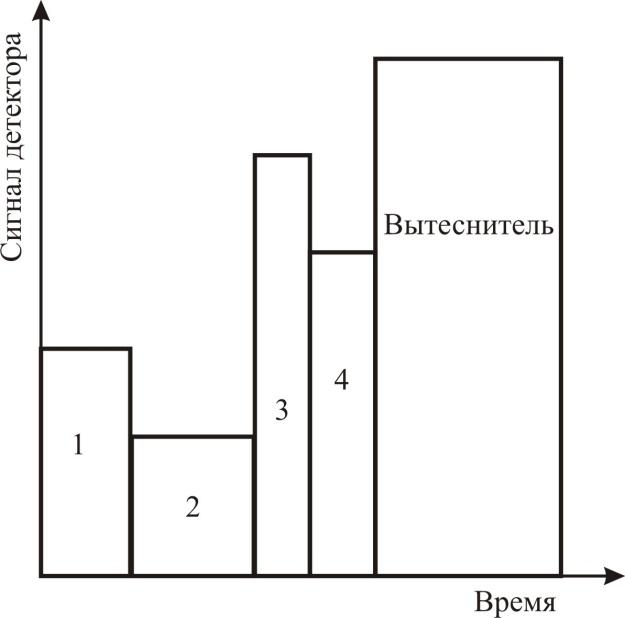
Вытеснительный анализ как метод разделения имеет весьма ограниченное применение и крайне редко используется в количественном анализе. Это объясняется тем, что в результате описанного процесса неполучается дискретных локальных полос индивидуальных соединений.
Электрохроматография — хроматографический процесс, при котором движение заряженных частиц осуществляется под действием приложенного напряжения. Скорость движения частиц определяется их массой и зарядом.
Т а б л и ц а 4
Области применения различных вариантов хроматографии
|
молекулярная масса | ||||||||
|
|
0 |
10 |
102 |
103 |
104 |
105 |
106 |
107 |
|
|
|
газы |
жидкости |
твердые вещества |
полимеры |
вирусы |
бактерии |
частицы |
|
газовая ионообменная полифазная | ||||||||
|
ионная жидкостная | ||||||||
|
электрофорез ситовая | ||||||||
|
разделение в полях гидродинамическая | ||||||||