
- •Комплексные соединения
- •Основные положения и понятия координационной теории.
- •Классификация и номенклатура комплексных соединений.
- •Комплексообразующая способность s-, р- и d- элементов
- •Характер химической связи в комплексных соединениях.
- •Внешнеорбитальные и внутриорбитальные комплексы
- •Представления о строении металлоферментов и других биокомплексных соединений (гемоглобин, цитохромы, кобаламины).
- •Устойчивость комплексных соединений в растворах
- •Механизм токсического действия тяжелых металлов.
- •Значение комплексных соединений в медицине.
Устойчивость комплексных соединений в растворах
Ионы внешней сферы соединены с комплексом ионной связью, поэтому в водных растворах они легко отщепляются: [Fe(Н2О)6]SO4 ↔ SO42- + [Fe(Н2О)6]2+.
Этот процесс называется первичной диссоциацией. Внутренняя сфера в зависимости от прочности также способна диссоциировать на комплексообразователь и лиганды:
[Fe(Н2О)6]2+
↔ Fe2+
+ 6 Н2О
– это вторичная
диссоциация.
Она аналогична диссоциации слабых
электролитов и характеризуется константой
равновесия: Крав.
=
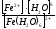
константа равновесия может служить мерой прочности комплекса: чем менее стоек комплекс, тем больше концентрация простых ионов или молекул Fe2+ и Н2О, тем больше численное значение константы. Поэтому константу равновесия,
называют константой нестойкости комплекса. Величина, обратная константе нестойкости, называется константой устойчивости:
Куст.=
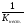 =
= .
.
Механизм токсического действия тяжелых металлов.
Всем известно, что загрязнение окружающей среды соединениями тяжелых металлов: ртути, свинца, кадмия, хрома, никеля и др. металлов – может привести к тяжелым отравлениям.
Механизм токсического действия таких соединений объясняется взаимодействием катионов тяжелых металлов (Мт) с бионеорганическими комплексами. Это можно записать в виде реакции:
МбL + Мт ↔ Мб + МтL
Где МбL – комплекс иона биогенного металла Мб (Fe, Zn, Cu, Co) с биоорганическим лигандом L (например порфирином); Мт – ион тяжелого металла.
Если устойчивость комплекса МтL больше, чем устойчивость МбL, происходит смещение равновесия вправо и в организме накапливаются соединения МтL, что приводит к нарушению нормальной работы организма.
Значение комплексных соединений в медицине.
Комплексообразование имеет большое значение для многих биологических процессов. В виде аквакомплексов находятся в крови, лимфе и тканевых жидкостях ионы щелочных и щелочноземельных металлов, выполняющих в организме важные и многообразные физиологические функции. Ионы d – элементов в результате высокой комплексообразующей способности находятся в организме исключительно в виде комплексов с белками и входят в состав гормонов, ферментов, витаминов и других жизненно важных соединений. Некоторые комплексные соединения обладают биологической активностью и применяются в качестве лекарственных препаратов - например витамин В12 , участвующий в процессах кроветворения, является комплексом кобальта.
Токсические свойства некоторых веществ обусловлены их высокой комплексообразующей способностью. Например, токсическое действие на организм цианидов и оксида углерода объясняется их способностью образовывать прочные комплексы с катионами железа. Цианиды блокируют атомы железа, входящие в состав дыхательного фермента цитохромоксидазы, в результате прекращается клеточное дыхание. Оксид углерода (СО) связывает железо гемоглобина, вследствие этого гемоглобин утрачивает способность осуществлять транспорт кислорода.
В медицинской практике при лечении многих заболеваний в качестве лекарственных препаратов используются соединения меди, серебра, цинка, кобальта, хрома, золота, платины, ртути и др.
