
- •Ароматичность
- •Взаимное влияние атомов в молекуле
- •Индуктивный эффект
- •Мезомерный эффект
- •Классификация органических реакций
- •Вопросы для самоконтроля:
- •Упражнения
- •Тесты для самостоятельной работы студентов
- •Органические кислоты
- •Основность органических соединений.
- •Факторы, влияющие на основность
- •Вопросы для самоконтроля
- •Упражнения
- •Тесты для самостоятельной работы студентов Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
Упражнения
Укажите соединения, в которых имеется: 1) - сопряжение, 2)р- сопряжение, 3) открытая или замкнутая сопряженная системы.
А) бутадиен-1,3 Б) гексатриен-1,3,5 В) фенол
Г) фуран Д) тиофен Е) бензол Ж) толуол
З) нафталин И) пиридин К) пиррол
Укажите соединения, которые являются ароматическими и какие не ароматическими:
А) бутадиен-1,3 Б) гексатриен-1,3,5 В) фенол
Г) фуран Д) тиофен Е) бензол Ж) толуол
З) нафталин И) пиридин К) циклогексан
В ниже приведенных соединениях:
1) укажите электронные эффекты (±I или ±М) ОН группы,
2) укажите соединения, в которых ОН группа является ЭД или ЭА
А) этанол, Б) глицерин, В) бензиловый спирт,
Г) п-аминофенол, Д) фенол, Е) 4-гидрокси бутановая кислота
В ниже приведенных соединениях:
1) укажите электронные эффекты (±I или ±М) NН2 группы,
2) укажите соединения, в которых NН2 группа является ЭД или ЭА
А) анилин, Б) этиламин, В) этаноламин,
Г) п-аминофенол, Д) п-аминобензойная кислота,
Е) 4-аминобутановая кислота
В ниже приведенных соединениях:
1) укажите электронные эффекты (±I или ±М) СООН группы,
2) укажите соединения, в которых СООН группа является ЭД или ЭА
А) этановая кислота, Б) пропановая кислота, В) бензойная кислота, Г) п-аминобензойная кислота,
Д) 4-гидроксибутановая кислота
Тесты для самостоятельной работы студентов
Вариант 1
Укажите соединения, в которых ОН-группа является электронодонорным заместителем:
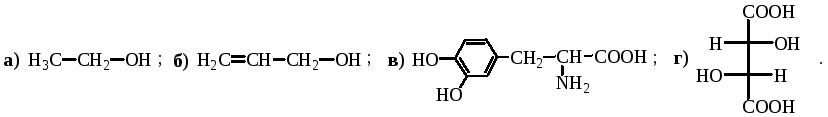
Укажите электронный эффект: а) + М, б) – М, в) + I, г) – I ; СООН-группы в соединениях:
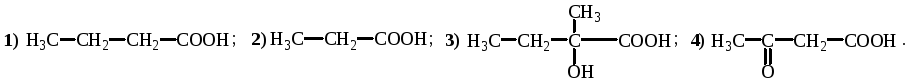
Укажите соединения, в которых имеется π,π-сопряженная система:
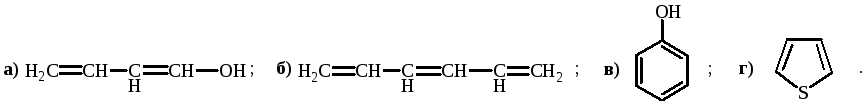
Укажите соединение, которое не является ароматическим:

Укажите соединение, которое не является сопряженным:
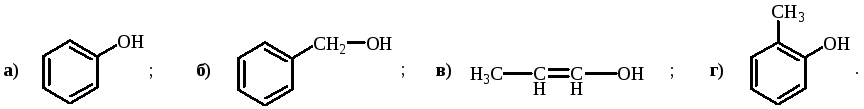
Вариант 2
Укажите соединения, в которых ОН-группа является электронодонорным заместителем:
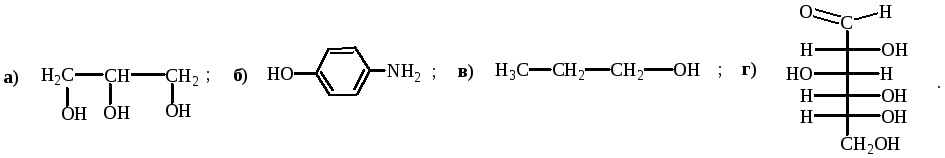
Укажите соединения, в которых NH2-группа является электроноакцепторным заместителем:
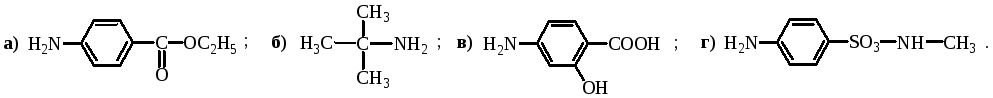
Укажите электронный эффект: а) + М, б) – М, в) + I, г) – I ; ОН-группы в соединениях:
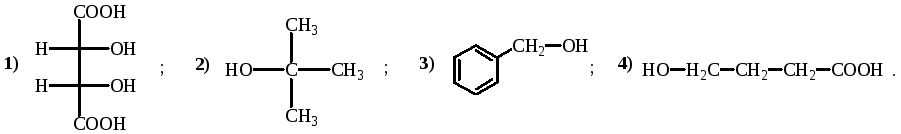
Укажите соединения, в которых имеется π,р-сопряжение:
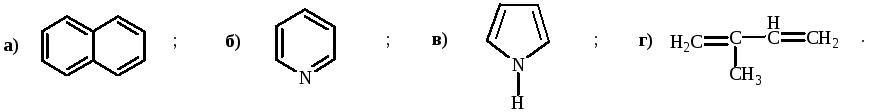
Укажите соединение, в котором нет сопряжения:
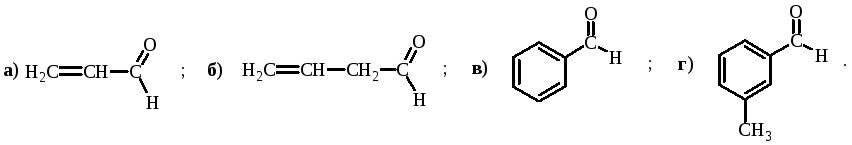
Вариант 3
Укажите соединения, в которых ОН-группа является электронодонорным заместителем:
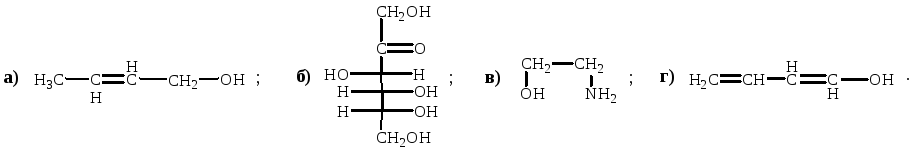
Укажите соединения, в которых NH2-группа является электроноакцепторным заместителем:
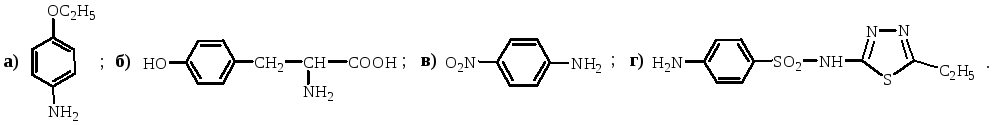
Укажите электронный эффект: а) + М, б) – М, в) + I, г) – I ; NH2-группы в соединениях:
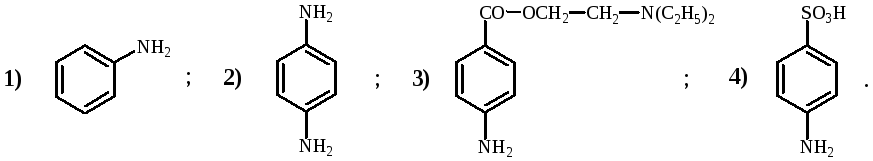
Укажите соединения, в которых имеется π,π-сопряжение:
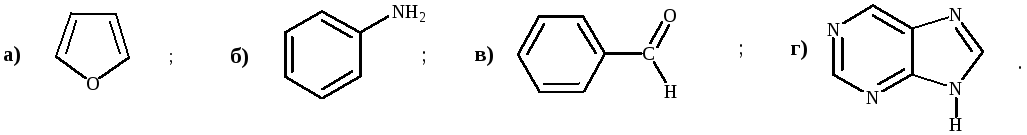
Укажите соединение, которое не является ароматическим:
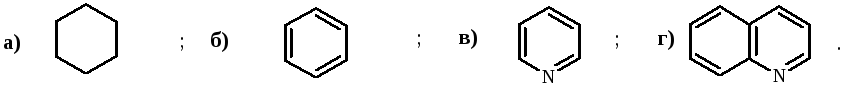
Вариант 4
Укажите соединения, в которых NH2-группа является электронодонорным заместителем:
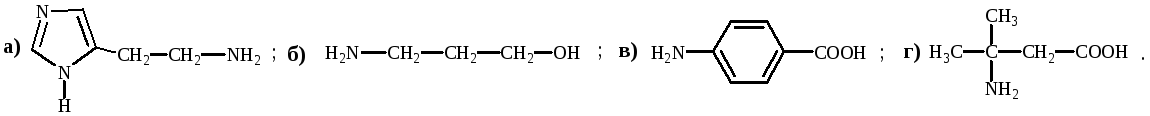
Укажите электронный эффект: а) + М, б) – М, в) + I, г) – I ; СООН-группы в соединениях:
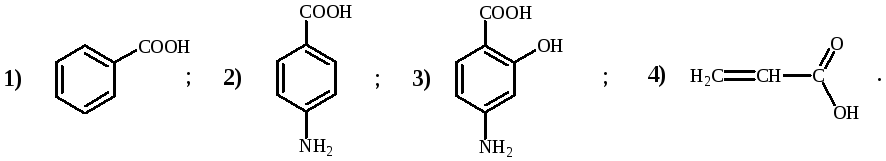
Укажите соединения, в которых имеется π,р-сопряжение:
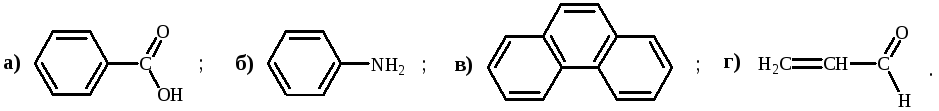
Укажите соединение, в котором нет сопряжения:
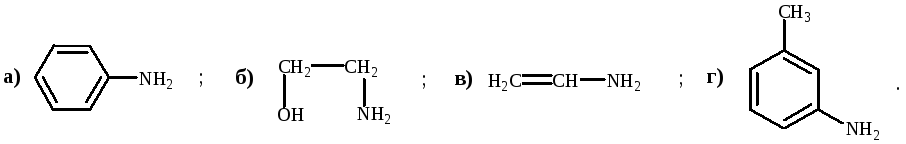
Укажите соединение, которое не является ароматическим:
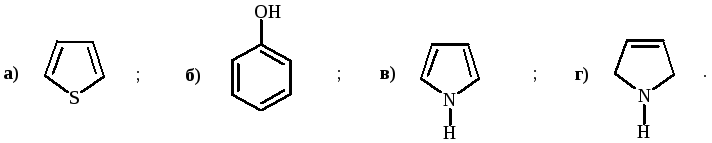
Вариант 5
Укажите соединения, в которых ОН-группа является электроноакцепторным заместителем:
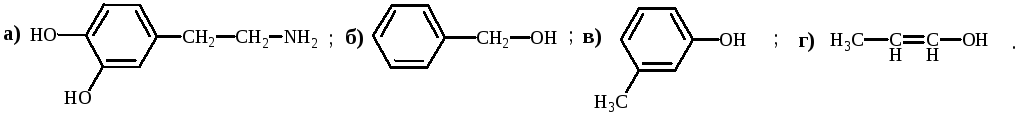
Укажите соединения, в которых NH2-группа является электронодонорным заместителем:
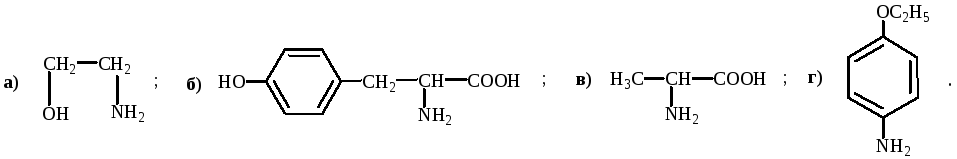
Укажите электронный эффект: а) + М, б) – М, в) + I, г) – I ; ОН-группы в соединениях:
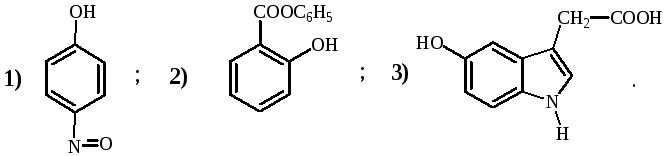
Укажите соединения, в которых нет сопряжения:
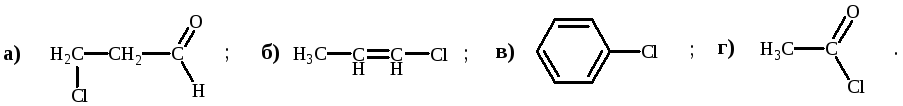
Укажите соединение, которое не является ароматическим:
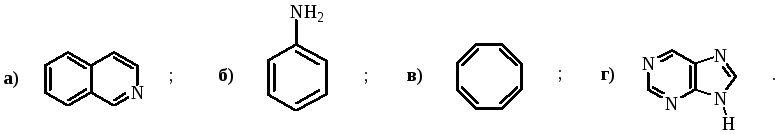
Ответы к тестам “ Взаимное влияние атомов в молекуле.”
|
вариант вопрос |
1 |
2 |
3 |
4 |
5 |
|
1 |
в |
б |
г |
в |
б |
|
2 |
б,г |
б |
б |
б,г |
г |
|
3 |
б |
г |
а,г |
б |
а,г |
|
4 |
в |
в |
в |
б |
а |
|
5 |
б |
б |
а |
г |
в |
Литература:
Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия, стр. 100 - 116
Кислотность и основность органических соединений
Важными аспектами реакционной способности органических соединений является их кислотные и основные свойства. Для описания кислотных и основных свойств химических соединений существует несколько теорий – теория Бренстеда и Лоури, теория Льюиса и ряд других. Наиболее распространенной является теория Бренстеда и Лоури, или протолитическая теория.
По теории Бренстеда – Лоури кислоты – это нейтральные молекулы или ионы, способные отдавать протон (доноры протона), а основания - это нейтральные молекулы или ионы, способные присоединять протон (акцепторы протона).
По теории Льюиса кислоты – это нейтральные молекулы или ионы, способные присоединять электронную пару (акцепторы электронной пары), а основания – это нейтральные молекулы или ионы, способные отдавать электронную пару (доноры электронной пары).
Из этого следует, что теоретически любое соединение, в состав которого входит атом водорода может его отдавать в виде протона и, проявлять свойства кислоты. Способность отдавать протон могут проявлять не только нейтральные молекулы (HCl, ROH), но и заряженные частицы – катионы (NH4+) и анионы кислот (HSO4- и др.).
В роли оснований могут выступать анионы – частицы, несущие отрицательный заряд, например С1-, OH-, HSO4-. Основаниями могут быть и нейтральные молекулы, в состав которых входит гетероатом, имеющий неподелённую пару электронов, например спирты ROH, NH3, Н2О.
Нейтральные молекулы или ионы, способные в зависимости от природы второго компонента проявлять свойства кислот или оснований называются амфотерными. Например, вода. Она может быть кислотой, отдавая протон, и основание, принимая протон:
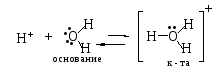
Кислоты и основания проявляют свои свойства только в присутствие друг друга. Ни одно вещество не будет отдавать протон, если в системе нет акцептора протона – основания, и наоборот. Таким образом, они образуют сопряжённую кислотно – основную пару в которой чем сильнее кислота, тем слабее сопряженное ей основание, и чем сильнее основание, тем слабее сопряженная ему кислота.
Кислота, отдавая протон, превращается в сопряженное основание, а основание, приняв протон, превращается в сопряженную кислоту. Кислоту обычно обозначают АН, а основание – В
Например:
1) НС1↔ Н+ + С1-,
где НС1 – сильная кислота; С1- ион – сопряженное слабое основание;
2) СН3СООН ↔ СН3СОО- + Н+,
где СН3СООН – слабая кислота, а СН3СОО- - ион сопряженное сильное основание.
Общий вид можно представить так:
Н+│ : А + В ↔ Н:В+ + А:-
к-та основ. сопр. сопр.
к-та основ.
