
- •1.Структура и рольРнк
- •У мужчин:
- •У женщин:
- •3.Желчные кислоты
- •Инсулин
- •Глюкагон
- •3.Клинич знач наруш безазотист комп крови
- •Основные показатели кор:
- •3.Роль ц.Кребса в обм
- •1.Участв в биол окислении
- •3.Синтез нукл к-т
- •Ингибиторы взаимодействуют с ферментами различными путями, они могут:
- •У мужчин:
- •У женщин:
- •1.Горм гипот и гипофиза
- •Система фибринолиза
- •3.Метаболизм арахидоновой кислоты:
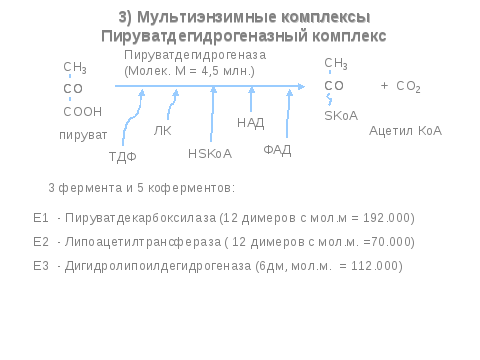
- •2 Этап. Окислительное декарбоксилирование пвк, катализируется мультиферментной системой и протекает в
- •Участие витамина с в метаболизме
- •Нарушения обмена порфиринов
- •Регуляция концентрации глюкозы крови.
1.Участв в биол окислении
а)Углев обм.- Окислительное декарбоксилирование пирувата и а- кетоглутарата
б)лип обм-b-окисление жирных кислот
Витамин В1 содержится практически во всех животных ткинях и растениях, богатым источником рибофлавина являются дрожжи,
мука грубого помола.
В животных тканях больше всего витамина содержится в печени, почках, сердце, а также в молочных продуктах и рыбе (треска). Суточная доза витамина: 2-3 мг.
Витамин В6 (пиридоксин,антидерматитный)
ГиповитаминозДерматиты, поражения слизистых Гомоцистинурия
Нарушения обмена триптофана
Судороги
Распространение: Печень, почки, мясо,
хлеб, горох, фасоль, картофель. Суточная потребность витамина В6 составляет 2 мг
Уч в обм проц:
1. Реакции переаминирования – кофактор аминотрансфераз(АЛТ, АСТ)
2. Декарбоксилирование a-аминокислот - синтез биогенных аминов
3. Синтез гема - кофактор d-Аминолевулинатсинтза
4. Пиридоксльфосфат учавствует в синтезе витамина РР из триптофана
5. Пиридоксальфосфат входит в состав гликоген- фосфорилазы.
3.Клинич знач ЛДГ
1.инфаркт миокарда
(уже спустя неск часов после начала иефаркта наблюд значит повыш актив ЛДГ в сывор крови)
2.заболев печени(при паренхим гепатите акт-ть сывороточной ЛДГ повыш,при мех желтухе-акт-ть ЛДГ в норме,при карциномах печени и метастазах рака в печень может иметь место подъем акт-ти ЛДГ
Акт-ть ЛДГ возраст при прогрессивной мыш дистрофии,хронич лимфогранулематозах,лейкозах,пернициозной анемии и др
Билет12
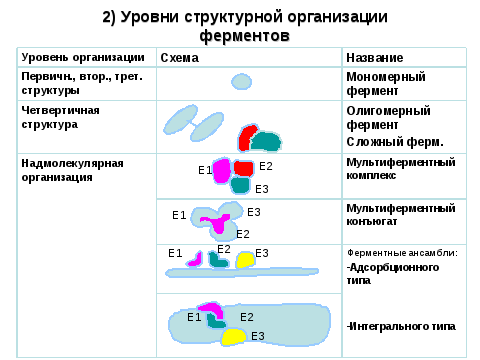
Виды организации полиферментных систем:
-Функциональная организация ( гликолиз – связующим звеном между растворенными ферментами являются метаболиты)
-Структурно – функциональная организация ( ПВК –ДГ комплекс, синтетаза ВЖК; фермент – ферментные взаимодействия -> структурные полиферментные надмолекулярные комплексы.
-Смешанный тип организации ( комбинация 1 и 2 - цикл Кребса; часть ферментов объединена в структурный комплекс, а часть соединена функционально с помощью связующих метаболитов.
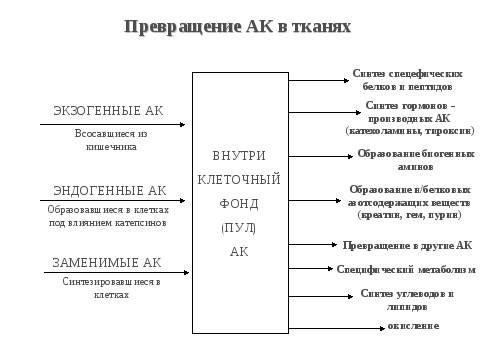
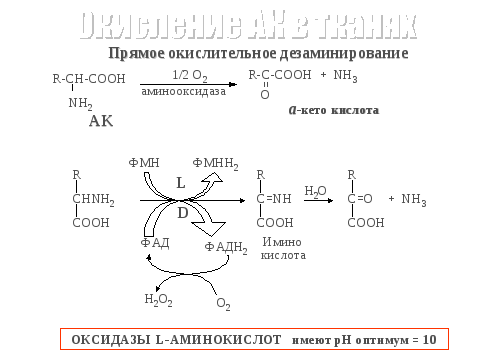
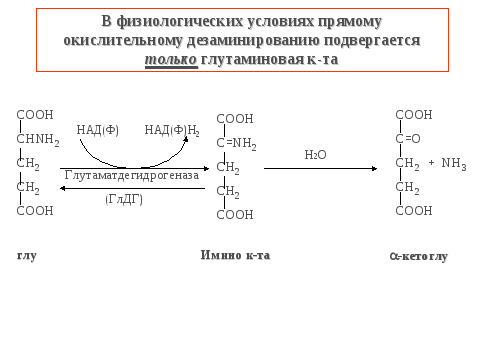
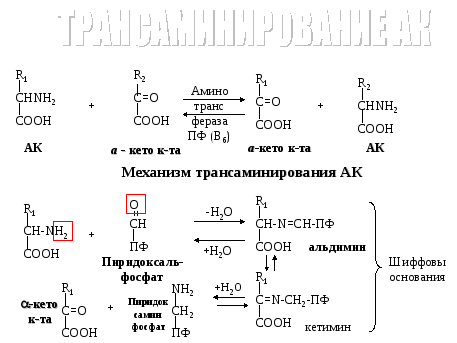
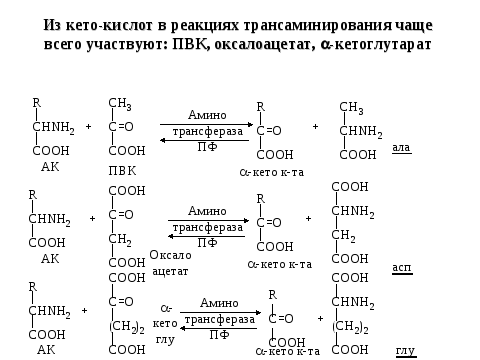
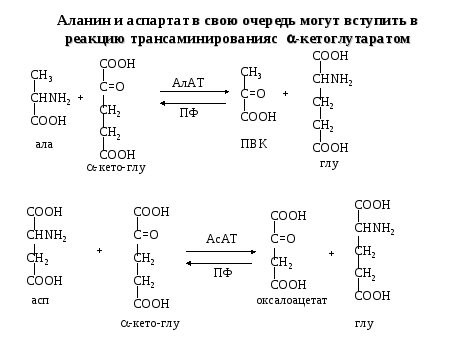
2.Окисление АК в тк,дезаминир

 3.Особ-ти
строения и мет-ма нерв ткани
3.Особ-ти
строения и мет-ма нерв ткани
Нервн тк имеет общ черты,кот присущи Кл любой тк,а также спецефич особ-ти,определяемые хар-м функций.Эти особ-ти проявл как в химич составе так и в метаболизме.
Морфологич состав:
1. Нейроны - нервные клетки, участвующие в генерации и передачи нервных импульсов. Основная функция: распространение и интегрирование информации в организме.
2. Нейроглия - система обкладочных клеток между нейронами, выполняющих трофическую и защитную функции и образующих изоляционный слой вокруг отростков нейронов в виде миелиновой оболочки.
3. Микроглия - глиальные макрофаги (клетки Ортеги).
Особенности Метаболизма Нервной Ткани
Высокий аэробный обмен (газообмен в мозге превышает газообмен в мышечной ткани в 20 раз). У человека головной мозг составляет 2-2,5% веса тела, а потребляет 10-20% кислорода, поглощаемого организмом.
Основной энергетический субстрат для нервной ткани - глюкоза. Ни один орган не поглощает глюкозу крови с такой скоростью и в таких количествах, как мозг. За 1 минуту 100 г ткани мозга потребляют 5 мг глюкозы. 85% глюкозы в мозговой ткани расходуется в цикле крэбса, 12% - в анаэробном гликолизе (до лактата) и 3% - по пентозофосфатному пути, образуя НАДФ•Н2, рибозу для синтеза РНК.
Виды нейромедиаторов:
Возбуждающие медиаторы - вызывают деполяризацию постсинаптической мембраны
Тормозные медиаторы - способствуют гиперполяризации мембраны, увеличивая прони-
цаемость мембраны для ионов К+ и Cl-.
1. Ацетилхолин - синтезируется из холина и активной формы уксусной кислоты - аце-
тилКоА. Обеспечивают переключение воздействий стволовой части мозга на кору
больших полушарий.
2. Норадреналин - синтезируется из тирозина. Синтезируется в основном в нейронах голубого ядра. Играет важную роль в формировании психоэмоционального состояния.
3. Дофамин - синтезируется преимущественно в нейронах чёрной субстанции из тирозина.
4. Серотонин - образуется нейронами ядер шва из триптофана. Связан с процессами сна.
5. Глутамат - образуются путём дезаминирования глутамина или из кетоглутаровой кислоты
6. ГАМК - основной тормозный медиатор (30%). Участвует в организации памяти.
7. Аденозин
8![]() .
Глицин - при
избытке может привести к нарушениям
психоэмоциональных функций.
.
Глицин - при
избытке может привести к нарушениям
психоэмоциональных функций.
Билет 13
1.Микросомал окисление
Одна из задач свободного(несопряженного) окисления-превращение природных или неприроднвх субстратов,называемых в этом случае ксенобиотиками(ксено-несовместимый,бИОС-жизнь)Они осуществляются ферментами диоксигеназами и монооксигеназами.Окисление протекет при участии специализированных цитохромов,локализованных чаще всего в ЭПР,поэтому иногда этот процесс называют микросомальным окислением. В реакц свобод окисл участв также кислород и восстановленные дыхат переносчики(чаще всего НАДФН).Акцептором электронов явл цитохром Р-450(иногда b-5).Окисление субстрата протекает по след схеме:SH+O2=SOH. В процессе свободного окисления вследствие особенностей используемых цепей передачи электронов не происходит образования АТФ.Биологич роль этих процессов заключается в метаболизме ряда природных и ксенобиотич субстратов.В послед случае свобод окисление выполн функц модификации чужерод соединений.(лек-ва,гербициды,продукты загрязнения окруж среды,попадающ в орг-м с водой,пищей,воздухом.

2.Биосинтез пуриновых и пиримидиновых оснований
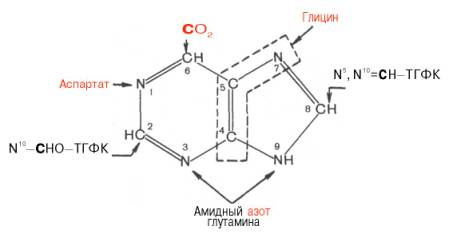
1. путь основной пурины, этапы включния:
1 этап - синтез Инозиновой кислоты.
1.Рибозо-5-фосфат 5-фисфорибозил-1-пирофосфат(ФРПФ) 5-фосфорибозиламин глицинамидрибонуклеотид
N-формилглицинамидрибонуклеотид
N- формилглицинамидинрибонуклеотид
5 – аминоимидазолрибонуклеотид рибонуклеотид-5-аминоимидазол-4-карбоновой кислоты5-аминоимидазол-4N-сукцинокарбоксамидрибонуклеотид5-аминоимидазол-4-карбоксамидрибонуклеотид5-формамидоимидазол-4-карбоксамидрибонуклеотидинозиновая кислота(ИМФ)
2 этап – синтез пуриновых нуклеотидов (АМФ и ГМФ):
ИФМксантиловая кислотаГМФ
ИМФАденилоянтарная кислотаАМФ
2. Синтез пуриновых нуклеотидов из аденина и гуанина:
Фосфорибозилирование пуриновых оснований («путь спасения»=регенерации):
![]()
Синтез пиримидиновых нуклеотидов:
I стадия синтеза УМФ включает образование карбамоил-фосфата из глутамина.
На II стадии карбамоилфосфат реагирует с аспартатом, образуется N-карбамоил-аспарагиновая кислота, подвергается циклизации образуется дигидрооротовая кислота, которая, подвергаясь дегидрированию, превращается в оротовую кислоту, реагирует с ФРПФ с образованием оротидин-5'-фос-фата (ОМФ). Декарбоксилирование приводит к образованию первого пиримидинового нуклеотида – уридин-5-фосфата (УМФ). 1)Синтез цитидиловых нуклеотидов:
2)Превращение дУМФ в дТМФ: УМФ(Тимидилатсинтаза)ТМФ
3.Биологическая роль и клиническое значение определения липопротеинов плазмы крови.
ЛПОНП-образ в печени и явл гл ьранспорт формой эндогенных триглицеридов
Клинич знач:дислипопроотеиннмия-изм в сод ЛП в плазме крови
Тип1-гиперхиломикронемия(повыш сод ХМ,норм или слегка повыш сод ЛПОНП,повыш Ур триглицеридов.Ксантоматоз)
Тип2а-гипер-В-липопротеинэмия(повыш ЛПНП,в норме Ур триглицеридов)
Тип 2б-гипер-В-липопротеиэмия)повыш ЛПНП,ЛПОНП,повыш ур триглицеридов)
Тип3-дис-В-липопротеинемия(в сывор появл ЛП повыш сод холестерина,ИБС,пораж сос ног)
Тип4-гиперпре-В-липопротеинемия(повыш Ур ЛПОНП,норм сод ЛПНП,отсутств ХМ,повыш сод триглиц,диабет,ожирение)
Тип5-гиперпре-В-липопротеиемияили гиперхиломикронемия(повыш Ур ЛПОНП,налич ХМ,ксантоматоз)
Билет14
1.Окислит фосфорилирование
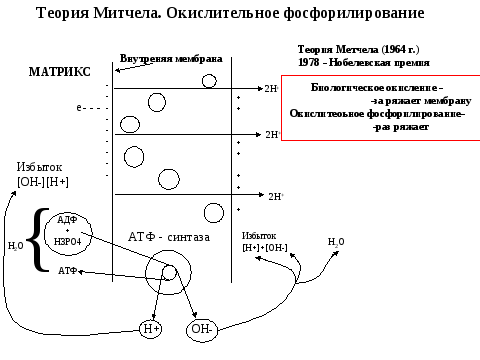
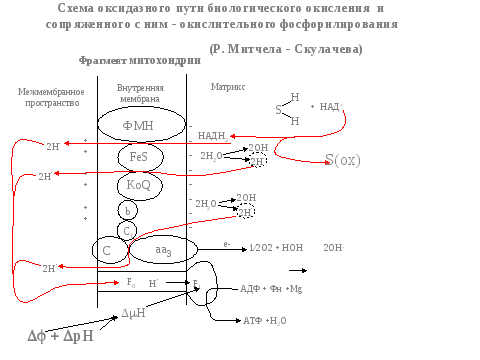
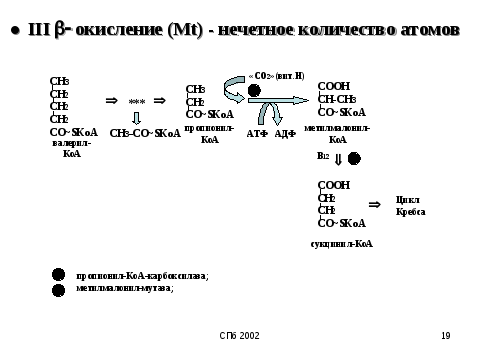
2.Окисление жирных кислот в Кл

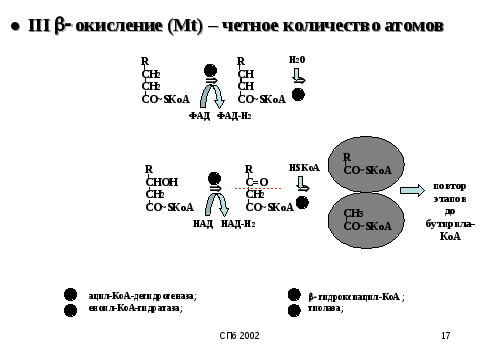
3.Иммуноглобулины или антитела,синтезируются В-лимфоцитами или образующимися из них плазматическими клетками.
5классов:IgA,G,M,D,E.Мол-ла иммуноглобулина состоит из двух идентичных пар полипептидных цепей.Каждая пара в свою очередь состоит из двух разных цепей:легкой(L) и тяжелой(Н).Каждая цепь разделена на спецефические домены или участки,имеющие определенное структурное и функциональное значение
Билет15
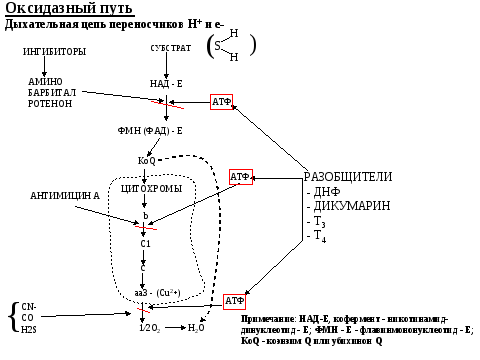
1.Оксидазный путь окисления

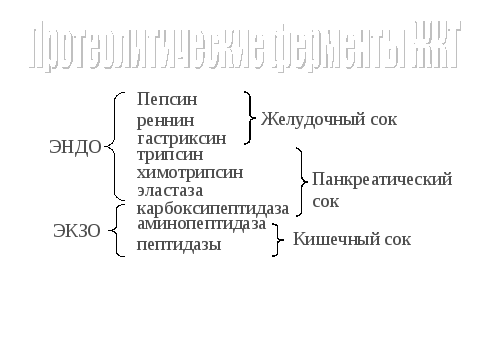
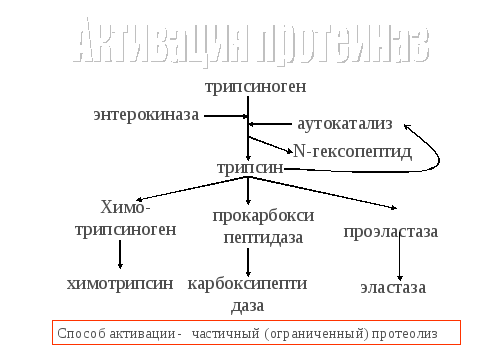
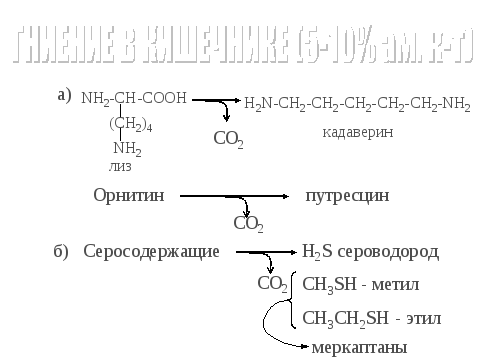
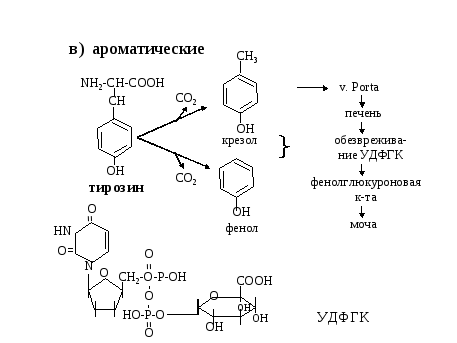
2.Переваривание белков в ЖКТ

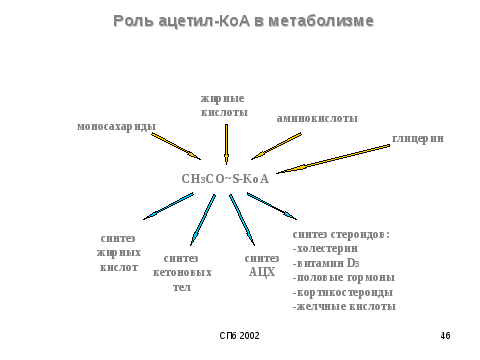
3.Метаболизм Ац-коА в Кл
Билет16
1.Биологическое окисление
Биологич окисление-совокупность реакций окисления субстратов в живых клетках,осн fкот-энергетич обеспечение метаболизма
2.вит К
Витамин К(филлохинон, антигеморрагический)
ГИПОВИТАМИНОЗ (редко):
-снижается свертывающая способность крови;
-развивается кровоизлияния в слизистых;
АВИТАМИНОЗ-редко(синтезируется в ЖКТ)

Витамин К(содержание в продуктах, мкг/г)
листья каштана шпинат крапива
люцерна овес томаты картофель
СУТОЧНАЯ НОРМА 1 МГ
3.Клинич знач опред липидов в крови
1.Клинич знач опред общих липидов
Гиперлипемия-мех и паренхим желтуха,острый и хронич гепатит,при диабете
Липурия-после приема с пищей больших к-в жира,при переломах трубчатых костей,сопровождающихся размножением костного мозга,травме обширн уч жиров тк,при липоидном нефрозе.
2.Клинич знач определ триглицеридов
Содерж ТГ повыш при нефрозах,диабете,беременности,панкреатитах…
3.Клинич знач фосфолипидов
Гиперфосфолипидемия-при диабете,гипотиреозе,гломерулонефрите,нефрозе,забол печени.
Гипофосфолипидемия-при тяжел формах острого гепатита,портального цирроза.
Клинич знач опред холестерина:
Гиперхолестеринемия-при микседеме,менингитах,диабете,беременности,при липоидном нефрозе,атеросклерозе
Гипохолестеринемия-при гипертиреозе,кахексии,хронич серд недостат,легочном туберкулезе,остром панкреатите,гемолитической желтухе
Клинич знач опред жирн к-т:
Гиперлипацидемия—при нефрозах,диабете,при голодании
Гиполипацидемия-при гипотиреозах,при лечении глюкокортикоидами
Билет17
1.Множест формы ферм.Изоферменты
4 Множественные молекулярные формы ферментов - это семейство или группа ферментов, катализирующих одну и ту же реакцию, но отличающихся по целому ряду физико – химических свойств:
-
По электрофоретической подвижности
-
По адсорбционным свойствам
-
По оптимуму рН
-
По термостабильности
-
По чувствительности к ингибиторам и сродству к субстрату
-
По способности образовывать комплексы с аналогами коферментов
ИЗОФЕРМЕНТЫ - это молекулярные формы ферментов, возникающие вследствие генетических различий в первичной структуре ферментного белка.

2.Сравнить энергетическую ценность окисления молекулы глюкозы и жирной кислоты с 6-ю углеродными атомами до С02 и Н20
Всего на 1 моль глюкозы в аэробн усл=38АТФ
С6
С-С/-С-С/-С-С/
5*3=15
12(атф)*3(*ацкоа)=36
-1(на активацию)
+6(сукцинил коА)
-1
=55АТФ
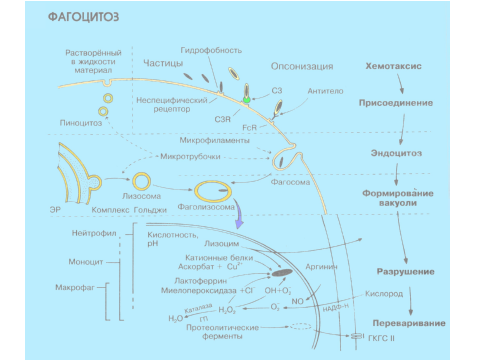
3.Биохимич основы фагоцитоза
Билет18
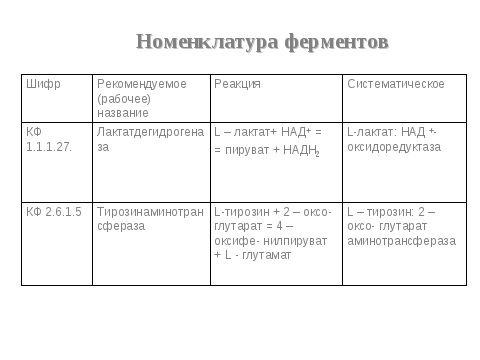
1.Классификация и номенклатура ферментов. Единицы измерения ферментативной активности.
Классификация ферментов
-
ОКСИДОРЕДУКТАЗЫ:
А) дегидрогеназы
-аэробные
-анаэробные
Б) цитохромы
2. ТРАНСФЕРАЗЫ: метил-, формил-, ацетил-, амино-, фосфо-.
3. ГИДРОЛАЗЫ: эстеразы, гликозидазы, фосфотазы, пептидгидролазы, амилазы.
4. ЛИАЗЫ:
-карбокси – лиазы
- амидин – лиазы
5. ИЗОМЕРАЗЫ:
А) рацемазы
Б) эпимеразы
В) внутримолекулярные оксидоредуктазы и трансферазы
6. ЛИГАЗЫ (синтетазы)
2. Способы выражения активности ферментов.
Используются 2 основные единицы:
-
КАТАЛ – такое количество фермента, которое может осуществить превращение 1 моль субстрата за 1 сек.
Катал = Моль/с, мМоль/с, мкМоль/с, нМоль/с
2) IU - International Units
МЕ( международная единица) – то количество любого фермента, которое катализирует превращение 1 мкМоля субстрата в минуту при заданных условиях.
МЕ = мкМоль / мин
Активность ферментов в сыворотке и плазме крови - в единицах на 1 литр : МЕ/л, Е/л
IU(МЕ) нкат/л К = 16,67
1 МЕ = 16,67 нкат/л
2.Витамин РР (никотинамид, антипеллагрический витамин)
Гиповитаминоз
Недостаток витамина РР вызывает пеллагру.
Пеллагра” означает по-итальянски “шероховатая кожа”. Испанский врач Касел впервые описал ее в 1735 г. и указал на важность в питании человека мяса, молока в предупреждении и лечении пеллагры.
Клиническая картина пеллагры включает следующие симптомы: (3 Д)
дерматит, диарея, димменция.
Кроме того: вялость, апатия, слабость в ногах, быстрая утомляемость, головокружение, раздражительность, бессонница, сердцебиение, цианоз губ, щек, рта и кистей рук, бледность и сухость кожи, снижение аппетита, падение веса, понижение сопротивляемости организма к инфекциям и понижение трудоспособности.

Участие витамина РР в обмене
Окислительно-восстановительные функции:
При участии никотинамидных коферментов специфические дегидрогеназы катализируют обратимые реакции дегидрирования спиртов, оксикислот, аминокислот в соответствующие альдегиды, кетоны и кетокислоты.
Наиболее важная биологическая функция никотинамидных коферментов состоит в их участии в переносе электронов и протонов от субстратов к кислороду в процессе клеточного дыхания.
а) Углеводный обмен ( 2 реакции в гликлизе) :
-- гликолитическая оксидоредукция
-- ЛДГ- реакция
-- в цикле Кребса - 3 реакции
-- в пентозном цикле ( 2 реакции)
б) липидный обмен:
-- б - окисление жирных кислот
-- синтез холистерина
в) белковый обмен
-- прямое окислительное дезаминирование глутаминовой
Распространение никотинамида
Из растительных продуктов - оболочка злаков
в грече, пшене, ячневой , овсяной и перловой крупах, а также в рисе
в бобовых: зеленый горошек, чечевица, фасоль, соя. в арахисе
в шпинате, томате, капусте, брюкве, баклажанах В картофеле
В красной свекле в свежих грибах
Из животных продуктов: мясо, печень , почки , сердце , рыба
В животных организмах витамин РР может синтезироваться из триптофана (слабо).
Суточная потребность витамина РР составляет 15-25 мг
