
- •Кафедра Общей Химической Технологии
- •Исходное сырье
- •Серный колчедан
- •С флотацияерный
- •Отходящие газы
- •Характеристика целевого продукта
- •Физико-химичекое обоснование основных процессов производства целевого продукта и экологической безопастности производства
- •Контактный метод получения серной кислоты
- •Получение обжигового газа из серы
- •Получение обжигового газа из колчедана
- •Подготовка обжигового газа к контактному окислению
- •Контактное окисление диоксида серы
- •Абсорбция триоксида серы
- •Описание схемы
- •Расчет материального баланса хтс Структурная блок-схема
- •Составление системы уравнений материального баланса.
- •Исходные данные для расчета
- •Соответствие переменных потока
- •Материальный баланс хтс
- •Поточная диаграмма
- •Расчет основных технологических показателей процесса
- •Заключение
- •Список используемой литературы
Описание схемы
Исходная сера поступает в плавитель, где плавясь нагревается до температуры 1200С и уже в виде жидкости поступает в печь циклонного типа 1 и нагревается до температуры 13000С, затем в котел-утилизатор 2, поступает сверху в пятислойный контактный аппарат 7 с температурой 4400С и концентрацией SO2 10%.
В трех верхних слоях катализатора происходит окисление диоксида серы примерно на 60 % в каждом и адиабатическое повышение температуры. Охлаждением газа в теплообменниках между полками достигается ступенчатое приближение к оптимальной кривой. На выходе из третьего слоя достигается степень превращения SO2 в SO3 на 93 – 95 %, при этом адиабата приближается к равновесной кривой и скорость реакции сильно уменьшается
Воздух осушается в сушильной башне 9, орошаемый 98%-ной кислотой. После подогрева в теплообменниках 8б и 8в в межтрубном пространстве направляется в печь 1.
Газ после первого слоя теплообменника 8а по трубам снова возвращается в контактный аппарат. После 2-го слоя газ поступает в теплообменник 8г по трубам и снова возвращается в контактный аппарат 7. После 3-го слоя газ поступает на абсорбцию по трубам теплообменников 8д, 8б, 8в в первый моногидратный абсорбер 10. После абсорбции газ выходит сверху и через теплообменники 8д, 8б, 8в направляется на 4-й слой контактного аппарата 7, где содержащийся в газе диоксид серы (около 0,5 %) окисляется на 90 – 95 %. Перед 4-ым слоем вводится дополнительное количество воздуха. После 5-го слоя (где селективность процесса составляет 99,5 % и выше) газ используется для подогрева воды в экономайзере 3 и уже оттуда направляется во второй моногидратный абсорбер 11, где происходит окончательное поглощение и выдача 93% H2SO4.
Расчет материального баланса хтс Структурная блок-схема



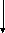


 O2+N2
H2O
O2+N2
H2O
011 03
 S
SO2+O2+N2
SO3+
SO2+O2+N2
H2SO4+H2O
S
SO2+O2+N2
SO3+
SO2+O2+N2
H2SO4+H2O

 1
2
3
1
2
3
 012
12 23
301
012
12 23
301
10 302
S SO3+ SO2+O2+N2
1 - (серная печь) сжигание серы
S + O2= SO2
2 – (контактный аппарат) контактное окисление
2SO2+ O2 = 2SO3
3 – (абсорбер) абсорбция SO3
SO3 + H2O = H2SO4
Составление системы уравнений материального баланса.
По 1-му блоку: по сере
![]()
По 2-му блоку
![]()

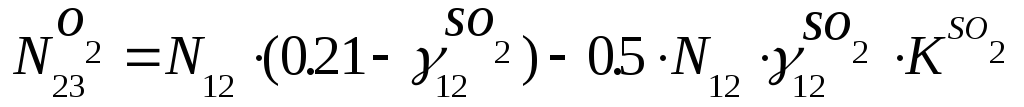
По 3-му блоку
![]()
Исходные данные для расчета
|
Показатель |
Условные обозначения |
Единица измерения |
Значение |
|
Степень превращения серы в SO2. |
КS |
% |
95,0 |
|
Степень превращения SO2 в SO3. |
КSO2 |
% |
99,7 |
|
Степень абсорбции SO3 |
КSO3 |
% |
99,9 |
|
Содержание SO2 в газе, поступающем в контактный аппарат. |
|
% (по объему) |
9,0 |
|
Содержание H2SO4 в целевом продукте |
|
% (по массе) |
92,8 |
|
Базис расчета, количество H2SO4 в продукте |
|
кг |
5000 |
Перепишу систему уравнений с учетом данных и обозначив неизвестные за Хi:
Х1 ∙ 0,95 / 32 = Х2 ∙ 0,09
Х3= Х2∙ 0,09 ∙ 0,997
Х4 = Х2 ∙ (1-0,997) ∙ 0,09
Х5 = Х2 ∙ (0,21 – 0,09) – 0,5 ∙ Х2 ∙ 0,09 ∙ 0,997
98 ∙ 0,999 ∙ Х3 = 5000 ∙ 0,928
Х6 = Х3 ∙ 0,999 ∙ 18 + 5000 ∙ (1 – 0,928)
Х7 = Х3 ∙ 80 ∙ (1 – 0,999) + Х4 ∙ 64 + Х5 ∙ 32 + 0,79 ∙ Х2 ∙ 28
Решение системы уравнений:
Х3 = 5000 ∙ 0,928 / 98 ∙ 0,999 = 47,4
Х2= 47,4 / 0,09 ∙ 0,997 = 528,3
Х1 = 528,3 ∙ 0,09 ∙ 32 / 0,95 = 1601,6
Х4 = 528,3 ∙ (1-0,997) ∙ 0,09 = 0,14
Х5 = 528,3 ∙ (0,21 – 0,09) – 0,5 ∙ 528,3 ∙ 0,09 ∙ 0,997 = 39,7
Х6 = 47,4 ∙ 0,999 ∙ 18 + 5000 ∙ (1 – 0,928) = 1212,3
Х7 = 47,4 ∙ 80 ∙ (1 – 0,999) + 0,14 ∙ 64 + 39,7 ∙ 32 + 0,79 ∙ 528,3 ∙ 28 = 12969,1
