Биоэнергетический
обмен. Общие пути метаболизма. Биологическое
окисление.
-
Понятие об обмене веществ.
Процессы ката- и анаболизма, их
характеристика, отличия и взаимосвязь
|
Обмен веществ –
совокупность процессов превращения
веществ и энергии в организме и обмен
веществами и энергией между организмом
и окружающей средой.
Включает 3 этапа:
-
Поступление
-
Метаболизм
-
Выделение конечных
продуктов из организма
Метаболизм:
|
Катаболизм
|
Анаболизм
|
|
Распад ВМС до мономеров с
выделением энергии АТФ и НАДН2
|
Синтез макромолекул с
затратой энергии
|
Отличаются
по:
-
Локализации
-
Количеству
реакций
-
Локализации
Взаимосвязь
катаболизма и анаболизма основывается
на единстве биохимических превращений,
обеспечивающих энергией все процессы
жизнедеятельности и постоянное
обновление тканей организма.
Процессы
анаболизма и катаболизма находятся
в организме в состоянии динамического
равновесия или временного
превалирования одного из них.
|
Преобладание анаболических
процессов
|
катаболических
|
|
приводит к росту, накоплению
массы тканей
|
к частичному разрушению
тканевых структур, выделению энергии
|
Состояние
равновесного или неравновесного
соотношения зависит от возраста:
|
В детском возрасте
|
У взрослых людей
|
в старческом
|
|
Преобладает анаболизм
|
находятся в равновесии
|
катаболизм
|
Их соотношение
зависит также от состояния здоровья,
физической или психоэмоциональной
деятельности.
|
-
Метаболические
пути, их виды
|
Общий
путь катаболизма – реакция
окислительного декарбоксилирования
ПВК и цикла Кребса.
Метаболические
пути:
|
Главные
|
Добавочные
|
Побочные
|
|
Универсальны
Поставляют
энергию
Синтез основных биополимеров
клетки
|
Менее
универсальны
Синтез
важных веществ
Энергия
НАДФН2
В определенных тканях
|
Пути
происходят при патологии
В норме иногда
|
Пример1:
|
Глюкоза
|
|
Главный
|
Добавочный
|
Побочный
|
|
Дихотомический
(аэробный) распад:
38АТФ из 1 глюкозы
|
Пентозный
цикл: В эритроцитах,
эндокринных железах, печени (т.е. в
определенных тканях)
Синтез пентоз, Энергия
НАДФН2
|
Лактоза (пример нормы)
|
Пример2:
|
Фенилаланин
|
|
Главный
|
Добавочный
|
Побочный
|
|
Биосинтез белка
|
Синтез тироксина (только
в щитовидной железе)
|
ФенилПВК (токсичное
соединение)
|
|
-
Основные
фазы унификации питательных веществ
в организме. Центральные метаболиты
|
Фазы:
-
Подготовительная
– не является поставщиком энергии
(1%).
ВМС распадаются в ЖКТ до мономеров.
-
Образование
центральных метаболитов –
протекает в цитоплазме, завершается
в митохондриях (20-30% энергии)
-
Полное
окисление – Цикл Кребса (70-80%
энергии) – в аэробных условиях полное
окисление поступивших с пищей веществ.
|
-
Цикл
Кребса, как основной «метаболический
котел» клетки (формулы). Регуляция и
локализация цикла Кребса
|
Цикл Кребса
(ЦТК, цикл трикарбоновых кислот,
лимоннокислый цикл)
Циклический,
в аэробных условиях, в матриксе
митохондрий
Реакции:
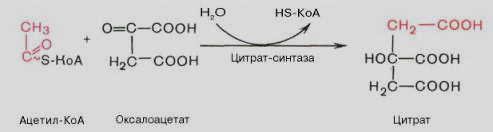
-
Цитрат-синтетазная
(цитрат-синтетаза:
класс 4 – лиазы)
|
-
Изомеризация
цитрата

|
-
Изоцитрат-дегидрогеназная
(класс
1 – оксидоредуктазы)

Кофактор: С, Мg2+
Кофермент: НАД, НАДФ
|
-
Окислительное
декарбоксилирование
α-кетоглутаровой
кислоты

Кофактор: Мg2+
Коферменты(5): ТПФ, HS-KoA, ФАД, НАД+,
амид липоевой кислоты
|
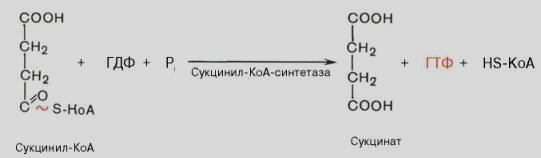
-
Реакция
субстратного фосфорилирования (за
счет энергии субстрата)
|
-
Сукцинат-дегидрогеназная

(встроена в мембрану
митохондрии)
Кофермент: ФАД
|
-
Фумаразная
реакция (класс
– гидролазы)

|
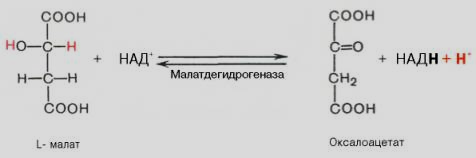
-
Малат-дегидрогеназная
|
 
При окислении
1 молекулы Ацетил-КОА в цикле Кребса
и в системе окислительного фосфорилирования
образуется 12АТФ:
1АТФ –
субстратное фосфорилирование, 11АТФ
– окислительное
СН3СоSКоА
+ 2Н2О + 3НАД + ФАД + АДФ + Рн
= > 2СО2 + 3НАДН2 + АТФ + ФАДН2
+ НSКоА
Функции
ЦТК (Цикла Кребса):
-
Интегрирующая
(взаимосвязь БЖУ)
-
Энергообразующая
(12АТФ)
-
Анаболитическая
(синтез соединений из метаболитов
ЦТК)
Пример:
|
сукцинилКОА
|
Оксало-ацетат
|
α-кетоглутарат
|
|
Синтез гема
|
Глюкоза
|
глу
|
Регуляция
цикла.
-
Регуляторные
энзимы:
-
Роль
витаминов:
|
Витамин
|
Рибофлавин (В2)
|
РР
|
Тиамин (В1)
|
Пантотеновая кислота
|
|
В составе кофермента
|
ФАД
|
НАД
|
ТПФ
|
КоА
|
|
Кофермент реакции
|
СДГ, α-кетоглутарат-ДГ комплекс
|
МДГ, ИДГ, α-кетоглутаратДГ
|
α-кетоглутаратДГ
|
ацетилКоА, сукцинилКоА
|
|
-
Понятие
о биологическом окислении, его отличие
от горения
|
Биологическое
окисление – совокупность реакций
окисления субстратов в живых клетках.
Главные
функции окислительных процессов:
-
Запас
энергии в утилизируемой форме
-
Рассеяние
энергии в виде теплоты
-
Образование
полезных соединений
-
Расщепление
вредных веществ
Отличие БО
от горения:
|
БО
|
Горение
|
|
Не является одноступенчатой
реакцией
|
Одноступенчатая реакция
|
|
Ферментативный процесс
|
|
|
Только в мягких условиях
|
|
|
Освобождение энергии за
счет восстановления водорода + Н2О
|
Освобождение
энергии за счет
С => СО2
|
|
Часть
энергии переходит в тепло,
Часть - в энергию
макроэргических связей АТФ
|
Вся энергия переходит в
тепловую
|
|
Окисление в основном
частичное
|
Окисление полное
|
Сущность
окисления:
Fe3+
+ электрон ↔ Fe2+
|
Fe3+
|
Fe2+
|
|
Окислитель, акцептор,
антиоксидант
|
Восстановитель, донор,
прооксидант
|
Каждая
редокс-пара – имеет свой потенциал.
Редокс-потенциал
указывает направление движения
электронов
|
-
Тканевое
дыхание. Субстраты тканевого дыхания
|
Тканевое
дыхание– вид биологического
окисления, при котором акцептором
электронов.
Субстраты
ТД:
(коферменты
реакций НАД,ФАД: изоцитрат, α-кетоглутарат,
сукцинат, малат)
-
ПВК
-
Лактат
-
АК
-
α-глицерофосфат
-
жирные
кислоты
Осуществляется
благодаря оксидоредуктазам дыхательной
цепи.
|
-
Дыхательная
цепь, ее структура, локализация,
биологическая роль
|
Дыхательная
цепь – последовательность
оксидоредуктаз во внутренней мембране
митохондрий, осуществляющих перенос
электронов и протонов от субстрата
на молекулярный кислород.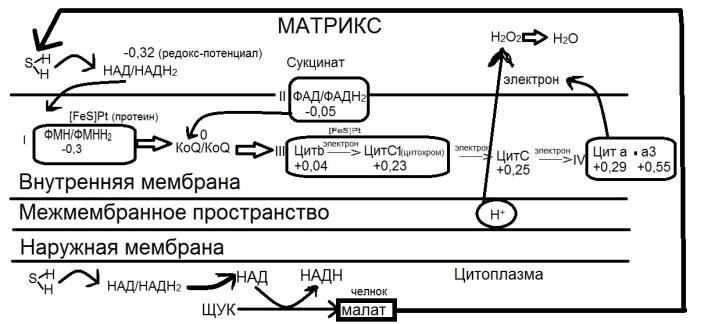
Функции:
-
Поставщик
энергии для синтеза АТФ
-
50%
энергии – выделяется в виде тепла
Поступление
водорода в виде НАДН2 либо ФАДН2
|
-
Характеристика
ферментных комплексов дыхательной
цепи
|
Комплексы
ДЦ:
|
Комплекс
|
Функция
|
Состав
|
Реакция
|
-
НАДН-КоQ-редуктаза
|
Перенос электронов от НАДН
к KoQ
|
Белки и липиды негемовые
[FeS]Pt,
НАДН-ДГ (является
флавопротеином => в составе кофермента
ФМН)
|
ФМН+НАДН2=>ДМНН2+НАД
(димононуклеотидаш2)
|
-
Сукцинат-KoQ-редуктаза
|
Перенос электронов от
сукцината к KoQ
|
СДГ (кофермент
ФАД), негемое железо, липиды и
белки КоQ
(убихинон): Источники – витамин К и
Е (антиоксиданты)
Убихинон
коллектор (собирает на себя электроны
и протоны)
|
КоQ+ФМНН2=>КоQН2+ФМН
|
-
КоQН2-цитС-редуктаза
|
Катализирует перенос
электронов от КоQH2
к цитС
|
цитВ, цитС,
негемовое железо, липиды и белки
В
центре цитохрома железо, которое
меняет валентность (редокс-пара)
|
|
-
Цитохром-оксидаза
|
Катализирует перенос
электронов от цитС к О2
|
Цит а, цит а3, негемовое
железо, липиды и белки
|
Отличия от других:
аутокситабельность (перенос электронов
на О2), наряду с Fe
есть Cu
|
|
-
Использование
цитоплазматического НАДН2 в дыхательной
цепи. Характеристика челночных
механизмов
|
Челночные
механизмы – переносят восстановленные
нуклеотиды (НАДН2) из цитоплазмы
в митохондрии.
Челнок –
малат.
В цитоплазме
происходит восстановление оксоло-ацетата
до малата, который проникает в
митохондрию.
В митохондрии
по действием митохондриальной МДТ
малат переходит в ЩУК, а НАДН2
передает электроны и протоны дыхательной
цепи.
|
-
Ингибиторы
тканевого дыхания
|
Ингибиторы:
Барбитураты
– блокируют переход электронов от
первого комплекса к убихинону.
Ряд
антибиотиков блокирует переход
электронов от цитохромаВ к цитохромуС
(комплекс3).
Цианиды,
угарный газ – ингибиторы цитохромоксидазы
(комплекс4)
Цианиды –
ингибиторы Fe2+
Угарный
газ - ингибитор Fe3+
|
-
Окислительное фосфорилирование,
его механизм и значение
|
Фосфорилирование
– образование АТФ из АДФ и неорганического
фосфата за счет энергии.
Различают 2 вида (в
зависимости от вида энергии):
|
Окислительное фосфорилирование
|
Субстратное фосфорилирование
|
|
Энергия дыхательной цепи
(тканевого дыхания)
|
Энергия субстрата
|
Для
образования 1 молекулы АТФ необходимо:
Р/О
(фосфор/кислород) – коэффициент
фосфорилирования – число моль
неорганического фосфата переведенных
в органическую форму (АТФ) в расчете
на каждый поглощенный атом кислорода.
Механизмы
окислительного фосфорилирования (ОФ)
Основные
положения ОФ:
-
движущей
силой ОФ является протонный
градиент ∆
μН+ /дельта
мю аш/
Электроны,
пробегая по ДЦ, каскадно дробно теряют
энергию.
За счет
этой энергии против градиента
концентрации происходит перемещение
протонов через мембрану (4Н+
на уровне 1го, 4Н+
на уровне
3го, 2Н+
на уровне 4го) из матрикса.
|
Заряд с одной стороны мембраны
|
отрицательный
|
положительный
|
|
Среда с одной стороны мембраны
|
щелочная
|
кислая
|
∆
μН+=∆ᴪ
+∆рН+
∆ᴪ
- мембранный потенциал, ∆рН
– градиент рН
Протоны в
дальнейшем возвращаются в матрикс
митохондрий по градиенту концентрации
по каналу, образованному белком-ферментом
АТФ-синтазой, которая состоит из 2х
компонентов F0F1
При этом
выделяется энергия для синтеза АТФ
-
ОФ
требует целостности мембраны
(внутренней митохондриальной)
-
Внутренняя
мембрана митохондрий не проницаема
для ионов (Н+,К+…)
|
-
Сопряжение
тканевого дыхания и окислительного
фосфорилирования
|
Для
образования 1 молекулы АТФ
необходимо:
Пункты
фосфорилирования (точки сопряжения)
В дыхательной
цепи – 3 участка (с перепадом в 0,2В):
На уровне
1,3,4 ферментного комплекса.
2й ферментный
комплекс не задействован.
Вывод:
-
Тканевое
дыхание заряжает мембрану, ОФ разряжает
мембрану
-
Энергопреобразующие
мембраны сначала генерируют ∆
μН+, а затем реализуют
его через АТФ-синтазу
АТФ-синтаза
(похож на гриб)
|
«Шляпка гриба»
|
«Ножка гриба»
|
|
Фермент АТФ-аза (F1),
состоит из 9 субъединиц
|
F0
– канал, встроенный в мембрану, по
которому пробегают протоны.
«О» - олиголизин,
ингибитор фермента
|
|
-
Регуляция
окислительноего фосфорилирования
(дыхательный контроль, действие
разобщителей)
|
Уровни
регуляции:
-
Дыхательный
контроль
– изменение
скорости дыхания с изменением
концентрации АДФ.
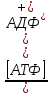 При
повышении концентрации АДФ =>
активизируется ЦТК, ДЦ, ОФ При
повышении концентрации АДФ =>
активизируется ЦТК, ДЦ, ОФ
При снижении
концентрации АДФ => тормозится ЦТК,
ДЦ, ОФ
-
Разобщители
– разобщают
перенос электронов и синтез АТФ.
Разобщают
тканевое дыхание (ТД) и ДЦ.
ДЦ работает,
но энергия ТД идет на тепло, а не на
АТФ.
Примеры
разобщителей:
-
Естественной
природы (прогестерон, тестостерон,
холод)
-
Патологические
(дифтерийный токсин)
-
Искусственные
(ряд антибиотиков)
|
-
Свободное
окисление. Бурый жир
|
Свободное
(нефосфорилирующее) окисление
В митохондриях
дыхание не всегда сопровождается
фосфорилированием.
Бурый жир
– термогенная ткань.
У человека
бурый жир находится у ключиц и вдоль
позвоночника.
Бурый –
т.к. содержит много цитохромов (а в них
Fe), а так же много
митохондрий, кровеносных сосудов,
симпатических нервных волокон.
Внутренняя
мембрана митохондрий бурого жира
имеет специальные поры для ионов Н+.
В них белок термогенин (из гема).
Термогенин
встроен в мембрану. Он разобщающий
белок.
|
-
Субстратное
фосфорилирование, его отличие от
окислительного фосфорилирования
|
Субстратное
фосфорилирование (СФ) – образование
АТФ за счет превращения субстрата,
имеющего макроэргическую связь.
Пример1:
(реакция №5 из ЦТК)
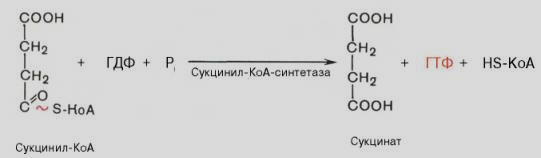
Реакция
проходит в митохондриях в аэробных
условиях.
ГТФ –
образуется за счет субстрата
Пример2:
пируват-киназная реакция (из гликолиза)
Отличия
ОФ от СФ:
|
Окислительное
фосфорилирование
|
Субстратное
фосфорилирование
|
|
За счет энергии окисления
(электроны в ДЦ)
|
За счет энергии субстрата
|
|
В митохондриях
|
В митохондриях и в цитоплазме
|
|
Главный генератор энергии
|
Дополнительный (но может
стать главным при нехватке кислорода)
|
|
Аэробный процесс
|
Аэробный, анаэробный
|
|
Зависит от разобщителей
|
Не зависит от разобщителей
|
|
-
Пути
образования свободных радикалов,
микросомальное окисление. Биологические
эффекты свободных радикалов
|
Использование
кислорода в организме:
-
80-90%
расходуется в ДЦ
-
В цепи
микросомального окисления
-
Реакции
катализируемые: оксигеназами (моно-
и диоксигеназами)
Свободно-радикальное
окисление.
Свободный
радикал – молекула с неспаренным
электроном на орбите.
Свободно-радикальное
окисление – универсальный процесс,
сопровождающий нормальную
жизнедеятельность и активизирующийся
при патологии.
Свободный
радикал образуется в организме:
-
В ДЦ
(при образовании эндогенной воды на
уровне убихинона)
-
При
фагоцитозе
-
При
микросомальном оксилении
-
При
синтезе ряда гормонов
Активные
формы кислорода:
Образование
активных форм кислорода:
-
О2 +
электрон => супероксид радикал (Ȱ2)
-
Супероксид
радикал + электрон + 2Н+ =>
вода
-
Вода +
электрон + Н+ => вода + гидроксил
радикал (ȮН)
-
Гидроксил
радикал + электрон + Н+ => вода
Пути
образовании супероксид радикала:
|
Ферментативный
|
Неферментативный
|
Под влиянием УФ-излучения
|
|
Ксантин-оксидазная реакция
|
Образование адреналина
|
|
Перекись
водорода – цитотоксична
Пути
образования:
|
Ферментативный
|
Неферментативный
|
|
В митохондриях:
СОД-фермент
В пероксисомах: уратоксидаза
|
|
Образование
гидроксил радикала:
Н2О2
+ супероксид радикал (Ȱ2) =>
гидроксил радикал (ȮН) + ОН-+ О2
Образуется
при облучениях.
Активные
формы кислорода:
ПОЛ
необходим для синтеза простагландинов,
лейкотриенов,…
ПОЛ:
повреждаются полиненасыщенные жирные
кислоты фосфолипидов мембран
RH
(жирная кислота) => R∙
=> ROO∙ (пероксидный
радикал) => ROOH
(гидропероксид)
ROOH
=> RO∙ + ȮН (гидроксил
радикал – самый страшный)
В результате
избыточного ПОЛ образуются:
Активация
ПОЛ (и др окислителей) – при многих
радикальных окислениях:
-
Лучевые
поражения
-
Опухоли
-
Гипоксия
-
Ишемия
-
Старение
|
-
Антиоксидантная
система организма. Ферменты –
антиоксиданты. Неферментативные
антиоксиданты
|
Антиоксидантная
система – система защиты биополимеров
от деструкции
|
Ферментативные антиоксиданты
|
Неферементативные
|
|
Богаты эритроциты
Н2О2 +
АН2 => (пероксидаза)
=> 2Н2О + А
АН2 – донор
протонов
Богаты эритроциты
Ȱ2 (супероксид
радикал)+
Ȱ2 + 2Н+ => (сод)
=> Н2О2 + О2
Сu и
Zn – кофакторы СОД
Лечение ожогов глаз
Н2О2 +
2GSH(восстановленный)=>
(глутатион-пероксидаза)
=> 2Н2О + GSSG
(окисленный)
(он
работает при малых концентрациях,
при больших вкл остальные)
GSH
– в активном центре содержит Se
-
Глутатион-редуктаза
-
Церулло-плазмин
Главный антиоксидант
плазмы крови
Кроме АО, еще и фермент (Fe2+=>
Fe3+
-антиоксидант)
|
(С, α-токоферол,
β-каротин, К, Р)
(церуло-плазмин,
лактоферрин, трансферрин, альбумин)
(Se,
Zn)
(эстроген, тироксин)
(серотонин)
-
АК (ароматические)
-
Пигмент меланин
-
Убихинон
-
Глутатион
|
Антиоксиданты
могут быть:
|
Внутриклеточные
|
Мембранные (α-токоферол)
|
Во внеклеточных жидкостях
|
Антиоксиданты
могут быть:
|
Первичные
|
Вторичные
|
Третичные
|
|
Предупреждают образование
свободных радикалов (СОД)
|
Удаляют уже образованные
(витамины)
|
ДНК-репарирующие
ферменты
Восстанавливающие
поврежденные ДНК структуры
|
|















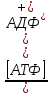 При
повышении концентрации АДФ =>
активизируется ЦТК, ДЦ, ОФ
При
повышении концентрации АДФ =>
активизируется ЦТК, ДЦ, ОФ