
- •Лабораторные работы
- •Техника безопасности при работе в химической лаборатории
- •1. Порядок работы в лаборатории
- •2. Обязательные требования к технике безопасности при работе студентов в химической лаборатории
- •3. Правила оказания первой медицинской помощи
- •Лабораторная работа № 1 химическая посуда и обращение с нею
- •Лабораторная работа № 2 лабораторные нагревательные приборы
- •Лабораторная работа № 3 весы. Взвешивание
- •Лабораторная работа № 4 фильтрование
- •Качественные реакции на катионы и анионы
- •Лабораторная работа № 5 общие приемы работы с газами
- •Лабораторная работа № 6 получение оксидов, кислот, оснований, солей
- •Лабораторная работа № 7 определение относительной молекулярной массы оксида углерода(IV)
- •Лабораторная работа № 8 приготовление раствора хлорида натрия заданной концентрации по навеске
- •Пример расчета и методика приготовления раствора
- •2 % -------------------- 0,019 Г/мл.
- •Лабораторная работа № 9
- •Приготовление раствора
- •Хлорида натрия заданной концентрации
- •Смешением из двух растворов
- •4,5% 1 М.Ч.
- •7,5 % 2 М.Ч.
- •2,0 % ------------------ 0,019 Г/мл
- •Лабораторная работа № 10 электролитическая диссоциация
- •Лабораторная работа № 11 реакции в растворах электролитов. Произведение растворимости
- •Лабораторная работа № 12 ионное произведение воды. Водородный показатель. Гидролиз солей
- •Лабораторная работа № 13 химическая кинетика. Химическое равновесие
- •Лабораторная работа № 14 окислительно-восстановительные реакции
4,5% 1 М.Ч.
6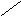 ,5
%
,5
%
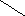
7,5 % 2 М.Ч.
Масса 4,5 %-го раствора относится к массе 7,5 %-го раствора как 1 : 2. На массу 6,5 %-го раствора приходятся 3 массовые части.
m4,5% - 1 м.ч.
m6,5% - 3 м.ч.
![]()
![]()
m7,5%= 105,80 – 35,27 = 70,53 г.
5. Определить объемы исходных растворов:
![]()
![]()
6. Приготовить 6,5 %-й раствор в колбе сливанием рассчитанных объемов исходных растворов. Объемы растворов измерить с помощью цилиндра с точностью до 0,5 мл. Раствор перемещать стеклянной палочкой.
7. Подобрать соответствующий ареометр и измерить плотность полученного раствора.
Предположим, что рэксп = 1,058 г/мл.
8. По измеренной плотности определить концентрацию полученного раствора ωэксп, используя метод интерполяции:
2,0 % ------------------ 0,019 Г/мл
х % ------------------- 0,005 г/мл (ρэксп - р6,0 %),
![]()
ωэксп = 6,0 + 0,53 = 6,53 %.
9. Рассчитать абсолютную (∆) и относительную (δ) погрешности измерения:
∆ = |6,53 - 6,5| = 0,03 %.
![]()
Вывод: определили концентрацию полученного раствора. Она равна 6,53 %. Относительная ошибка эксперимента равна 0,46 %.
Контрольные вопросы и задания: получите у преподавателя индивидуальное задание и приготовьте раствор хлорида натрия заданной концентрации смешением двух растворов с различной массовой долей растворенного вещества в них. Рассчитайте абсолютную (∆) и относительную (δ) погрешности эксперимента.
Контрольные вопросы:
1. Какая масса 20 %-ного раствора соляной кислоты потребуется для нейтрализации 45 г 15 %-ного раствора гидроксида натрия?
2. В каком соотношении по объему смешали 4,2 % раствор гидроксида натрия (плотность 1,045 г/мл) и раствор того же вещества с концентрацией 6,12 моль/л (плотность 1,22), если при этом получился 10,1% раствор.
3. Какой объем раствора уксусной кислоты с молярной концентрацией 1,98 моль/л (плотность 1,015 г/мл) был добавлен к 10 мл 40,2% раствора того же вещества (плотность 1,05 г/мл), если при этом получился 27,2% раствор (плотность 1,035 г/мл).
4. 1 мл 25% раствора содержит 0,458 г растворенного вещества. Какова плотность этого раствора?
5. Масса соли, которая вводится в организм при вливании 353 г физиологического раствора, содержащего 0,85% по массе поваренной соли, равна?
6. Массовая доля нитрата серебра в насыщенном при 20 оС водном растворе равна 69,5%. Вычислите массу этой соли, которая растворится в 100 г воды при этой же температуре?
7. Какую массу воды надо испарить из 1200 г 20% раствора вещества, чтобы увеличить массовую долю в 1,5 раза?
8. Какую массу квасцов КAl(SO4)2 ∙12H2O необходимо добавить к 500 г 6% раствора сульфата калия, чтобы массовая доля последнего увеличилась вдвое? Найдите объем газа (при н. у.), который выделится при действии на полученный раствор избытка сульфида калия.
9. При поглощении оксида серы(VI) 55,6 мл раствора серной кислоты (массовая доля кислоты 91%, плотность раствора 1,8 г/мл) массовая доля кислоты в образовавшемся растворе составила 96,3%. Определите массу поглощенного оксида серы(VI).
10. Из 300 г насыщенного при 40 оС раствора хлорида цинка (растворимость 452,5 г в 100 г воды) при охлаждении до 0 оС выпало 254 г кристаллогидрата, а массовая доля соли в растворе снизилась до 73,1%. Установите формулу кристаллогидрата?
