
- •Лабораторные работы
- •Техника безопасности при работе в химической лаборатории
- •1. Порядок работы в лаборатории
- •2. Обязательные требования к технике безопасности при работе студентов в химической лаборатории
- •3. Правила оказания первой медицинской помощи
- •Лабораторная работа № 1 химическая посуда и обращение с нею
- •Лабораторная работа № 2 лабораторные нагревательные приборы
- •Лабораторная работа № 3 весы. Взвешивание
- •Лабораторная работа № 4 фильтрование
- •Качественные реакции на катионы и анионы
- •Лабораторная работа № 5 общие приемы работы с газами
- •Лабораторная работа № 6 получение оксидов, кислот, оснований, солей
- •Лабораторная работа № 7 определение относительной молекулярной массы оксида углерода(IV)
- •Лабораторная работа № 8 приготовление раствора хлорида натрия заданной концентрации по навеске
- •Пример расчета и методика приготовления раствора
- •2 % -------------------- 0,019 Г/мл.
- •Лабораторная работа № 9
- •Приготовление раствора
- •Хлорида натрия заданной концентрации
- •Смешением из двух растворов
- •4,5% 1 М.Ч.
- •7,5 % 2 М.Ч.
- •2,0 % ------------------ 0,019 Г/мл
- •Лабораторная работа № 10 электролитическая диссоциация
- •Лабораторная работа № 11 реакции в растворах электролитов. Произведение растворимости
- •Лабораторная работа № 12 ионное произведение воды. Водородный показатель. Гидролиз солей
- •Лабораторная работа № 13 химическая кинетика. Химическое равновесие
- •Лабораторная работа № 14 окислительно-восстановительные реакции
Лабораторная работа № 8 приготовление раствора хлорида натрия заданной концентрации по навеске
Цель работы: экспериментально применить знания теоретического материала по теме «Растворы неэлектролитов»; отработать умение приготовления растворов с заданной массовой долей вещества в растворе из твердого вещества и воды.
Реактивы и материалы: хлорид натрия твердый, дистиллированная вода.
Оборудование: технохимические весы с набором разновесов, набор ареометров, цилиндр высокий узкий, мерная колба на 100 мл, химические стаканы, колбы, воронки стеклянные, шпатели.
Техника безопасности: соблюдать основные правила работы в химической лаборатории.
Пример расчета и методика приготовления раствора
Задание: Приготовить 100 мл 6,5 %-го раствора хлорида бария.
По табл. 1 рассчитать плотность 6,5 %-ного раствора хлорида бария.
Таблица 1
Зависимость плотности раствора от массовой доли растворенного вещества
|
ω,%
|
ρ, г/мл |
ω, %
|
ρ, г/мл | ||
|
ВаСl2 |
NaCl |
ВаСl2 |
NaCl | ||
|
2.0 |
1.016 |
1.013 |
12.0 |
1.113 |
1.086 |
|
4.0 |
1.034 |
1.027 |
14.0 |
1.134 |
1.101 |
|
6.0 |
1.053 |
1.041 |
16.0 |
1.156 |
1.116 |
|
8.0 |
1.072 |
1.056 |
18.0 |
1.179 |
1.132 |
|
10.0 |
1.092 |
1.071 |
20.0 |
1.203 |
1.148 |
Плотности 6,5 %-ного раствора хлорида бария можно рассчитать методом интерполяции, предполагая, что зависимость плотности от концентрации в узком интервале линейная. Массовая доля 6,5 % находится между 6,0 % и 8,0% следовательно плотность 6,5 %-ного раствора находится между значениями 1,053 и 1,072 г/мл. Концентрация 6,5% больше, чем 6,0% на 0,5 %. При увеличений концентрации на 2 % от 6,0 % до 8,0 % плотность увеличивается от 1,053 до 1,072. Пропорцией можно определить, на сколько г/мл плотность 6,5 %-ного раствора больше, чем плотность 6 % - ного раствора (х).
при изменении концентрации раствора на 2 % плотность изменяется на 0,019 г/мл (1,072-1,053)
при изменении концентрации раствора на 0,5 % плотность изменяется на х г/мл
х = 0,005 г/мл.
Плотность 6,5 %-ного раствора равна: сумме 6,0 %-ного раствора и х.
ρ6,5% = ρ6% + ρ0,5% = 1,053 + 0,005 = 1,058 г/мл.
2. Рассчитать массу заданного раствора:
mp-pa= V ∙ p = 100 ∙ 1,058 = 105,80 г.
3. Рассчитать массу растворенного вещества:
m(ВаС12) = mр-ра ∙ ω = 105,80 ∙ 0,065 = 6,88 г.
4. На технохимических весах взвесить 6,88 г ВаС12.
5. С помощью стеклянной воронки перенести соль в мерную колбу на 100 мл, смыть дистиллированной водой остатки соли с воронки и довести объем до метки. Закрыть колбу пробкой и перемешать раствор, переворачивая колбу до исчезновения кристаллов соли.
6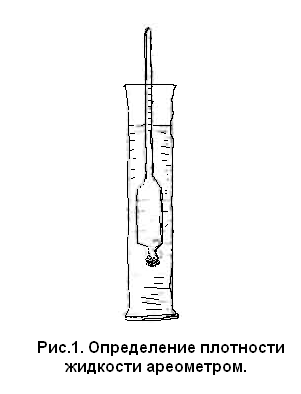 .
С помощью ареометра измерить плотность
полученного раствора (рис. 1). Для этого
перелить раствор в цилиндр, подобрать
ареометр по плотности раствора. Измерение
плотности проводить под руководством
преподавателя. Предположим, что плотность
полученного раствора ρэксп
= 1,059 г/мл.
.
С помощью ареометра измерить плотность
полученного раствора (рис. 1). Для этого
перелить раствор в цилиндр, подобрать
ареометр по плотности раствора. Измерение
плотности проводить под руководством
преподавателя. Предположим, что плотность
полученного раствора ρэксп
= 1,059 г/мл.
7. Определить концентрацию полученного раствора ωэксп, используя метод интерполяции (см. п. 1).
