
- •Содержание.
- •1. Устройства отображения на электролюминесцентных и вакуумных люминесцентных приборах.
- •2. Светодиодные уо.
- •2.2. Индикаторы на светодиодах.
- •3. Устройства отображения на жидких кристаллах.
- •4. Лазерные и голографические индикаторы.
- •4.2.1.Основные сведения о голографии.
- •5. Устройства отображения на лампах накаливания.
- •6. Устройства отображения на газоразрядных приборах.
- •Τз.Ср., мкс
- •100 150 200 250 300 Uз , в
- •7. Электрохимические уо.
- •8. Новые технологии и разработки. Перспективы развития сои.
- •9. Вопросы проектирования сои.
- •9.4. Оценка проектируемой системы на отдельных этапах разработки.
- •10. Математическое обеспечение средств отображения информации.
- •10.1. Общее математическое обеспечение комплексов.
- •10.2. Специальное математическое обеспечение комплексов.
- •11. Вопросы проектирования программного обеспечения.
- •Графические языки программирования изображений.
- •Список литературы.
7. Электрохимические уо.
Оксиды переходных металлов (ОПМ) представляют собой один из наиболее интересных классов веществ с разнообразными и перспективными для практического применения свойствами. Благодаря существованию незаполненных электронных d-оболочек, в соединениях с кислородом элементы переходных групп образуют сложные системы фаз с переменной валентностью, обладающие широким спектром различных физико-химических свойств. В частности, по типу проводимости эти вещества могут быть как диэлектриками (Ta2О5, Nb2О5) или полупроводниками (FeO, MnO2), так и металлами (VO, TiO, RuO2). Неординарные свойства соединений переходных металлов обусловлены спецификой поведения d-электронов: малая пространственная протяжённость d-волновых функций, сильныe межэлектронныe и электрон-фононныe корреляции; т.е. в соединени-ях d-элементов характерные энергии взаимодействия электронов с фононами и между собой сравнимы с шириной зоны или с кинетической энергией электрона. Одним из ярких проявлений указанных эффектов фазовый переход металл- изолятор, проявляющийся во многих оксидах переходных металлов.
Для многих оксидов переходных металлов характерно также явление переключения, связанное с развитием токовых неустойчивостей в сильных электрических полях, приводящих к появлению на вольт-амперных характеристиках участков с отрицательным дифференциальным сопротивлением. Эффект отрицательного сопротивления потенциально перспективен для создания различных приборов и устройств .
Еще одним направлением исследований в физико-химии оксидов переходных металлов важным как в научном так и прикладном аспектах является исследование модификации их свойств под действием высокоэнергетичных потоков когерентного оптического (лазерного) излучения, а также при электронной и ионной бомбардировке. Многие оксидные фазы проявляют высокую чувствительность к фотонным и корпускулярным потокам. Причина высокой чувствительности соединений переходных металлов к такого рода воздействиям связана опять же с электронным строением атомов d-элементов. Наличие недостроенной d-оболочки приводит к тому, что переходные металлы проявляют в соединениях широкий набор валентных состояний, образуя целый ряд фаз. причем существуют окислы, не отвечающие формально какому-то целочисленному значению валентности металла. Для большинства оксидов переходных металлов характерны также значительные отклонения от стехиометрического состава в пределах достаточно широкой области гомогенности. Следствием указанных особенностей электронного строения является также то, что энергии различных фазовых и структурных преобразований в оксидах d-металлов относительно невелики. Это открывает возможность селективного воздействия при лазерной или корпускулярной модификации, управляемой выбором длины волны излучения или энергией частиц.
7.1. Применение материалов с переходом металл-изолятор (ПМИ) в электронной технике. При ПМИ наблюдаются резкие, обратимые и значительные изменения электрических и оптических свойств материала, что дает уникальную возможность для разработки электронных и оптоэлектронных устройств. Резкое изменение электропроводности при ПМИ используется при разработке критических терморезисторов. Освоен промышленный выпуск критических терморезисторов на основе VO2 и V2O3 (для последнего Тt=150 К). Подобные терморезисторы можно создавать на основе других материалов с ПМИ на другие критические температуры. Такие терморезисторы могут применяться в схемах тепловой защиты, стабилизации температуры, термических реле, ограничителей тока.
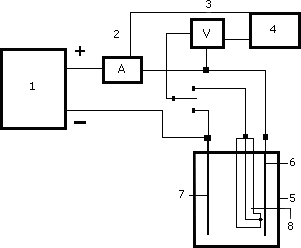
Рис.7.1.― Схема анодного окисления.
1. Блок питания .
2. Амперметр .
3. Вольтметр .
4. Двухкоординатный самописец (компьютер) .
5. Электрохимическая ячейка.
6. Анод (окисляемый металл).
7. Катод (никель, нержавеющая сталь).
8. Противоэлектрод (Pt проволока в стеклянном капилляре).
Наличие на ВАХ материалов с ПМИ участка отрицательного дифференциального сопротивления обуславливает широкие возможности применения переключающих элементов на основе материалов с ПМИ в микроэлектронике. Для VO2, например, показана возможность создания управляемой током индуктивности. Очевидна возможность использования переключательных элементов в схемах защиты микроэлектронной аппаратуры и компонентов от перенапряжений.
В ряде работ показана возможность использования VO2 для создания различных устройств управления и преобразования микроволнового излучения.
Таким образом, можно выделить три основных направления использования оксидов ванадия в электронной технике: микро- и оптоэлектроника и микроволновая техника. Однако возможности и преимущества использования материалов с ПМИ будут очевидны в том случае, если появится возможность перейти от теплового к электронному способу управления ПМИ.
7.2. Электрохромный эффект. Явление электрохромизма в тонких пленках связано с реверсивными процессами инжекции или экстракции катионов (H+, Li, Na, K и др.) и электронов в пленке и заключается в обратимом изменении оптических свойств материала (светопропускания, цвета и т.д.).
Электрохромным эффектом (ЭХЭ) обладают аморфные и кристаллические пленки предельных окислов ряда переходных металлов, таких как W, Mo, V, Nb, Ti, Ni, а также гидроокиси и гидратированные окислы некоторых металлов. Обычно для достижения ЭХЭ электрод с нанесенной на него окисной пленкой катодно поляризуют в электролите, содержащем протоны или одновалентные катионы щелочных металлов. Достаточно подробно ЭХЭ изучен в триоксиде вольфрама WO3. Появление и исчезновение окраски связывают с процессами электродиффузии катионов из электролита и обратно, а электронный заряд обеспечивает компенсацию заряда диффундирующего катиона. Электрохимический процесс при катодной поляризации можно представить как одновременный процесс переноса катиона (K+) со стороны электролита в окисел и электрона от границы электрод. При этом цвет пленки меняется от бледно-серого до голубого или синего. Изменение полярности на противоположную по знаку приводит окисел к первоначальному неокрашенному состоянию.
В некоторых оксидных системах электрохромные свойства определяются реверсивным движением кислорода в структуре материала при изменении поляризации в электролите. Так ЭХЭ в Nb2O5 приводит к сдвигу края собственного поглощения в коротковолновую область, что связывается с разупорядочением в кислородной подрешетке окисла в результате экстракции кислорода из приповерхностного слоя, приводящим к структурным изменениям в объеме окисла.
Важным с практической точки зрения является возможность инжекции и экстракции в некоторые оксидные системы ионов щелочных металлов. Так ионные процессы внедрения ионов лития в пентаксид ванадия актуальны для разработки литий-ванадиевых электрохимических источников тока.
7.3 . Электрохромные индикаторы. Электрохромный эффект перспективен для разработки индикаторов. На рисунке 7.3.1. представлена типичная схема процесса окрашивания и обесцвечивания для прибора с сэндвич-структурой. Когда на электроде отрицательный потенциал, из него в пленку WO3 инжектируются электроны, а из электролита - катионы. При этом цвет пленки меняется от бледно-серого до голубого или синего Это продолжается до тех пор, пока WO3 не превратится в вольфрамовую бронзу HxWO3. Изменение полярности на противоположную по знаку приводит окисел к первоначальному неокрашенному состоянию и объясняется обратной реакцией удаления из материала протонов и электронов.
Образование водородовольфрамовой бронзы представляют как окислительно-восстановительную реакцию, в ходе которой образуются низковалентные ионы W.5+. Однако образование КxWO3 подобно легированию вещества, тогда как в окислительно-восстановительной реакции на аноде или катоде происходит выделение вещества, объем которого зависит от длительности процесса.
Изменение оптических свойств в WO3 характеризуется появлением широкой полосы поглощения с максимумом между 0,9 и 1,46 эВ в зависимости от свойств пленки (рис.7.3.2). Предполагается, что механизм поглощения света в окрашенных аморфных пленках WO3 - интервалентный оптически индуцированный перенос 5d1- электрона иона W.5+(А) на соседнюю пустую 5d0 -орбиталь другого иона W.6+(В): W.5+(А) + W.6+(В) <-> W.6+(А) + W.5+(В).

Рис.7.3.1― Конструкция электрохромной ячейки.
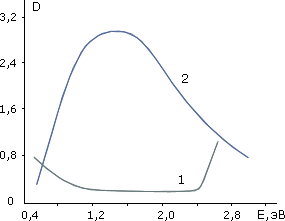
Рис.7.3.2.― Кривые оптической плотности (D) для аморфного окисла вольфрама:1 - неокрашенная WO3, 2 - окрашенная WO3.
