
- •Механика и молекулярная физика
- •Содержание
- •Раздел 1. Подготовка, выполненИе и оформление отчета по лабораторнЫм рабоТам Подготовка к лабораторному практикуму
- •Правила выполнения и оформления лабораторных работ
- •Раздел 2. Обработка результатов измерений Виды измерений
- •Классификация ошибок
- •Обработка результатов прямого измерения
- •Округление результатов
- •Обработка результатов косвенного измерения
- •Метод наименьших квадратов
- •Раздел 3. Лабораторные работы по механике и молекулярНой физиКе Лабораторная работа № 1
- •Лабораторная работа № 2
- •Лабораторная работа № 3
- •3.2.1. Ускорение силы тяжести
- •3.2.2. Описание установки
- •Лабораторная работа № 4
- •4.2.1. Основное уравнение динамики вращательного движения, момент силы, момент инерции
- •4.2.2. Маятник Обербека
- •4.4.1. Проверка зависимости углового ускорения от момента силы при постоянном моменте инерции
- •4.4.2. Проверка зависимости момента инерции грузов от расстояния до оси вращения
- •4.5.1. Определение момента инерции маятника
- •4.5.2. Определение момента инерции груза
- •Лабораторная работа № 5
- •5.2.1. Математический маятник
- •5.2.2. Физический маятник
- •5.2.3. Описание лабораторной установки
- •5.4.1. Определение ускорения свободного падения при помощи математического маятника
- •5.4.2. Определение момента инерции физического маятника
- •5.4.3. Определение момента инерции физического маятника в зависимости от распределения массы
- •5.5.1. Определение погрешности ускорения свободного падения
- •5.5.2. Расчет момента инерции физического маятника
- •5.5.3. Расчет момента инерции физического маятника в зависимости от распределения массы
- •Лабораторная работа № 6
- •6.2.1. Закон Гука
- •6.2.2. Описание лабораторной установки
- •Лабораторная работа № 7
- •7.2.1. Теплоемкость, коэффициент Пуассона
- •7.2.2. Описание и теория метода
- •Лабораторная работа № 8
- •8.2.1. Затухающие колебания. Внутреннее трение
- •8.2.2. Описание установки
- •8.4.1. Определение постоянной прибора с
- •8.4.2. Определение вязкости исследуемой жидкости
- •8.5.1. Погрешность определения постоянной прибора с
- •8.5.2. Определение вязкости исследуемой жидкости
- •Приложения
- •Список Литературы
- •Учебно-методическое издание
- •Лицензия на издательскую деятельность
7.2.2. Описание и теория метода
Предлагаемый
метод определения показателя адиабаты
![]() основан на применении адиабатического
и изохорического процессов.
основан на применении адиабатического
и изохорического процессов.
|
|
|
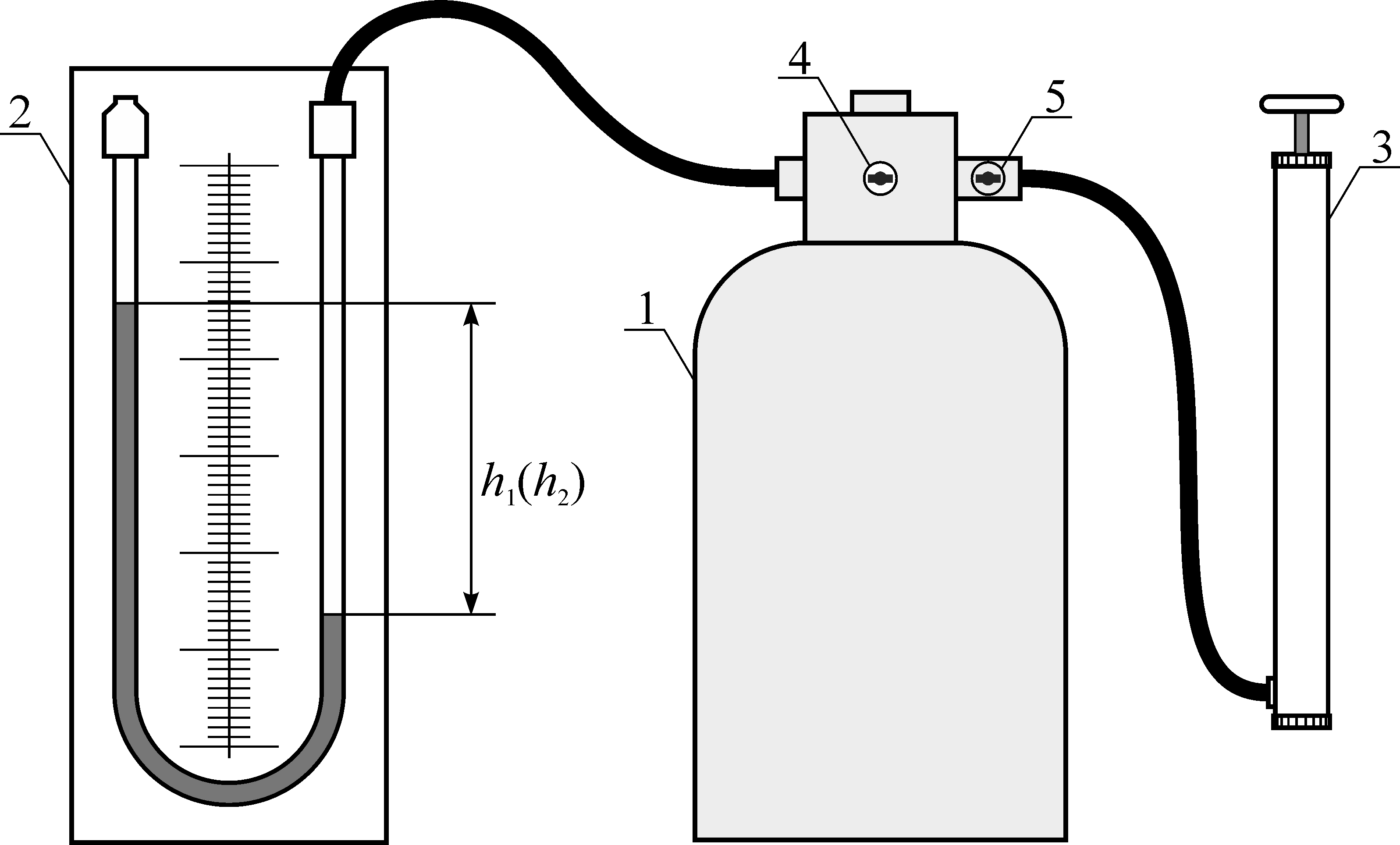
Рис. 16. Экспериментальная установка |
Установка
состоит из баллона 1, соединенного с
манометром 2 и насосом 3 (рис. 16).
Посредством крана 4 баллон может быть
соединен с атмосферой, и соответственно,
первоначальное давление в нем равно
атмосферному. Кран 5 служит для закрытия
подачи воздуха из насоса. Если с помощью
насоса быстро накачать в баллон некоторое
количество воздуха и закрыть кран, то
давление в баллоне повысится, но если
это повышение было произведено достаточно
быстро, то манометрический столбик не
сразу займет окончательное положение,
так как сжатие воздуха было адиабатическим
и, следовательно, его температура
повысится. Окончательная разность
уровней в манометре
![]() установится только тогда, когда
температура воздуха внутри баллона
сравняется, благодаря теплопроводности
стенок, с температурой окружающего
воздуха.
установится только тогда, когда
температура воздуха внутри баллона
сравняется, благодаря теплопроводности
стенок, с температурой окружающего
воздуха.
Обозначим
через
![]() термодинамическую температуру окружающего
воздуха и через
термодинамическую температуру окружающего
воздуха и через![]() – давление газа внутри сосуда,
соответствующее показанию манометра
– давление газа внутри сосуда,
соответствующее показанию манометра![]() .
Очевидно, давление, установившееся в
сосуде, будет равно
.
Очевидно, давление, установившееся в
сосуде, будет равно
|
|
(10) |
где
![]()
![]() – приращение давления, происшедшее
фактически за счет увеличения массы
воздуха в сосуде по сравнению с массой
воздуха в начальном состоянии.
– приращение давления, происшедшее
фактически за счет увеличения массы
воздуха в сосуде по сравнению с массой
воздуха в начальном состоянии.
Эти
два параметра
![]() и
и![]() характеризуют состояние газа, которое
мы назовем первым состоянием газа.
характеризуют состояние газа, которое
мы назовем первым состоянием газа.
При
быстром открывании крана воздух из
сосуда начнет выходить в атмосферу,
т.е. расширяться до тех пор, пока давление
в сосуде не сравняется с атмосферным.
Это расширение происходит достаточно
быстро и система не успевает обменяться
теплом с окружающей средой. Следовательно,
воздух расширяется адиабатически, в
результате чего его температура понизится
до некоторого значения
![]() .
Оставшаяся в сосуде масса
.
Оставшаяся в сосуде масса![]() воздуха будет в состоянии, характеризуемом
давлением
воздуха будет в состоянии, характеризуемом
давлением
![]() ,
температурой
,
температурой
![]() и объемом
и объемом![]() ,
которое назовем вторым состоянием.
,
которое назовем вторым состоянием.
Если
после этого снова закрыть кран, то
находящийся в сосуде воздух массой
![]() при давлении
при давлении
![]() и температуре
и температуре
![]() начнет изохорно нагреваться за счет
теплообмена с окружающей средой до тех
пор, пока температура внутри и вне сосуда
не станет одинаковой. При этом давление
указанной массы воздуха увеличится на
некоторую величину
начнет изохорно нагреваться за счет
теплообмена с окружающей средой до тех
пор, пока температура внутри и вне сосуда
не станет одинаковой. При этом давление
указанной массы воздуха увеличится на
некоторую величину
![]() и станет равным
и станет равным
|
|
(11) |
В
итоге мы имеем третье состояние воздуха
с параметрами
![]() ,
,![]() ,
,![]() и
и![]() .
.
Адиабатический переход воздуха из первого состояния во второе описывается законом Пуассона (9), которое, используя уравнение состояния (2), можно записать в виде
|
|
(12) |
а изохорный переход из второго состояния в третье – законом Гей-Люссака
|
|
(13) |
Принимая во внимание (10) и (11), из (12) и (13) получим
 .
.
Логарифмируя это выражение, имеем:
![]() .
.
В
случае относительно малых изменений
давления
![]() и
и![]() по сравнению с атмосферным
по сравнению с атмосферным![]() ,
можно воспользоваться соотношением
,
можно воспользоваться соотношением![]() ,
в итоге получим
,
в итоге получим
![]() ,
,
откуда
|
|
(14) |
Таким
образом, при относительно небольших
изменениях давления
![]() и
и![]() их измерение дает возможность определить
значение.
их измерение дает возможность определить
значение.
Установка,
схема которой приведена на рис. 16,
связана с водяным манометром со шкалой
для измерения перепада давления воздуха
в баллоне по сравнению с атмосферным.
Поэтому изменение давления
![]() ,
заключенного в баллоне воздуха по
сравнению с атмосферным давлением,
определяется разностью высот уровней
воды в коленах манометра
,
заключенного в баллоне воздуха по
сравнению с атмосферным давлением,
определяется разностью высот уровней
воды в коленах манометра
![]() ,
,
где h – разность высот уровней воды в манометре; – плотность воды; g – ускорение свободного падения.
Поэтому
измерение![]() и
и![]() сводится
к измерению соответствующих разностей
сводится
к измерению соответствующих разностей
![]() и
и![]() высот уровней воды в коленах манометра,
а формула (14) для расчета
– к формуле
высот уровней воды в коленах манометра,
а формула (14) для расчета
– к формуле
|
|
(15) |
Приборы и принадлежности
Баллон – 1 шт.
Манометр – 1 шт.
Насос – 1 шт.
Штангенциркуль – 1 шт.
Порядок выполнения работы
1. При закрытом кране баллона 4 открыть кран насоса 5 и с помощью насоса накачать в баллон воздух до тех пор, пока разность высот уровней воды в манометре не достигнет 10 – 15 см. Закрыть кран насоса 5.
2. Выждав
2 – 3 минуты, пока температура внутри
баллона не станет равной температуре
окружающего воздуха, измерить
установившуюся разность высот
![]() уровней воды в коленах манометра.
уровней воды в коленах манометра.
3. Поворотом рукоятки крана 4 открыть баллон и в момент, когда уровни воды в коленах манометра сравняются, быстро закрыть кран.
4. Выждать
опять 2 – 3 минуты, пока охлажденный при
адиабатическом расширении воздух
нагреется до прежней (комнатной)
температуры, и измерить установившуюся
разность уровней
![]() .
.
5. Поворотом крана 4 открыть баллон для установления в нем атмосферного давления, а затем снова закрыть.
6. Повторить
опыт 10 раз, меняя каждый раз значение
![]() .
Результаты эксперимента занести в
таблицу 22.
.
Результаты эксперимента занести в
таблицу 22.
Таблица 22. Коэффициент Пуассона для воздуха
|
№ |
h1, мм |
h2, мм |
|
|
|
, % |
|
1 |
|
|
|
|
|
|
|
… |
|
|
| |||
|
10 |
|
|
|
Обработка результатов измерения
1. По формуле (15) вычислить значение и записать в таблицу 22.
2. Для
определения погрешности измерения
необходимо использовать метод наименьших
квадратов, т.к. измерения физических
величин различны. Зависимость значения
уровня высоты
![]() от
от![]() выражается из (15) линейной зависимостью
выражается из (15) линейной зависимостью
![]() ,
,
где
![]() .Для
начала необходимо вычислить значения
величин
.Для
начала необходимо вычислить значения
величин
![]() ,
,![]() для каждого измерения и записать в
таблицу 23, а затем найти среднее значение
коэффициентаk
по формуле
для каждого измерения и записать в
таблицу 23, а затем найти среднее значение
коэффициентаk
по формуле
 .
.
Таблица 23. Оценка погрешности коэффициента Пуассона
|
№ п/п |
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
… |
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
– |
– |
|
|
– |
|
3. Вычислить коэффициент Пуассона по формуле
![]() .
.
4. Вычислить среднеквадратичную ошибку среднего арифметического, используя данные из таблицы 23 по формуле
 .
.
5. Найти
абсолютную погрешность
![]() по формуле
по формуле
![]() ,
,
где
коэффициент Стьюдента
![]() для надежности
для надежности![]() и числа измерений
и числа измерений![]() взять из таблицы 29.
взять из таблицы 29.
6. Окончательный результат записать в виде
![]() при
при
![]() ,
,![]() .
.
Контрольные вопросы
1. Что называют удельной (молярной) теплоемкостью вещества?
2. Получите взаимосвязь между удельной и молярной теплоемкостями идеального газа,.
3. Что называют числом степеней свободы молекулы? Чему равно число степеней свободы для одноатомного, двухатомного, трехатомного газа?
4. Пользуясь первым началом термодинамики, получите связь между молярными теплоемкостями при постоянном объеме и при постоянном давлении через число степеней свободы молекулы. Как записывается уравнение Майера?
5. Что такое коэффициент Пуассона? Как объяснить, что его значение для любого газа больше единицы? Чему равен коэффициент Пуассона для воздуха?
6. Какие процессы происходят с воздухом в настоящей работе? Каким законам они подчиняются?
7. Какой процесс называют адиабатическим? Получите уравнение этого процесса для идеального газа, пользуясь первым законом термодинамики и уравнением состояния.
8. Изобразите
в координатах
![]() адиабатический и изотермический
процессы.
адиабатический и изотермический
процессы.
9. Что утверждает закон равнораспределения энергии по степеням свободы молекул? Каковы границы его применимости?

 ,
,