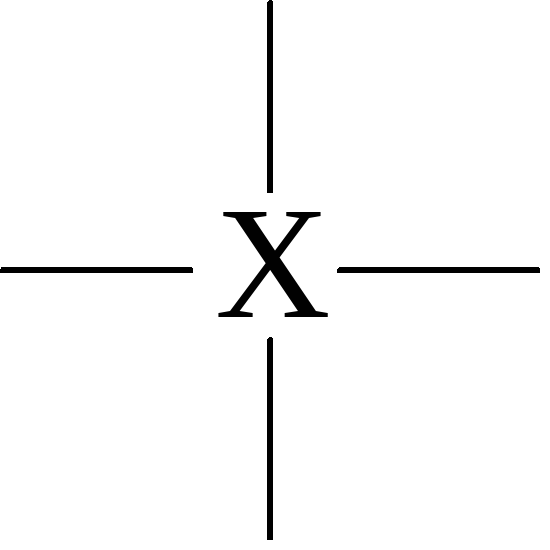- •Сборник заданий
- •Задание 1 по теме "строение вещества"
- •1 Задание 1 по теме: «строение атома»
- •2.1 Опишите строение предложенных в варианте задания молекул и молекулярных ионов по методу валентных связей (мвс).
- •2.2 Строение молекул и ионов по методу молекулярных орбиталей (мо)
- •Раздел 3.1
- •3.1 Проанализируйте влияние сил межмолекулярного взаимодействия на свойства веществ (решите задачу с указанным номером).
- •Список рекомендуемой литературы
- •Задание 2 по теме: «термохимия. Направление химических реакций»
- •Примеры решения задач
- •2 Рекомендации для самостоятельной работы студентов и варианты заданий
- •3 Задачи для самостоятельного решения
- •4. Варианты заданий
- •1 Примеры решения задач
- •1.3 Вычисление константы химического равновесия
- •1.4 Вычисление равновесных концентраций
- •1.5 Направление смещения равновесия
- •Задачи для самостоятельного решения
- •Варианты заданий
- •Список рекомендуемой литературы
- •Задание 4 по теме «Растворы»
- •Примеры решения задач
- •1.1 Процентная концентрация
- •1.3 Моляльная концентрация (моляльность) , мольная доля, титр
- •1.4 Осмотическое давление. Закон вант- гоффа
- •1.5 Давление насыщенного пара растворов. Тонометрический закон рауля
- •1.6 Температуры кипения и замерзания растворов.
- •2.Задачи для самостоятельного решения
- •3. Варианты заданий для самостоятельной работы
- •Список рекомендуемой литературы
- •Задание 5 по теме "растворы электролитов"
- •Примеры решения задач
- •1.1 Вычисление степени диссоциации слабых электролитов
- •1.2 Сильные электролиты. Вычисление степени электролитической диссоциации
- •1.3 Произведение растворимости
- •1.5 Обменные реакции в растворах электролитов
- •Задачи для самостоятельного решения
- •Варианты домашних заданий
- •Приложение а
- •Список рекомендуемой литературы
- •Задание 6 по теме «гидролиз солей»
- •Примеры решения задач
- •Варианты контрольных заданий
- •Приложение а
- •Список рекомендуемой литературы
- •Задание 7 по теме «Окислительно–восстановительные реакции. Электрохимия»
- •Примеры решения задач
- •2 Задания для самостоятельного решения
- •Список рекомендуемой литературы
- •Задание 8 по теме «Классификация и свойства неорганических веществ»
- •Примеры решения задач
- •Пример 5. С какими из перечисленных веществ вступит в реакцию серная кислота:koh,CuO,Ba(oh)2,Fe2o3,Al2o3,co2,SiO2,h3po4, o2,h2o? Составьте уравнения возможных реакций.
- •Задания для самостоятельного решения
- •Варианты заданий
- •Список рекомендуемой литературы
- •Задание 9 по теме "Комплексные соединения"
- •Примеры решения задач
- •2 Задачи для самостоятельного решения
- •3 Варианты заданий
- •Список рекомендуемой литературы
- •Задание 10 по теме «свойства элементов и их соединений»
- •ПримерЫ решения задач
- •3 Варианты заданий
- •Список рекомендуемой литературы
- •Сборник заданий для самостоятельной работы студентов по дисциплине «Общая и неорганическая химия»
- •450062, Республика Башкортостан, г.Уфа, ул. Космонавтов,1
2.1 Опишите строение предложенных в варианте задания молекул и молекулярных ионов по методу валентных связей (мвс).
а) Составьте структурную формулу.
б) Определите геометрию молекулы (молекулярного иона) по методу
отталкивания валентных электронных пар.
в) Определите полярность связей и полярность молекулярной частицы.
г) Объясните, как образуются связи:
- укажите, какие связи (σ, π) в молекулярной частице;
- механизм образования (обменный или донорно-акцепторный);
- из каких частиц (атомов, ионов) формируется молекулярная частица;
- составьте электронно-графические формулы валентных электронов (в
основном и возбужденном состояниях);
- определите тип гибридизации атомных орбиталей центрального атома;
составьте схему перекрывания атомных орбиталей, при образовании
σ – связей;
- опишите, как образуются π- связи.
Пример
Описать строение молекулы NH3 по методу валентных связей (МВС).
Решение: Составим электронные формулы атомов.
7N
1s22s22p3
валентные электроны 2s22p3;
![]()
1H
1s1
валентный электрон
![]()
Атом азота имеет три неспаренных электрона и четыре валентные атомные орбитали. Возбужденное состояние для него энергетически невыгодно, так как в валентном уровне нет свободных орбиталей. Валентность атома азота в соединениях может быть 3 или максимально – 4. У атома водорода один неспаренный электрон и его валентность в соединениях только 1.
Атом N является центральным, вокруг которого координируются атомы Н.
Можно записать структурную формулу молекулы NH3.

Атом азота находится в основном состоянии. Три неспаренных электрона образуют три ковалентные σ- связи по обменному механизму. В образовании связей у атома азота принимают участие одна s-орбиталь и три p-орбитали (с учетом неподеленной пары электронов). Следовательно, должна наблюдаться sp3- гибридизация валентных атомных орбиталей атома азота.
σ-Связи N-H образуются по обменному механизму перекрыванием sp3-гибридных атомных орбиталей атома азота и 1s-орбиталей атомов водорода.
sp3 –Гибридные атомные орбитали ориентированы из центра тетраэдра к его вершинам, под углом 109°28'. Одна из вершин «тетраэдра» (в направлении неподеленной электронной пары) остается свободной. Таким образом, молекула NH3 имеет геометрическую форму треугольной пирамиды, вершиной которой является атом азота, а в основании находятся атомы водорода. Валентный угол между связями HNH должен составлять 109°28'.
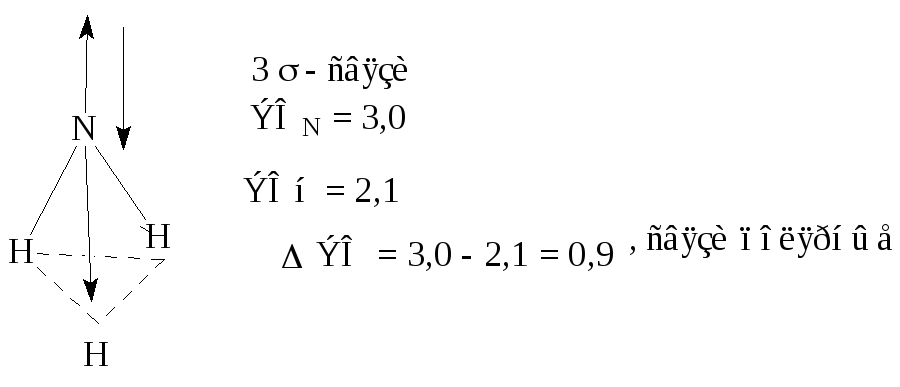
Степень ионности связи N-H находим на основании таблиц 6 и 7. Чем выше различие в ЭО, тем в большей степени cвязь приближается к ионной. Например, для связи Н-F: ΔЭО = 4-2,1=1,9; следовательно, связь полярно-ионная на 50%.
Рассчитаем ионность связи N-H. Значение ∆ЭО=0,9 находится между значениями 0,6 и 1,2. Разница 1,2-0,6=0,6 единиц, разница степени ионности: (25 – 7 = 18). Разница ∆ЭО в нашем случае: (0,9 - 0,6 = 0,3). На разность ∆ЭО = 0,3 приходится разность степени ионности, рассчитанная по пропорции:
 0,6
- 18 х=9.
0,6
- 18 х=9.
0,3 - х
Прибавляем 9 к меньшему значению 7 и получаем степень ионности связи N-H: (7 + 9=16%).
Так как σ -связи молекулы полярные и молекула NH3 имеет несимметричное строение, то суммарный дипольный момент молекулы не равен 0 (μ≠0), т.е. молекула NH3- полярная и ее можно представить, как диполь, в котором избыточный отрицательный заряд находится на азоте, а положительный на атомах водорода.
Теоретический валентный угол HNH (без учета гибридизации) равен 900, но так как наблюдается sp3-гибридизация, валентный угол должен приблизиться к 109°28', справочные данные -107°.
Таблица 6- Определение степени ионности связи
|
ΔЭО |
0 |
0,6 |
1,2 |
1,8 |
2,2 |
2,6 |
|
Степень ионнос-ти связи, % |
0 |
7 |
25 |
47 |
61 |
74 |
Таблица 7- Относительные электроотрицательности элементов (по Полингу)
|
Н 2,2 |
| ||||||||||||||||
|
Li 1,0 |
Be 1,6 |
|
В 1,8 |
C 2,5 |
N 3,0 |
O 3,4 |
F 4,0 | ||||||||||
|
Nа 0,93 |
Mg 4,3 |
|
Al 1,6 |
Si 1,9 |
P 2,2 |
S 2,6 |
Cl 3,2 | ||||||||||
|
K 0,82 |
Ca 1,0 |
Sc 1,4 |
Ti 1,5 |
V 1,6 |
Cr 1,7 |
Mn 1,6 |
Fe 1,8 |
Co 1,9 |
Ni 1,9 |
Cu 2,0 |
Zn 1,6 |
Gd 1,8 |
Ge 2,0 |
As 2,2 |
Se 2,6 |
Br 3,0 | |
|
Rb 0,82 |
Sr 0,9 |
Y 1,2 |
Zr 1,5 |
Nb 1,6 |
Mo 2,2 |
Tc - |
Ru 2,2 |
Rh 2,3 |
Pd 2,2 |
Ag 1,9 |
Cd 1,7 |
In 1,6 |
Sn 1,8 |
Sb 2,0 |
Te 2,1 |
I 2,7 | |
|
Cs 0,79 |
Ba 0,9 |
|
Pt 2,3 |
Au 2,5 |
Hg 2,0 |
Tl 2,0 |
Pb 2,3 |
Bi 2,0 |
PO - |
| |||||||
Геометрия основных типов молекулярных структур приведена в таблице 8
Таблица 8-Геометрия основных типов молекулярных структур
|
Число сте-реоактив-ных электр. пар |
Расположение электронных пар |
Число связываю-щих элек-тр. пар |
Число не-поделен-ных пар |
Геометрия молекулы |
Примеры |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
1 |
линейное |
2 |
0 |
линейная =Х= линейная
|
СO2, N2O, HCN |
Продолжение
|
1 |
2 |
3 |
4 |
5 |
6 |
|
2 |
треугольное равностороннее |
3
2 |
0
1 |
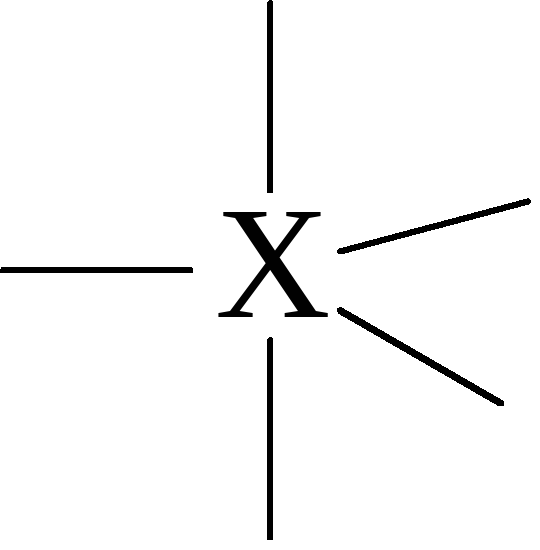
плоская треугольная
изогнутая
|
SO3, BF3, СН2О CO32-,NO3-
SO2, NO2- |
|
3 |
тетраэдрическое |
4
3
2 |
0
1
2 |
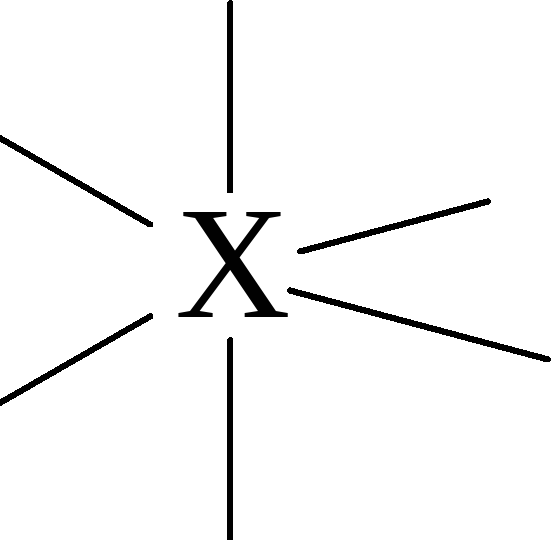
тетраэдричес-кая
тригональная пирамидальная
изогнутая
|
CH4, NH4+ SO42- BF4-
NH3, ClO3-, SO32- PCl3 H3O+
H2O ClO2- |
|
4 |
тригональное бипирамидальное |
5
4
3
2 |
0
1
2
3 |
тригональная бипирамидаль-ная
«ходульная»
Т-образная
линейная |
PCl5 SbCl5
SF4 TeCl4
ClF3 BrF3
XeF2 J3- |
|
5 |
октаэдрическое |
6
5
4 |
0
1
2 |
октаэдрическая
пирамидальная квадратная
плоская квадратная
|
SF6 SiF2- PF6-
BrF5,ХeOF4, SbCl5
BrF4-, ХeF4 |