
- •Билет 1
- •I. Препараты обратимого действия
- •II. Препараты необратимого действия
- •Третичные амины
- •Четвертичные амины
- •Фосфорорганические соединения (фос).
- •Острое отравление фос
- •Неотложная помощь при интоксикации фос:
- •3.Пути введения и выведения лекарственных веществ из организма ( лечебное и токсическое значение) Энтеральные пути введения
- •Парентеральные пути введения
- •Почечная экскреция
- •Другие пути экскреции
- •Билет 2
- •1.Мочегонные средства (антагонисты альдостерона и ингибиторы карбоангидразы) Физиологические основы мочеобразования и возможные механизмы действия диуретиков.
- •Типы транспорта веществ в почках
- •1. Пассивная диффузия
- •2. Активная диффузия в базальной мембране нефроцитов
- •Классификация диуретиков
- •По характеру мочегонного эффекта:
- •Диуретики с преимущественным действием на клубочек. (Эуфиллин, Теофиллин)
- •Диуретики с преимущественным действием на проксимальный каналец. Осмотические диуретики(Маннит, Мочевина)
- •Ингибиторы карбоангидразы. (Диакарб)
- •Диуретики, действующие на восходящую часть петли Генле («петлевые» диуретики)
- •Диуретики, действующие на начальную часть дистального канальца.
- •Тиазидные диуретики. Гидрохлоритизид (Гипотиазид, Дихлотиазид), Циклометиазид.
- •Тиазидоподобные диуретики. Оксодолин, Клопамид, Индапамид
- •Диуретики с преимущественным действием на конечную часть дистального канальца и собирательные трубки (калийсберегающие диуретики).
- •Конкурентные антагонисты альдостерона. Спиронолактон (Верошпирон).
- •Блокаторы натриевых каналов. Триамтерен, Амилорид.
- •2.Противогрибковые средства
- •Характеристика грибковых заболеваний
- •Классификация противогрибковых препаратов.
- •Механизм действия противогрибковых препаратов.
- •Антибиотики полиеновой структуры.
- •Амфотерицин в.
- •Нистатин.
- •Натамицин (пимафуцин)
- •Производные имидазола.
- •Гризеофульвин.
- •Аллиламины тербинафин (ламизил) и нафтифин (экзодерил)
- •Эхинокандины Каспофунгин (кансидас) и микафунгин (микамин)
- •Аморолфин (лоцерил)
- •Циклопирокс (батрафен)
- •Хлорнитрофенол (нитрофунгин)
- •3.Определение фармакологии, место среди других наук.
- •Билет 3
- •Ацеклидин.
- •2.Противотуберкулезные средства Туберкулез вызывают микобактерии туберкулеза. Классификация:
- •Билет 4
- •Стадия возбуждения:
- •2. Стадия угнетения:
- •Платифиллина гидротартрат.
- •Метацин.
- •Средства при бронхоспазме
- •Адреналина гидрохлорид
- •Билет 5.
- •Никотин.
- •Лобелина гидрохлорид.Цититон.
- •Взаимосвязь между химическим строением и антибактериальным действием сульфаниламидных препаратов.
- •Механизм действия.
- •Классификация сульфаниламидных препаратов по химическому строению.
- •Производные алифатического ряда:
- •3. Производные ароматического ряда
- •Классификация сульфаниламидных препаратов по спектру действия.
- •По продолжительности действия:
- •В зависимости от растворимости, всасываемости и применения.
- •Фармакокинетические показатели сульфаниламидных препаратов.
- •Фармакологическая характеристика сульфаниламидных препаратов
- •Принципы лечения сульфаниламидными препаратами.
- •Побочные эффекты.
- •1. Действие на цнс.
- •2. Действие на функцию щитовидной железы.
- •3. Действие на систему крови.
- •4. Действие на сердечно-сосудистую систему.
- •5. Действие на почки.
- •8. Аллергические реакции.
- •Взаимодействие сульфаниламидных препаратов с другими антимикробными препаратами.
- •Сульфаметоксазол с триметопримом («Ко-тримоксазол», «Бисептол», «Бактрим»)
- •Производные алифатического ряда Сульфацил-натрий.
- •Уросульфан.
- •Производные ароматического ряда. Сульфапиридазин.
- •Сульфадимезин.
- •Сульфадиметоксин.
- •Билет 6
- •Бензогексоний.
- •Арфонад.
- •Курареподобные средства (миорелаксанты периферического действия).
- •Миорелаксанты деполяризующего действия.
- •Дитилин.
- •Миорелаксанты антидеполяризующего действия.
- •1) Препараты окситоцина
- •2) Препараты вазопрессина
- •Окситоцин (вводят в/м, в/в)
- •Вазопрессин
- •7 Билет
- •Классификация адренергических средств.
- •Адреналина гидрохлорид
- •Влияние на сердце
- •Влияние на метаболизм
- •Норадреналина гидротартрат.
- •Отличия норадреналина гидротартрата от адреналина.
- •Особенности действия нафтизина и галазолина.
- •Изадрин
- •Добутамин
- •Сальбутамол
- •Симпатомиметики ( адреномиметики непрямого действия).
- •Классификация
- •Отхаркивающие средства (секретомоторные).
- •Средства рефлекторного действия (препараты лекарственных растений, бензоат натрия).
- •Средства резорбтивного действия (калия иодид).
- •Билет 8
- •2. Средства, блокирующие нейрональные кальциевые каналы т-типа.
- •3.Средства, усиливающие тормозные гамКергические влияния вЦнс.
- •Клиническая классификация противоэпилептических средств
- •Последовательность (ранжирование) выбора пэс в зависимости от типа эпилептического припадка (препараты 1, 2, 3-го выбора и т. Д.)
- •2.Фибринолитические и антифибринолитические средства Фибринолиз – процесс растворения тромба
- •Фибринолитические средства.
- •Классификация фибринолитические средств
- •Фибринолизин (плазмин)
- •Активаторы профибринолизина (плазминогена).
- •Фибринспецифические тромболитические средства — активаторы плазминогена
- •Ингибиторы фибринолиза.
- •Синтетические ингибиторы фибринолиза.
- •Ингибиторы фибринолиза животного происхождения.
- •Классификация
- •Средства влияющие на ионные каналы
- •Донаторы окиси азота
- •Миотропные вазодилататоры
- •1. Средства, влияющие на ионные каналы (миотропные вазодилататоры непрямого действия):
- •2. Донаторы окиси азота (n0).
- •3. Препараты с разным механизмом действия. Блокаторы кальциевых каналов (бкк)
- •Активаторы калиевых каналов
- •Донаторы окиси азота (nо)
- •Препараты с разным механизмом действия (миотропные вазодилататоры прямого действия)
- •Билет 9
- •Классификация адреноблокирующих средств.
- •Анаприлин
- •Кардиоселективные β1-адреноблокаторы
- •Классификация:
- •Препараты хлора.
- •(Хлоргексидина глюконат, гибитан, манусан, себидин, хибитан)
- •«Себидин»
- •Препараты йода.
- •Раствор йода спиртовой.
- •Органические препараты йода.
- •Йодофоры
- •Йодоформ
- •Йодинол
- •Препараты фтора.
- •Билет 10
- •Классификация:
- •Тропафен
- •Празозин
- •Тамсулозин
- •Доксазозин
- •2.Препараты водорастворимых витаминов
- •Классификация
- •3.Принципы антибиотикопрофилактики
- •Билет 11
- •Классификация нейролептиков
- •2). Сильные блокаторы d2-рецепторов, слабо или умеренно блокирующие также серотониновые с2α-рецепторы и α1-адренорецепторы
- •3). Поливалентные седативные нейролептики
- •4). Нейролептики, практически в равной степени блокирующие d2-с2α-рецепторы (в несколько большей степени последние) и слабее – α1-адренорецепторы
- •5). Атипичные поливалентные нейролептики, подобно препаратам третьей группы не дифференцированно блокирующие большинство рецепторов в цнс
- •Сравнительная степень блокирующего действия нейролептиков на рецепторы мозга
- •Механизм действия нейролептиков.
- •Центральные и периферические эффекты нейролептиков Антипсихотическое действие
- •Психоседативное действие
- •Влияние на вегетативные функции Гипотермическое действие
- •Противорвотное действие
- •Ортостатическая гипотензия
- •Влияние на сердечную деятельность
- •Изменение секреции гормонов
- •Блокада м-холинорецепторов
- •Влияние на моторику
- •Выраженность седативного и антипсихотического действия нейролептиков, дозы и аминазиновые эквиваленты
- •3. Некоторые пограничные состояния: психопатии, повышенная возбудимость, агрессивность, нарушения поведения у детей, подростков, пожилых людей.
- •4. Тошнота и рвота центрального происхождения, икота.
- •5. Травматический и ожоговый шок
- •Побочные эффекты нейролептиков.
- •Производные фенотиазина
- •Производное бутирофенона
- •Антипсихотические нейролептики — дофаминоблокаторы
- •1. Производные фенотиазина с пиперазиновым радикалом
- •2. Производное бутирофенона
- •3. Производные замещенного бензамида сульпирид
- •Атипичные нейролептики
- •Ингибиторы ангиотензинпревращающего фермента
- •Эффекты иАпф, связанные с подавлением активности плазменной рас:
- •Эффекты иАпф, связанные с подавлением активности тканевой рас:
- •Блокаторы рецепторов аii
- •Билет 12
- •Классификация болеутоляющих средств.
- •1). Классификация по химическому строению
- •2). Классификация по взаимодействию с опиоидными рецепторами (о.Р.)
- •Механизм действия опиоидных (наркотических) анальгетиков.
- •Морфина гидрохлорид.
- •Влияние на цнс Кора больших полушарий
- •Гипоталамус и железы внутренней секреции
- •Средний мозг
- •Продолговатый мозг Дыхательный центр
- •Центр блуждающего нерва
- •Рвотный центр
- •Сосудодвигательный центр
- •Спинной мозг
- •Влияние на сердечно-сосудистую систему
- •Влияние на органы с гладкой мускулатурой
- •Острое и хроническое отравление. Меры помощи.
- •Хроническое отравление наркотическими анальгетиками
- •Омнопон.
- •Промедол.
- •Фентанил.
- •Понятие о нейролептанальгезии.
- •Пентазоцин.
- •Бупренорфин.
- •Буторфанол.
- •Привыкание, лекарственная зависимость.
- •Профилактика и принципы лечения наркоманий.
- •Препараты ртути.
- •Препараты серебра. Серебра нитрат. Обладают противомикробным, вяжущим, противовоспалительным и прижигающим действием.
- •Препараты меди. Меди сульфат.
- •Препараты цинка. Цинка сульфат.
- •Цинка оксид (цинка окись, деситин)
- •Растворы для внутреннего применения
- •Билет 13
- •Транквилизаторы (лат. Tranquillium - спокойствие, покой), или Анксиолитики (лат. Anxius - тревожный, полный боязни, охваченный страхом, греч. Lysis - растворение)
- •Классификация транквилизаторов
- •1). Мощные, ночные, тяжелые:
- •2). Дневные, слабые:
- •Механизм действия транквилизаторов.
- •Основные фармакологические эффекты транквилизаторов:
- •Показания и противопоказания к применению транквилизаторов.
- •Побочные эффекты транквилизаторов.
- •Раствор перекиси водорода.
- •Калия перманганат.
- •Метиленовый синий
- •Этакридина лактат.
- •Бриллиантовый зеленый.
- •Формалин
- •Гексаметилентетрамин
- •Раствор формальдегида.
- •Спирт этиловый.
- •Билет 14
- •1. Формы рецептурных бланков и правила их оформления
- •2. Лекарственная зависимость (физическая и психическая). Медицинские и социальные аспекты борьбы с наркоманиями.
- •Билет 15
- •Классификация противопаркинсонических средств
- •1.Адренергические вещества:
- •2. Агонисты имидазолиновых рецепторов:
- •Адренергические вещества.
- •Клофелин (Клонидин, Гемитон, Катапресан)
- •Гуанфацин (Эстулик)
- •Метилдопа (Альдомет, Допегит) (l-изомер)
- •Агонисты имидазолиновых рецепторов.
- •3.Противокашлевые средства Вещества, способные угнетать кашлевой рефлекс в центральном звене или за счет воздействия на чувствительные окончания в дыхательных путях.
- •Кодеин (метилморфин) и Этилморфина гидрохлорид (дионин).
- •Глауцина гидрохлорид(глаувент) и тусупрекс (окселадина цитрат).
- •Либексин.
- •Билет 16
- •Ганглиоблокирующие средства Пентамин, Бензогексоний, Гигроний.
- •Симпатолитики Гуанетдин (октадин), Резерпин.
- •Лабеталол.
- •Мерказолил.
- •Органопрепараты
- •Билет 17
- •Классификация ноотропных средств
- •Актопротекторы
- •Пенициллины.
- •Цефалоспорины.
- •Карбапенемы.
- •Классификация
- •В зависимости от консистенции:
- •В зависимости от места изготовления:
- •В зависимости от дозы:
- •Билет 18
- •Билет 19
- •Ингибиторы соляной кислоты и пепсиногена.
- •Холинолитические средства.
- •H2‑антигистаминные средства.
- •Ингибиторы протонной помпы.
- •Простагландины.
- •2.Препараты гормонов женских половых желез . Лекарственные средства для контрацепции.
- •Классификация женских половых гормонов
- •1. Содержащие э с т р о г е н и п р о г е с т и н:
- •Эстрогенные препараты
- •Антиэстрогенные средства.
- •Гестагенные (прогестагенные) и антигестагенные препараты
- •Антигестагенные средства
- •Гормональные контрацептивные средства.
- •Классификация гормональных контрацептивных препаратов:
- •1. Комбинированные эстроген‑гестагенные препараты:
- •2. Гестагенные препараты:
- •Билет 20
- •Билет вроде 21
- •1.Лс растительного происхождения (настои, отвар, настойка, экстракт)
- •Настойки
- •Микстуры
- •Новогаленовые препараты
- •2.Противотуберкулезные средства
- •Классификация По активности
- •По происхождению
- •1 Группа
- •Механизм действия
- •Побочные эффекты
- •2 Группа
- •Фармакологический эффект: бактериостатический
- •Фармакологический эффект: бактерицидный
- •3 Группа
- •Фармакологический эффект: бактериостатический
- •Классификация:
- •Противопоказания
- •Побочное действие
- •Билет 22
- •Билет 23
- •3.Виды действия лекарственных веществ По локализации фармакологических эффектов:
- •Билет 24
- •1.Жирорастворимые витамины
- •Классификация
- •2.Антикоагулянты Антикоагулянты
- •Антикоагулянты прямого действия.
- •Антикоагулянты непрямого действия
- •3.Мягкие лекарственные формы
- •Накожные (трансдермальные) терапевтические системы
- •Задача про бисептол Билет 25
- •1. Производные бензодиазепина
- •2.Производные других хим групп ( т.Е. Циклопирролона)
- •3.Производные барбитуровой кислоты
- •Слабительные, размягчающие каловые массы.
- •Слабительные, увеличивающие объем химуса.
- •Слабительные, раздражающие рецепторы кишечника.
- •Классификация:
- •Макролиды.
- •Билет 26
- •Таблетки
- •Капсулы
- •Классификация
- •Препараты тромбина.
- •Фибриноген.
- •Факторы свертывания VIII и IX
- •Препараты витамина k.
- •Классификация
- •1) Средства, применяемые для лечения кишечных гельминтозов
- •2) Средства, применяемые для лечения внекишечных гельминтозов
- •Билет 27
- •4). Производные пиперидина:
- •Психомоторные стимуляторы
- •Влияние на нейрофизиологические процессы Повышение бодрствования мозга
- •Повышение змоционально-мотивационного реагирования
- •Оживление движений
- •Влияние на психофизиологические процессы
- •Препараты психомоторных стимуляторов Производные фенилалкиламина
- •Производные сиднонимина
- •Производные ксантина
- •Препараты гормонов передней и средней доли гипофиза.
- •Препараты гормонов передней доли гипофиза и их фармакологические эффекты
- •Билет 28
- •Анальгетическое действие.
- •Противовоспалительное действие.
- •Жаропонижающее действие.
- •Показания к применению неопиоидных анальгетиков.
- •2. Послеоперационные боли средней интенсивности.
- •5. Миозиты, невралгии, радикулиты.
- •6. Болевой синдром при спазме мочевыводящих, желчевыводящих путей (колики), панкреатите.
- •8. Гиперпиретические состояния (лихорадка) при инфекционных заболевани-
- •Побочные эффекты и осложнения.
- •Противопоказания к применению
- •Билет 29
- •30 Билет
- •1.Слабительные средства , вызывающие изменение объема химуса и механическое раздражение рецепторов слизистой кишечника
- •Классификация
- •3.Противовирусные средства Классификация :
- •Билет 31
- •1) Средства, стимулирующие образование желчи (холеретики)
- •2) Средства, способствующие выведению желчи (холекинетики)
- •Холеретики Холензим
- •Холосас
- •Оксафенамид
- •Магния сульфат
- •3.Жидкие лекарственные формы из растительного сырья ( настои, отвары, настойки, экстракты)
Атипичные нейролептики
Атипичные нейролептики в меньшей степени, чем производные фенотиазина и бутирофенона, блокируют D2-рецепторы дофамина в нигростриарной системе и гипоталамусе, вызывают блокаду этих рецепторов в течение непродолжительного срока, являются антагонистами рецепторов серотонина 5-НТ2A (блокада этих рецепторов сопровождается повышенным выделением дофамина в префронтальной коре
Они эффективно подавляют психопродуктивную симптоматику, коморбидные аффективные расстройства (дисфория, депрессия), медленно, через 1 — 6 мес. терапии, улучшают коммуникативные способности, абстрактное мышление, познавательные функции, внимание, память, речевую беглость у больных шизофренией, редко вызывают экстрапирамидные нарушения и избыточную секрецию пролактина.
Оказывают терапевтическое действие у пациентов, резистентных к лечению традиционными препаратами, пригодны для противорецидивной терапии.
Представителем класса атипичных нейролептиков является производное бензодиазепина клозапин.
КЛОЗАПИН
Обладает низким аффинитетом к D2-рецепторам дофамина в полосатом теле и гипоталамусе, блокирует D4-рецепторы в лимбической системе и префронтальной области коры больших полушарий, α-адренорецепторы, М-холинорецепторы, H1-рецепторы гистамина и рецепторы серотонина 5-НТ2A.
Проявляет антипсихотическую и психоседативную активность, не вызывает заторможенность, апатию, вялость, сглаживает негативные симптомы (интравертность, бедность речи).
При терапии клозапином не повышается секреция пролактина, редко возникают экстрапирамидные расстройства.
У 1 % больных клозапин вызывает тяжелый агранулоцитоз, у 7 % — ортостатическую гипотензию, в редких случаях создает опасность токсико-аллергического миокардита.
Атипичные нейролептики несколько различаются между собой по профилю психотропного действия и спектру побочных эффектов.
При равной общей антипсихотической активности клозапин и оланзапин характеризуются более выраженным глобальным антипсихотическим влиянием, а рисперидон и амисульприд — избирательным антибредовым и антигаллюцинаторным действием.
Седативные свойства в большей степени выражены у клозапина, оланзапина, кветиапина, активирующий эффект — у амисульприда и рисперидона.
Антиманиальное действие доказано в отношении оланзапина, кветиапина и рисперидона.
Амисульприд и рисперидон эффективно редуцируют депрессивную и энергическую симптоматику.
Длительный прием атипичных нейролептиков сопряжен с риском заболевания сахарным диабетом типа 2.
У пациентов сначала возникает гиперинсулинемия, затем наступают резистентность к инсулину и гипергликемия.
Развитие сахарного диабета обусловлено прибавкой в весе, блокадой рецепторов серотонина 5-НТ2С и рецепторов гистамина Н1 повышением в крови уровня лептина (вырабатывается адипоцитами, стимулирует катаболизм липидов и тормозит их синтез).
Отмена нейролептиков приводит к обратному развитию сахарного диабета.
Наибольший диабетогенный эффект характерен для клозапина.
Применение нейролептиков противопоказано при болезни Паркинсона и лекарственном паркинсонизме, тяжелой депрессии, эпилепсии, выраженном церебральном склерозе, глаукоме, аденоме предстательной железы с расстройством мочеиспускания, гиперпролактинемии, сахарном диабете, порфирии, агранулоцитозе, аритмии, артериальной гипотензии, беременности.
Производные бензамида опасно назначать больным феохромоцитомой.
При лечении нейролептиками следует прекратить грудное вскармливание, воздерживаться от потенциально опасных видов деятельности, требующих высокой скорости и точности психических и двигательных реакций.
2.Антибиотики ( группы тетрациклина и левомицитина) – это продукты микробного происхождения, которые в ничтожно малых концентрациях способны убивать другие микроорганизмы.
Тетрациклины
К группе тетрациклинов относят природные и полусинтетические антибиотики, структурную основу которых составляют четыре конденсированных шестичленных кольца (рис. 17.17).
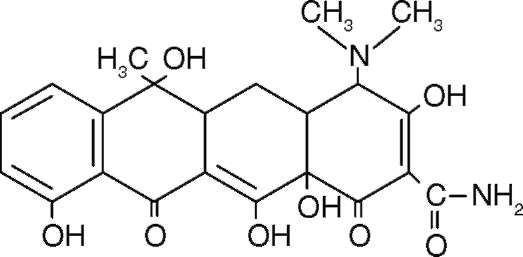
Рис. 17.17. Химическая структура тетрациклина
Тетрациклины классифицируют в зависимости от способа получения:
• природные (биосинтетические) антибиотики - тетрациклин, окситетрациклин;
• полусинтетические антибиотики - метациклин, доксициклин.
Тетрациклины угнетают синтез белков на уровне рибосом бактерий.
Тетрациклины связываются с 30S-субъединицей бактериальных рибосом, блокируя связывание аминоацил-тРНК с участком А на мРНК-рибосомном комплексе.
В результате нарушается присоединение последующих аминокислот к растущей полипептидной цепочке и приостанавливается процесс удлинения полипептида.
Тетрациклины проникают в грамотрицательные бактерии путем пассивной диффузии через белки порины наружной мембраны, после которой следует активный (энергозависимый) транспорт через внутреннюю цитоплазматическую мембрану.
Проникновение в грамположительные бактерии, такие как возбудитель сибирской язвы, происходит аналогичным образом с помощью энергозависимой транспортной системы.
В отличие от бактерий, в клетках млекопитающих отсутствует система активного транспорта тетрациклинов.
Механизм проникновения тетрациклинов в клетку объясняет избирательность действия антибиотиков на клетки бактерий.
Тетрациклины - антибиотики широкого спектра с бактериостатическим характером действия, наиболее активны в отношении размножающихся микроорганизмов.
Высокая степень липофильности обеспечивает хорошую всасываемость препаратов в ЖКТ, способность преодолевать биологические барьеры, накапливаться в тканях, проникать внутрь клеток и воздействовать на внутриклеточных возбудителей - хламидий, легионелл, микоплазм, риккетсий.
Важная особенность фармакокинетики этой группы антибиотиков - способность связывать в хелатные комплексы двух- и трехвалентные ионы (железа, кальция, магния, цинка, алюминия).
Ионы кальция могут содержаться в молочных продуктах, ионы кальция, алюминия - в антацидах.
Во избежание нарушения всасывания тетрациклины, как правило, принимают натощак.
Взаимодействие антибиотиков с катионами, в частности с кальцием, может привести к секвестрации препаратов в костях и зубах, что потенциально ведет к аномалиям развития и нежелательному прокрашиванию костной ткани и зубов у пациентов детского возраста.
По этой причине тетрациклины не следует назначать детям до 8 лет и беременным.
Изменение окраски зубов происходит вследствие способности тетрациклинов поглощать волны ультрафиолетового спектра.
Тетрациклины могут вызвать значительную фотосенсибилизацию кожи.
Длительность антибактериального действия тетрациклинов неодинакова.
По этому признаку среди них следует различать:
• тетрациклины короткого действия (6-8 ч) - тетрациклин и окситетрациклин;
• тетрациклины длительного действия (12-24 ч) - метациклин и доксициклин.
Побочные эффекты:
• аллергические реакции - кожная сыпь, крапивница, отек Квинке и анафилактический шок;
• раздражающее действие на слизистые оболочки пищеварительного тракта (тошнота, рвота, боли в животе, метеоризм, диарея) при пероральном применении, а при внутривенном введении - тромбофлебиты;
• гепатотоксическое действие;
• нарушение образования скелета, желтое или серо-коричневое окрашивание и повреждение зубов;
• дисбактериоз и суперинфекция с развитием кандидамикоза и псевдомембранозного энтероколита;
• фотосенсибилизация.
По сравнению с другими тетрациклинами лишь небольшая часть доксициклина выводится через почки, что делает этот препарат безопасным для применения у пациентов с почечной недостаточностью.
Доксициклин также выделяется с калом, в основном в неактивной форме, поэтому минимально изменяет кишечную флору.
Таким образом, использование доксициклина связано с более низкой частотой появления тошноты, рвоты и суперинфекции, чем у других тетрациклинов, особенно у иммунокомпрометированных больных.
К группе тетрациклинов относят природные и полусинтетические антибиотики, структурную основу которых составляют четыре конденсированных шестичленных кольца
Тетрациклины. |
|
Классификация: |
1. Биосинтетические - окситетрациклина дигидрат (террамицин, тетран, тархоцин), тетрациклин (десхлорбиомицин), демеклоциклин. 2. Полусинтетические - метациклина гидрохлорид (рондомицин), доксициклина гидрохлорид (вибрамицин), миноциклин. |
Механизм действия: |
Угнетение внутриклеточного синтеза белка рибосомами бактерий; связывание Me (Mg2+, Ca2+) с образованием хелатных соединений и ингибирование ферментных систем.
Тетрациклины угнетают синтез белков на уровне рибосом бактерий.
Тетрациклины связываются с 30S-субъединицей бактериальных рибосом, блокируя связывание аминоацил-тРНК с участком А на мРНК-рибосомном комплексе.
В результате нарушается присоединение последующих аминокислот к растущей полипептидной цепочке и приостанавливается процесс удлинения полипептида. Тетрациклины проникают в грамотрицательные бактерии путем пассивной диффузии через белки порины наружной мембраны, после которой следует активный (энергозависимый) транспорт через внутреннюю цитоплазматическую мембрану.
|
Характер противомикробного действия: |
антибиотики широкого спектра с бактериостатическим характером действия, наиболее активны в отношении размножающихся микроорганизмов.
|
Фармакодинамика: |
Широкий спектр действия. Чувствительны – Грам+ и Грам- кокки, возбудители бациллярной дизентерии, брюшного тифа, патогенные спирохеты, возбудители ООИ – чумы, туляремии, бруцеллеза, холеры; риккетсии, хламидии, простейшие (возбудители амебной дизентерии). Нечувствительны – протеи, синегнойная палочка, истинные вирусы и патогенные грибы. |
Фармакокинетика: |
Пути введения – внутрь, паренетреально (в/м, в/в, в полости тела), местно (ЛФ – мази). Периодичность введения – 4-8 ч. Всасывание – из желудка, тонкой кишки (неполная абсорбция, но достаточная для создания бактериостат. Со). Max Co в плазме крови – спустя 2-4 ч. Хар-но образование неабсорбируемых хелатных соединений с Ca2+, Fe2+, Al3+ - нарушение всасывания тетрациклинов при содержании в пище этих ионов (Са2+ в молоке, молочных продуктах) или в составе ЛС (антацидные средства). Исключение – доксициклин, миноциклин. Связь с белками плазмы – 20-80%. По длительности действия: демеклоциклин > доксициклин > метациклин > окситетрациклин > тетрациклин. Способны проникать сквозь ткани, в т.ч. через ТПБ. Немного – через ГЭБ (при введении внутрь – в высоких дозах). Депонирование в печени и костях. Выделение – с мочой и желчью (NB! Повторное всасывание из тонкой кишки). |
Показания к применению: |
Риккетсиозы, сыпной тиф, пневмония, вызванная микоплазмами, инфицирование хламидиями (пневмония, пситтакоз, трахома), гонорея, сифилис, возвратный тиф, бруцеллез, туляремия, холера, бациллярная и амебная дизентерия, кокковая инфекция, лептоспирозы. Развитие устойчивости микроорг-в к пенициллинам или стрептомицину, сенсибилизация больного к ним. |
Побочные эффекты: |
1. Аллергические реакции – поражение кожных покровов (фотосенсибилизация (демеклоциклин) и дерматиты), легкая лихорадка – редко; 2. Неаллергические реакции – диспепсические явления (тошнота, рвота, диарея), глоссит, стоматит вследствии раздражающего действия (окситетрациклин) на слизистую ЖКТ; болезненность инъекций, тромбофлебиты. - Гепатотоксичность (окситетрациклин). - С осторожностью – во 2-й половине беременности, детям (за счет депонирования в костной ткани, зубах – нарушение формирования скелета, окрашивание и повреждение зубов). - Влияние на обмен в-в: угнетение синтеза белка (антианаболическое действие), ↑ выведения Na+, H2O, АК, vit. - Вестибулярные расстройства (миноциклин). - Суперинфекция (за счет подавления сапрофитной флоры ЖКТ – кандидамикоз (лечение – сочетание ТЦ с нистатином, витаминами гр. В), инфекция стафилококками (энтероколит, пневмония), протеем, синегнойной палочкой, недостаточность витаминов группы В); псевдомембранозный колит (лечение – ванкомицин). - Постепенное развитие резистентности микроорганизмов. |
Левомицетин
Основной представитель группы – левомицетин (хлорамфеникол) – выделен в 1947 г., а спустя два года был налажен его синтез в промышленных масштабах.
Левомицетин является ингибитором синтеза белка в микробных клетках. Он избирательно связывается с большой субъединицей рибосом, ингибирует фермент пептидилтрансферазу и прекращает удлинение полипептидных цепей. Левомицетин оказывает бактериостатический эффект в фазе активного роста микроорганизмов. На некоторые высокочувствительные штаммы бактерий может оказывать бактерицидное действие.
Спектр противомикробного действия левомицетина весьма широк, но в полной мере реализовать его в медицине не удается из‑за высокой токсичности антибиотика. Область применения левомицетина сегодня значительно сузилась, и его следует рассматривать как антибиотик резерва. Левомицетин подавляет рост большинства штаммов пневмококков, стрептококков, стафилококков, менингококков, гемофильной палочки, бруцелл, риккетсий, хламидий, микоплазм, холерного вибриона. К нему чувствительны многие штаммы кишечной палочки, шигелл, сальмонелл, энтеробактера. Важным достоинством антибиотика является выраженное ингибирование роста анаэробов – бактероидов, фузобактерий, анаэробных кокков.
Резистентность микроорганизмов к левомицетину развивается медленно. Роста микробной устойчивости к нему не отмечается вследствие сравнительно редкого в последнее время применения.
При приеме внутрь левомицетин хорошо всасывается из ЖКТ, легко проникает в различные органы и жидкие среды организма. Высокие концентрации антибиотика создаются в ликворе. До 75 – 80 % принятой дозы подвергаются биотрансформации в печени, метаболиты выводятся почками; 5 – 10 % антибиотика выводится с мочой в неизмененном виде.
Показания к применению определяются с учетом опасности возникновения тяжелых, порой фатальных осложнений, связанных прежде всего с поражением аппарата кроветворения. Поэтому левомицетин назначают сегодня только при заболеваниях, которые:
а) опасны для жизни и вызваны микробами с частой устойчивостью к менее токсичным антибиотикам;
б) протекают на фоне непереносимости больными (аллергии, нарушения почечной функции и т. п.) других препаратов;
в) вызваны возбудителями с заведомо высокой чувствительностью к левомицетину.
С учетом всех этих условий левомицетин рассматривается как антибиотик выбора (в сочетании с ампициллином) при лечении брюшного тифа, менингитов и тяжелых пневмоний, вызванных гемофильной палочкой, сепсиса, вызванного бактероидами и другими анаэробами, при тяжелой риккетсиозной инфекции (сыпной тиф), устойчивой к тетрациклинам; его иногда применяют местно при лечении трахомы, раневых и ожоговых инфекций глаз, гнойных ран, фурункулеза.
Для лечения гнойничковых поражений кожи, фурункулеза, ожогов, трещин, при гнойной раневой инфекции – в виде 10 % линимента, синтомицинового линимента (1 %, 5 %, 10 %), а также в составе комбинированных препаратов: мазей «ируксол», «левосин», «левомеколь»; аэрозолей «левовинизоль», «олазоль».
Побочные эффекты левомицетина многочисленны. Наблюдается нейтропения, лимфопения, анемия, в том числе гемолитическая, тромбоцитопения с повышенной кровоточивостью. В сравнительно редких случаях развивается фатальная апластическая анемия вследствие аплазии костного мозга. Это осложнение не поддается терапии и является серьезным доводом за исключение левомицетина везде, где он может быть заменен другими химиотерапевтическими средствами.
Наиболее опасными из них являются угнетение кроветворения и так называемый «серый синдром» (у новорожденных).
Токсичность левомицетина выражена сильнее у новорожденных с низкой активностью фермента (глюкуронилтрансферазы), участвующего в инактивации антибиотика в печени, вследствие чего препарат может накапливаться в организме и вызывать «серый синдром» (гипотермия, гипотония, бледность кожных покровов, срыгивание); летальность младенцев в первые 24 – 48 ч достигает 40 %. Синдром наблюдается при лечении большими дозами (выше 50 мг/кг в сутки) левомицетина.
Левомицетин обладает очень горьким вкусом и может вызывать тошноту, рвоту, понос.
Иногда наблюдаются осложнения, связанные с химиотерапевтическим эффектом: реакция обострения вследствие массового распада микробных клеток и освобождения эндотоксинов (при лечении брюшного тифа, бруцеллеза), дисбактериоз кишечника, кандидоз, суперинфекция (синегнойной палочкой, устойчивыми штаммами стафилококка).
3.Антигипертензивные средства, влияющие на ренин-ангиотензин-альдостероновую систему Гипотензивные средства, влияющие на РААС, снижают АД за счёт изменений в системной гуморальной регуляции АД.
Ренин-ангиотензиновая система (РАС) играет важную роль в регуляции АД, сердечной деятельности, водно-электролитного баланса.
Ее активность возрастает при артериальной гипертензии, хронической сердечной недостаточности и диабетической нефропатии.
При остром инфаркте миокарда активность РАС повышается уже в первые сутки, при осложненном течении инфаркта чрезмерная активация РАС сохраняется длительно после выписки больного из стационара.
Высокая активность ренина и повышенное содержание ангиотензина II в крови являются показателями неблагоприятного прогноза у пациентов с сердечно-сосудистыми заболеваниями.
Известно, что ангиотензин II относится к наиболее активным эндогенным вазопрессорным веществам и, кроме того, принимает участие в регуляции продукции альдостерона (рис. 14.12).
Поэтому и возникла идея создания веществ, угнетающих ренин-ангиотензиновую систему.
Одно направление исследований связано с поиском веществ, снижающих содержание в плазме протеолитического фермента ренина (образуется в почках, в юкстагломерулярных клетках), который обеспечивает превращение ангиотензиногена в ангиотензин I (оба вещества не обладают активностью).
В дальнейшем из ангиотензина I образуется вазоактивный ангиотензин II.
Из ангиотензина II образуется ангиотензин III.
Оба соединения имеют сходную направленность действия.
Однако ангиотензин II в 4 раза превосходит ангиотензин III по вазопрессорному эффекту.
Вместе с тем, по стимулирующему влиянию на продукцию альдостерона они равноценны.
Естественно, что вещества, угнетающие продукцию ренина, должны быть наиболее эффективны при повышенном его высвобождении.
Последнее возникает в следующих ситуациях:
- при снижении давления и уменьшении объема крови в афферентных артериолах почечных клубочков;
- при снижении содержания NaCl в дистальных канальцах почек (сигнал идет от эпителиальных клеток плотного пятна - macula densa - к юкстагломерулярным клеткам, с которыми они контактируют);
- при повышении тонуса адренергической иннервации;
- при повышенной продукции простациклина и простагландина Е2.
Исходя из этих данных, продукцию ренина можно уменьшить, понижая тонус адренергической иннервации.
Это можно осуществить как за счет снижения центрального симпатического тонуса (клофелин, метилдофа), так и путем блокады передачи импульсов на уровне пресинаптических окончаний (октадин, резерпин) и β1-адренорецепторов (анаприлин и др.).
В гипотензивном действии указанных нейротропных препаратов снижение выделения ренина может иметь определенное значение, но обычно оно небольшое.
Снижение продукции ренина наблюдается также при угнетении синтеза простагландинов (простациклина, ПГЕ2), которые стимулируют образование и высвобождение ренина.
Таким эффектом обладают нестероидные противовоспалительные средства (индометацин и др.), ингибирующие циклооксигеназу и благодаря этому подавляющие биосинтез простагландинов.
Имеются препараты, которые оказывают прямое ингибирующее действие на ренин (эналкирен, ремикирен), снижая его активность.
Действие этой очень важной группы антигипертензивных средств нацелено на нейтрализацию конечных эффектов ренина почек, опосредованных через ангиотензин II.
Протеолитический фермент — ренин — секретируется юкстагломерулярным аппаратом почек (клетками в области афферентных артерий клубочков) и способен гидролизовать относительно крупные белки плазмы.
Тем самым включается сложная цепь биохимических реакций с участием присутствующего в плазме АПФ.
Последний отщепляет от биологически неактивного ангиотензина I две аминокислоты, превращая его в высокоактивный ангиотензин II (рис. 18).
Функция АПФ не ограничивается образованием ангиотензина II, он осуществляет параллельно инактивацию физиологического вазодилататора брадикинина, роль которого в регуляции АД невелика, но полезна (он расширяет периферические артериолы).
С участием серии пептидаз ангиотензин II быстро переходит в менее активный ангиотензин III и неактивные фрагменты.
АПФ обнаружен не только в плазме крови, он присутствует в эндотелии сосудов, в миокарде и мозгу, где также активирует образование ангиотензина II.
Ренин-ангиотензиновой системе (РАС) отводят очень важную роль в патогенезе ГБ, сердечной недостаточности и ряда других патологических состояний.
Ее вовлечение в реакции осуществляется через симпатическую иннервацию (β1-адренорецепторы в юкстагломерулярных клетках) и, видимо, посредством иных, в том числе местных, механизмов осмо- и волюморецепторов.
Любые фармакологические и другие сдвиги, ведущие прямо или рефлекторно к повышению тонуса симпатической иннервации, сопровождаются усилением секреции ренина; она активируется при снижении уровня ангиотензина в крови и тормозится (механизм обратной связи) при его повышении.
Гипонатриемия и бедная поваренной солью диета также являются сильными активаторами секреции ренина.
Большой интерес представляют препараты, ингибирующие ангиотензинпревращающий фермент.
Последний является пептидилдипептидгидролазой (кининаза II).
Образуется в эндотелии сосудов, в легких, почках и других периферических тканях.
Этот фермент способствует превращению ангиотензина I в высокоактивный ангиотензин II.
Для фармакологической блокады РАС используют ингибиторы ангиотензинпревращающего фермента и непептидные антагонисты рецепторов ангиотензина II.
Ингибиторы АПФ были введены в широкую практику лечения ГБ в середине 1980-х гг. и сегодня занимают равное место с блокаторами кальциевых каналов, диуретиками и β-адреноблокаторами.
Изучение механизма гипотензивного эффекта иАПФ показало следующие его аспекты:
1. Основное значение имеет снижение образования в кровеносном русле сильнейшего сосудосуживающего вещества — ангиотензина II, тем самым предупреждается не только его прямое действие на артериолы, но и активация им высвобождения норадреналина из симпатических терминалей.
Эффект проявляется быстрым и стойким снижением ОПС и системного АД.

Рис. 14.12. Значение ренин-ангиотензиновой системы в регуляции артериального давления и локализация действия ряда гипотензивных средств.
Кроме того, уменьшается секреция надпочечниками альдостерона, который способствует задержке натрия и воды в организме (продукция альдостерона у больных ГБ обычно повышена).
При применении иАПФ наблюдается временное усиление выделения натрия и воды (этому способствует и увеличение почечного кровотока), в результате чего несколько снижается ОЦК, однако диуретический эффект начинает исчезать примерно через два-три месяца приема препаратов.

Рис. 18. Схема ренин-ангиотензиновой системы.
Пути фармакологического воздействия на функции системы:
АТ-II — ангиотензин-II; AT1 — ангиотензиновые рецепторы 1-го типа
2. Дополнительным механизмом действия иАПФ является торможение инактивации брадикинина.
Брадикинин разрушается ферментом киназой II, который идентичен АПФ.
Ингибируя этот фермент, иАПФ увеличивают концентрацию брадикинина, обладающего сосудорасширяющим действием, что усиливает гипотензивное действие препаратов.
3. Определенную положительную роль играет торможение под влиянием иАПФ системы ренин-ангиотензина в разных тканях (мозг, легкие, миокард и др.) и в стенке сосудов.
В небольших количествах иАПФ проникают в ЦНС, тем не менее они снижают тонус центров симпатической иннервации без подавления рефлекторной регуляции АД (поэтому ортостатической гипотензии не наблюдается).
Более существенное значение имеет, видимо, предотвращение образования ангиотензина II в эндотелиальных клетках сосудов, что устраняет локальное вазоконстрикторное действие этого фактора.
При систематическом применении иАПФ постепенно уменьшают гипертрофию миокарда (возникновение этого явления отчасти связывают с ангиотензином II).
Классификация:
1. Ингибиторы ангиотензинпревращающего фермента
- Первое поколение
Каптоприл (капотен)
- Второе поколение
Эналаприл (ренитек, энам, энап)
Эналаприлат (энап)
Лизиноприл (диротон, лизмнотон)
Рамиприл (томудекс)
Периндоприл (Престариум)
Спираприл (квадроприл)
Фозиноприл (моноприл)
Хинаприл (Аккупро)
Цилсуаприл (инхибейс)
Беназеприл (лотензин)
Моэксиприл (моэкс 15, моэкс 7,5)
2. Блокаторы ангиотензиновых рецепторов
Эпросартан (теветен)
Лозартан (козаар)
Вальсартан (диован)
Телмисартан (микардис)
Кондесартан (атакан)
