
- •Практикум по токсикологической химии
- •Часть I
- •Введение
- •Настоящее пособие построено на основе материалов, используемых при проведении практических работ по токсикологической химии студентов заочного отделений фармацевтического факультета двгму.
- •Тема 1 хта группы веществ, изолируемых минерализацией («металлические яды»)
- •Раздел 1. Изолирование «металлических» ядов из биологического материала
- •1.1. Минерализация биологического материала смесью
- •1.2. Минерализация биологического материала смесью серной, азотной и хлорной кислот (метод Каана)
- •1.3. Денитрация минерализата
- •1.4. Минерализация перекисью водорода и концентрированной серной кислотой
- •1.5. Метод сухого озоления
- •1.6. Метод сплавления
- •1.7. Деструкция на ртуть
- •1.8. Подготовка минерализата к анализу.
- •Тестовые задания
- •Раздел 2. Дробный метод анализа « металлических» ядов
- •2.1. Качественные реакции на катионы металлов
- •2.1.1. Качественное обнаружение иона свинца
- •2.1.2. Качественное обнаружение иона бария
- •2.1.3. Качественное обнаружение иона марганца
- •2.1.4. Качественное обнаружение иона хрома
- •2.1.5. Качественное обнаружение иона серебра
- •2.1.6. Качественное обнаружение иона меди
- •2.1.7. Качественное обнаружение иона цинка
- •2.1.8. Качественное обнаружение иона висмута
- •2.1.9. Качественное обнаружение ионов сурьмы
- •2.1.10. Качественное обнаружение ионов таллия
- •2.1.11. Качественное обнаружение иона кадмия
- •2.1.12. Качественное обнаружение иона мышьяка
- •Контрольные вопросы
- •Тестовые задания
- •Тема 2 хта группы веществ, изолируемых дистилляцией ( «летучие» яды)
- •Раздел 1 . Микродиффузия
- •1.1. Определение этилового спирта методом микродиффузии
- •1.2. Обнаружение формальдегида
- •1.3. Обнаружение ацетона
- •1.4. Обнаружение фенолов
- •Раздел 2. Изолирование «летучих» ядов дистилляцией с водяным паром
- •Раздел 3. Химический анализ «летучих» ядов
- •3.1.Качественное обнаружение синильной кислоты
- •3.2. Качественное обнаружение галогенпроизводных алифатического ряда (хлороформа и хлоралгидрата)
- •3.3. Качественное обнаружение формальдегида
- •3.4. Качественное обнаружение метилового спирта
- •3.5. Качественное обнаружение изоамилового спирта
- •3.6. Качественное обнаружение этилового спирта
- •3.7. Качественное обнаружение ацетона
- •3.8. Качественное обнаружение этиленгликоля
- •3.9. Качественное обнаружение уксусной кислоты
- •3.10. Качественное обнаружение фенола
- •2. Реакция образования трибромфенола
- •4. Реакция Либермана
- •3.11. Качественное обнаружение анилина
- •3.12. Количественное фотоколориметрическое определение формальдегида в дистилляте. В основу этого метода положена способность формальдегида образовывать окрашенный продукт с фуксинсернистой кислотой.
- •Раздел 4. Гжх метод анализа «летучих» ядов
- •4.1.Гжх определение спиртов алифатического ряда алкилнитритным методом.
- •4.1.1.Качественное определение.
- •4.1.2.Количественный анализ
- •4.2. Методика гжх-анализа « летучих» ядов Международного совета по систематическому химико-токсикологическому анализу
- •4.3. Методика гжх-анализа «летучих» ядов Московского городского бсмэ.
- •Контрольные вопросы
- •Тестовые задания
- •Тз 15. Общая реакция для обнаружения ацетона и этанола
- •Тема 3 Группа веществ, изолируемых водой с последующей очисткой диализом
- •Раздел 1. Изолирование кислот, оснований и солей из биологического материала
- •Раздел 2.Качественное определение кислот, щелочей и солей
- •2.1. Качественное определение соляной кислоты
- •2.2. Качественное определение азотной кислоты
- •2.3. Качественное определение серной кислоты
- •2.4. Качественное определение кон
- •2.5. Качественное определение NaOh
- •2.6. Качественное определение аммиака
- •2.7. Качественное обнаружение нитритов
- •Контрольные вопросы
- •Тестовые задания
- •Тема 4 Группа веществ, не требующих изолирования. Химико-токсикологический анализ на угарный газ
- •Раздел 1. Качественный анализ на угарный газ
- •1.1. Химический метод.
- •1.2. Метод микродиффузии.
- •1.3. Спектроскопический метод
- •Раздел 2.Количественное определение карбоксигемоглобина в крови
- •2.1.Спектрофотометрический метод
- •Контрольные вопросы
- •Тестовые задания
- •Список литературы
- •Оглавление
- •Тема 1.Хта группы веществ, изолируемых минерализацией
- •Раздел 1. Изолирование «металлических» ядов из биологического материала……………………………………………………………………..9
- •Раздел 2.Дробный метод анализа «металлических» ядов………….17
- •Раздел 4.Гжх метод анализа «летучих» ядов………………………..50
- •Тема 3. Группа веществ, изолируемых водой с последующей очисткой диализом………………………………………………………………..56
- •Раздел 1. Изолирование кислот, оснований и солей из биологического материала…………………………………………………………….57
- •Раздел 2. Качественное определение кислот, щелочей и солей….58
- •Тема 4. Группа веществ, не требующих изолирования. Химико-токсикологический анализ на угарный газ……………………………...63
- •Раздел 1.Качественный анализ на угарный газ……………………….64
- •Раздел 2. Количественное определение карбоксигемоглобина в крови………………………………………………………………………………66
4. Реакция Либермана
1-2 капли исследуемого раствора вносят в фарфоровую чашку и выпаривают досуха. К сухому остатку прибавляют каплю 1% свежеприготовленного раствора нитрита натрия в H2SO4 конц. и смесь оставляют на несколько минут. После охлаждения смеси по каплям прибавляют 4н NaOH до щелочной реакции (по лакмусу). При наличии фенола в пробе появляется синяя окраска, переходящая в красную, а затем в зелёную.

5. Реакция с бензальдегидом
В пробирку вносят 0,5 мл исследуемого
раствора и 2 мл H2SO4
конц. и 1-2 капли бензальдегида. При
нагревании смеси до кипения появляется
тёмно-красное окрашивание. После
охлаждения смеси добавляют к ней 10 мл
воды и 10% NaOH
до щелочной реакции по лакмусу. Окраска
переходит в сине-фиолетовую. При
взбалтывании этого раствора с хлороформом
окраска переходит в органический слой.
пробирку вносят 0,5 мл исследуемого
раствора и 2 мл H2SO4
конц. и 1-2 капли бензальдегида. При
нагревании смеси до кипения появляется
тёмно-красное окрашивание. После
охлаждения смеси добавляют к ней 10 мл
воды и 10% NaOH
до щелочной реакции по лакмусу. Окраска
переходит в сине-фиолетовую. При
взбалтывании этого раствора с хлороформом
окраска переходит в органический слой.
3.11. Качественное обнаружение анилина
1. Реакция образования анилинового черного
1 мл исследуемого раствора смешивают с 2-3 каплями 10% H2SO4 и 10% K2Cr2O7. При наличии анилина образуется чёрное окрашивание вследствие образования анилинового чёрного – сложной смеси продуктов окисления анилина.
2. Реакция образования азокрасителя
К 2 мл исследуемого раствора добавляют
10% раствор HCl
и NaNO2
насыщенный до посинения йодкрахмальной
бумаги, затем добавляют несколько капель
щелочного раствора -нафтола.
При наличии анилина наблюдается появление
красной окраски. Окраска переходит в
органический слой.
2 мл исследуемого раствора добавляют
10% раствор HCl
и NaNO2
насыщенный до посинения йодкрахмальной
бумаги, затем добавляют несколько капель
щелочного раствора -нафтола.
При наличии анилина наблюдается появление
красной окраски. Окраска переходит в
органический слой.

3. Реакция образования триброманилина
К 1 мл исследуемого раствора добавляют насыщенный раствор бромной воды. При наличии анилина образуется белый осадок.

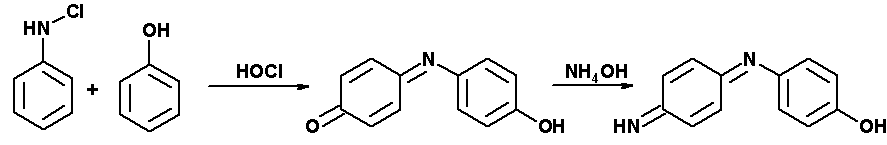
4. Реакция образования индофенола
К 1-2 мл исследуемого раствора добавить 2 мл хлорной извести и 1 каплю фенола. При наличии анилина появляется грязно-фиолетовая окраска, которая при добавлении 10% раствора аммиака переходит в индигово-синюю.

3.12. Количественное фотоколориметрическое определение формальдегида в дистилляте. В основу этого метода положена способность формальдегида образовывать окрашенный продукт с фуксинсернистой кислотой.
Готовят стандартный раствор формальдегида с содержанием его 2 мг в 1 мл. Для построения калибровочного графика готовят серию разведений. В ряд пробирок из бесцветного стекла вносят 0,05, 0,1, 0,2, 0,3, 0,4, 0,5 мл стандартного раствора формальдегида. Во все пробирки наливают Н2О дистиллированную до 5 мл, а затем добавляют по 1 мл 25% раствора серной кислоты и 1 мл фуксинсернистой кислоты. Одновременно с приготовлением шкалы готовят одну пробирку для контроля – в нее наливают 5 мл Н2О дистиллированной и одну пробирку с исследуемой пробой – в нее наливают 5 мл исследуемого раствора. В обои пробирки добавляют по 1 мл 25% раствора серной кислоты и фуксинсернистой кислоты.
Заключение о количественном содержании формальдегида делают через 1 минуту путем ФЭК определения сначала серии разведений при =540 нм с измерением оптической плотности и построением калибровочного графика. Затем измеряется оптическая плотность исследуемого раствора.
Метод применим для малых количеств формальдегида.

