
- •Практикум по токсикологической химии
- •Часть I
- •Введение
- •Настоящее пособие построено на основе материалов, используемых при проведении практических работ по токсикологической химии студентов заочного отделений фармацевтического факультета двгму.
- •Тема 1 хта группы веществ, изолируемых минерализацией («металлические яды»)
- •Раздел 1. Изолирование «металлических» ядов из биологического материала
- •1.1. Минерализация биологического материала смесью
- •1.2. Минерализация биологического материала смесью серной, азотной и хлорной кислот (метод Каана)
- •1.3. Денитрация минерализата
- •1.4. Минерализация перекисью водорода и концентрированной серной кислотой
- •1.5. Метод сухого озоления
- •1.6. Метод сплавления
- •1.7. Деструкция на ртуть
- •1.8. Подготовка минерализата к анализу.
- •Тестовые задания
- •Раздел 2. Дробный метод анализа « металлических» ядов
- •2.1. Качественные реакции на катионы металлов
- •2.1.1. Качественное обнаружение иона свинца
- •2.1.2. Качественное обнаружение иона бария
- •2.1.3. Качественное обнаружение иона марганца
- •2.1.4. Качественное обнаружение иона хрома
- •2.1.5. Качественное обнаружение иона серебра
- •2.1.6. Качественное обнаружение иона меди
- •2.1.7. Качественное обнаружение иона цинка
- •2.1.8. Качественное обнаружение иона висмута
- •2.1.9. Качественное обнаружение ионов сурьмы
- •2.1.10. Качественное обнаружение ионов таллия
- •2.1.11. Качественное обнаружение иона кадмия
- •2.1.12. Качественное обнаружение иона мышьяка
- •Контрольные вопросы
- •Тестовые задания
- •Тема 2 хта группы веществ, изолируемых дистилляцией ( «летучие» яды)
- •Раздел 1 . Микродиффузия
- •1.1. Определение этилового спирта методом микродиффузии
- •1.2. Обнаружение формальдегида
- •1.3. Обнаружение ацетона
- •1.4. Обнаружение фенолов
- •Раздел 2. Изолирование «летучих» ядов дистилляцией с водяным паром
- •Раздел 3. Химический анализ «летучих» ядов
- •3.1.Качественное обнаружение синильной кислоты
- •3.2. Качественное обнаружение галогенпроизводных алифатического ряда (хлороформа и хлоралгидрата)
- •3.3. Качественное обнаружение формальдегида
- •3.4. Качественное обнаружение метилового спирта
- •3.5. Качественное обнаружение изоамилового спирта
- •3.6. Качественное обнаружение этилового спирта
- •3.7. Качественное обнаружение ацетона
- •3.8. Качественное обнаружение этиленгликоля
- •3.9. Качественное обнаружение уксусной кислоты
- •3.10. Качественное обнаружение фенола
- •2. Реакция образования трибромфенола
- •4. Реакция Либермана
- •3.11. Качественное обнаружение анилина
- •3.12. Количественное фотоколориметрическое определение формальдегида в дистилляте. В основу этого метода положена способность формальдегида образовывать окрашенный продукт с фуксинсернистой кислотой.
- •Раздел 4. Гжх метод анализа «летучих» ядов
- •4.1.Гжх определение спиртов алифатического ряда алкилнитритным методом.
- •4.1.1.Качественное определение.
- •4.1.2.Количественный анализ
- •4.2. Методика гжх-анализа « летучих» ядов Международного совета по систематическому химико-токсикологическому анализу
- •4.3. Методика гжх-анализа «летучих» ядов Московского городского бсмэ.
- •Контрольные вопросы
- •Тестовые задания
- •Тз 15. Общая реакция для обнаружения ацетона и этанола
- •Тема 3 Группа веществ, изолируемых водой с последующей очисткой диализом
- •Раздел 1. Изолирование кислот, оснований и солей из биологического материала
- •Раздел 2.Качественное определение кислот, щелочей и солей
- •2.1. Качественное определение соляной кислоты
- •2.2. Качественное определение азотной кислоты
- •2.3. Качественное определение серной кислоты
- •2.4. Качественное определение кон
- •2.5. Качественное определение NaOh
- •2.6. Качественное определение аммиака
- •2.7. Качественное обнаружение нитритов
- •Контрольные вопросы
- •Тестовые задания
- •Тема 4 Группа веществ, не требующих изолирования. Химико-токсикологический анализ на угарный газ
- •Раздел 1. Качественный анализ на угарный газ
- •1.1. Химический метод.
- •1.2. Метод микродиффузии.
- •1.3. Спектроскопический метод
- •Раздел 2.Количественное определение карбоксигемоглобина в крови
- •2.1.Спектрофотометрический метод
- •Контрольные вопросы
- •Тестовые задания
- •Список литературы
- •Оглавление
- •Тема 1.Хта группы веществ, изолируемых минерализацией
- •Раздел 1. Изолирование «металлических» ядов из биологического материала……………………………………………………………………..9
- •Раздел 2.Дробный метод анализа «металлических» ядов………….17
- •Раздел 4.Гжх метод анализа «летучих» ядов………………………..50
- •Тема 3. Группа веществ, изолируемых водой с последующей очисткой диализом………………………………………………………………..56
- •Раздел 1. Изолирование кислот, оснований и солей из биологического материала…………………………………………………………….57
- •Раздел 2. Качественное определение кислот, щелочей и солей….58
- •Тема 4. Группа веществ, не требующих изолирования. Химико-токсикологический анализ на угарный газ……………………………...63
- •Раздел 1.Качественный анализ на угарный газ……………………….64
- •Раздел 2. Количественное определение карбоксигемоглобина в крови………………………………………………………………………………66
3.3. Качественное обнаружение формальдегида
1. Реакция с фуксинсернистой кислотой
1 мл исследуемого раствора смешивают в фарфоровой чашке с 5 мл концентрированной H2SO4 и после охлаждения добавляют 1 мл фуксинсернистой кислоты. При наличии формальдегида появляется синее или сине-фиолетовое окрашивание.

2. Реакция с реактивом Фелинга
2 мл исследуемого раствора смешивают с 2 мл 10% раствора NaOH и 5 каплями реактива Фелинга. Смесь осторожно нагревают. При наличии формальдегида появляется осадок желтого цвета, переходящий в красный.
4K2Na2[Cu(C4H3O6)2] + CH2O + 3H2O → 2Cu2O↓ + 8KNaC4H4O6 + CO2
3. Реакция с раствором резорцина в щелочной среде
К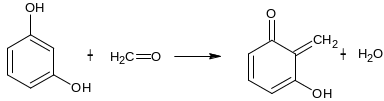 1 мл дистиллята добавляют 1 мл 1% раствора
резорцина в 10% растворе NaOH,
нагревают на кипящей водяной бане 5-10
мин. При наличии формальдегида возникает
розовое или малиново-красное окрашивание.
1 мл дистиллята добавляют 1 мл 1% раствора
резорцина в 10% растворе NaOH,
нагревают на кипящей водяной бане 5-10
мин. При наличии формальдегида возникает
розовое или малиново-красное окрашивание.
4. Реакция восстановления окиси серебра
В пробирку вносят 5 капель 1% раствора нитрата серебра и по каплям 10% раствор аммиака. Образовавшийся бурый осадок должен раствориться в избытке аммиака. К полученной жидкости добавляют 1 мл исследуемой жидкости, и смесь осторожно нагревают в пламени горелки. При наличии формальдегида образуется черный осадок металлического серебра.
2[Ag(NH3)2]OH + CH2O → 2Ag↓ + HCOONH4 + 3NH3
5. Реакция с хромотроповой кислотой
К 1 мл дистиллята добавляют 0,2 мл 1% раствора хромотроповой кислоты в конц. серной кислоте, а затем 5 мл конц. серной кислоты и взбалтывают. При наличии формальдегида появляется фиолетовое окрашивание.

3.4. Качественное обнаружение метилового спирта
1. Реакция образования сложного эфира
1 мл исследуемого раствора смешивают с 0,03 г салициловой кислоты и двойным объемом концентрированной серной кислоты. При нагревании в присутствии метилового спирта ощущается запах метилового эфира салициловой кислоты.

2. Реакция окисления метилового спирта в формальдегид
К 5 мл исследуемого раствора добавляют 2-3 мл 10% раствора серной кислоты, и жидкость охлаждают под струей холодной воды. Затем по каплям добавляют 1% раствор перманганата калия до сохраняющейся светло-розовой окраски. Через 15-20 минут для обесцвечивания избытка перманганата калия добавляют по каплям 15% раствор щавелевой кислоты или 15% раствор сульфита натрия. При необходимости жидкость фильтруют и с фильтратом проделывают реакции, описанные для формальдегида.
CH3OH + [O] → CH2O + H2O
3.5. Качественное обнаружение изоамилового спирта
1. Реакция с п-диметиламинобензальдегидом в конц. H2SO4 (реакция Комаровского)
К исследуемому раствору в фарфоровой чашке добавляют 5-10 капель реактива. В присутствии изоамилового спирта раствор окрашивается в темно-красный цвет, при разбавлении водой он приобретает фиолетовую окраску.

2. Реакция окисления
2-3 мл исследуемого раствора помещают в пробирку и содержимое ее испаряют, к остатку добавляют несколько капель концентрированного раствора перманганата калия и равный объем концентрированной серной кислоты. В течение 1-2 минут пробирку нагревают на водяной бане, при наличии изоамилового спирта появляется едва уловимый приятный запах изовалерианового альдегида, а затем неприятный запах (гнилого сыра), присущий изовалериановой кислоте.
(CH3)2CHCH2CH2OH + [O] → (CH3)2CHCH2CHO + [O] → (CH3)2CHCH2COOH
3. Реакция получения изоамилацетата
2-3 мл исследуемого раствора помещают в фарфоровую чашку и содержимое ее испаряют. Остаток смешивают с 2 каплями концентрированной серной кислоты и небольшим избытком (0,03 г.) высушенного ацетата натрия. При слабом нагревании в присутствии изоамилового спирта ощущается характерный запах изоамилацетата (запах грушевой эссенции); запах становится резче, если реакционную смесь залить 20-25-кратным объемом воды.
(CH3)2CHCH2CH2OH + CH3COONa + H2SO4 → (CH3)2CHCH2CH2OC(O)CH3 + NaHSO4 + H2O
4. Реакция с салициловым альдегидом (реакция Комаровского)
2 -3
мл исследуемого раствора помещают в
фарфоровую чашку и содержимое ее
испаряют. К остатку добавляют 20-25 капель
1% раствора салицилового альдегида и 3
мл концентрированной серной кислоты.
По охлаждении содержимого чашки ее
помещают на 3 минуты на кипящую водяную
баню. Появляется розово–красное
окрашивание. При больших количествах
изоамилового спирта розово–красное
окрашивание появляется без нагревания.
Реакция не специфична. Предел обнаружения
1,5 мг изоамилового спирта в остатке.
-3
мл исследуемого раствора помещают в
фарфоровую чашку и содержимое ее
испаряют. К остатку добавляют 20-25 капель
1% раствора салицилового альдегида и 3
мл концентрированной серной кислоты.
По охлаждении содержимого чашки ее
помещают на 3 минуты на кипящую водяную
баню. Появляется розово–красное
окрашивание. При больших количествах
изоамилового спирта розово–красное
окрашивание появляется без нагревания.
Реакция не специфична. Предел обнаружения
1,5 мг изоамилового спирта в остатке.
