
6 курс / Клиническая фармакология / Кукес. Клиническая фармакология
.pdfПрепараты этой группы утратили свое положение в фармакотерапии респираторных заболеваний, но остаются незаменимы при ряде заболеваний, таких, как муковисцидоз и бронхоэктатиче-ская болезнь.
Ацетилцистеин. Эффект препарата связан с наличием в его молекуле свободной сульфгидрильной группы, которая расщепляет дисульфидные связи гликопротеинов слизи. В результате образуются дисульфиды М-ацетилцистеина, имеющие значительно меньшую молекулярную массу, и снижается вязкость мокроты. Длительное применение ацетилцистеина нецелесообразно, так как в целом он подавляет мукоцилиарный транспорт и продукцию секреторного IgA. При назначении ацетилцистеина необходимо обеспечить условия для адекватного удаления мокроты: постуральный дренаж, вибромассаж. При приеме внутрь препарат быстро и хорошо всасывается, в печени расщепляется до своего активного метаболита - цистеина. Максимальная концентрация в плазме крови достигается через 1-3 ч, период полувыведения препарата короткий - около 1 ч.
Эффект другого муколитика - карбоцистеина связан с активацией сиаловой трансферазы - фермента бокаловидных клеток слизистой оболочки бронхов, под влиянием которой замедляется продукция кислых муцинов и уменьшается вязкость мокроты.
Рекомбинантная α-ДНКаза. Вязкий гнойный секрет в дыхательных путях больных муковисцидозом содержит очень высокие концентрации внеклеточной ДНК, которая высвобождается из разрушающихся лейкоцитов. α-ДНКаза специфически расщепляет высокомолекулярные нуклеиновые кислоты и нуклеопротеиды до небольших и растворимых молекул, что способствует уменьшению вязкости мокроты, а также оказывает противовоспалительное действие. α-ДНКаза - генно-инженерный вариант природного фермента человека, который расщепляет внеклеточную ДНК. В норме ДНКаза присутствует в сыворотке человека. В терапевтических дозах ингаляции α- ДНКазы не вызывают повышения активности фермента в крови, что свидетельствует о малом системном всасывании или малой кумуляции. Препарат достаточно безопасен.
Бромгексин оказывает муколитическое (секретолитическое) и отхаркивающее действие, что связано с деполимеризацией и разрушением мукопротеинов и мукополисахаридов, входящих в состав мокроты, кроме того, препарат обладает незначительным противокашлевым действием. Активный метаболит бромгекси-на - амброксол существенно превосходит его по клинической эффективности. После приема внутрь амброксол быстро и полностью всасывается, но 20-30% препарата подвергается быстрому метаболизму в печени вследствие феномена «первого прохожде-
ния» через печень. Продолжительность действия после приема одной дозы составляет 6-12 ч. Препарат подвергается биотрансформации в печени: образуются дибромантраниловая кислота и глукуроновые конъюгаты.
20.11. СРЕДСТВА ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ ПРИ ИХ ИНГАЛЯЦИОННОМ ВВЕДЕНИИ
Ингаляционный путь введения ЛС при лечении заболеваний дыхательных путей имеет ряд дополнительных преимуществ:
-быстрое начало действия (ЛС поступает непосредственно в область рецепторов);
-высокая эффективность;
-высокий уровень безопасности (системные концентрации ЛС и, как следствие, выраженность НЛР - невелики).
В виде ингаляций наиболее часто назначают бронхолитики (Р2-адреномиметики и м-холиноблокаторы) и глюкокортикоиды для лечения бронхообструктивных заболеваний - БА, ХОБЛ; муколитики и антибактериальные препараты (например, фуза-фунгин® или гентамицин) для лечения хронических легочных инфекций.
История применения различных устройств для ингаляций ЛС насчитывает уже около 100 лет. Основным требованием к подобным устройствам считают оптимальный размер частиц аэрозоля, вдыхаемого больным. Диаметр таких частиц должен составлять 2-5 мкм, что обеспечивает их проникновение в область крупных и средних бронхов. Очень крупные (>5 мкм) частицы аэрозоля практически не поступают в бронхи, а их адсорбция в полости рта и глотки создает условия для всасывания ЛС в кровоток и появления системных эффектов. С другой стороны, очень мелкие частицы (<2 мкм) способны проникать в самые мелкие бронхи, что также сопровождается уменьшением клинического эффекта и увеличением системной концентрации ЛС. Кроме того, ингалятор должен быть прост в употреблении и по возможности быть более компактен.
Современный арсенал средств доставки ингаляционных ЛС можно разделить на несколько основных типов ингаляторов:
-аэрозольный дозированный ингалятор (АДИ);
-порошковый ингалятор (ПИ);
-небулайзер.
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
Аэрозольный дозированный ингалятор
Наиболее распространенная в настоящее время форма ингалятора. Позволяет распылять в виде аэрозоля различные ЛС. Его можно применять для доставки препаратов в легкие, носоглотку или полость носа (глюкокортикоиды). Основным недостатком АДИ считают необходимость координировать дыхательный маневр (интенсивный и равномерный вдох) с активацией ингалятора (нажатие пальцами на баллончик). Больного следует проинструктировать о том, что:
-ингаляции с помощью АДИ следует проводить сидя или стоя (но не лежа);
-перед использованием необходимо встряхнуть ингалятор;
-при вдохе губы больного должны плотно обхватить ингалятор;
-после завершения вдоха следует задержать дыхание на 5-10 с для обеспечения лучшей адсорбции аэрозоля.
Правильная техника ингаляций обеспечивает проникновение в бронхи около 15-20% (до 50% при использовании новых пропе-лентов, не содержащих фреон) дозы препарата, если же возникают ошибки в использовании этого АДИ, доля препарата, попавшего в бронхи, становится еще меньше.
Некоторые пациенты (дети, пожилые, лица со сниженным интеллектом или неврологическими нарушениями) испытывают проблемы при использовании АДИ, разрешить которые можно применяя спей-сер или ингалятор «легкое дыхание». Последний представляет собой АДИ, который автоматически активируется при вдохе больного.
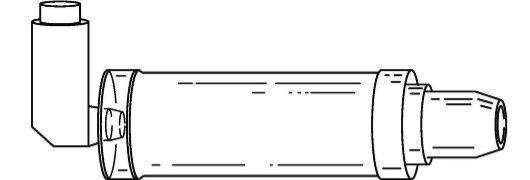
Спейсер
Спейсер (рис. 20-1) представляет собой емкость различного объема. Его применение позволяет, во-первых, аккумулировать ЛС перед его приемом. При этом нет необходимости в координации между вдохом и активизацией ингалятора, во-вторых, очень крупные частицы аэрозоля адсорбируются на поверхности спейсера, благодаря чему не попадают в полость рта и не всасываются в системный кровоток. ЛС с выраженными НЛР (например, глюкокортикоиды) лучше назначать через спейсер.
Применение спейсера позволяет проводить ингаляции у больных с резким ограничением скорости воздушного потока (например, при приступе БА). В последнем случае клиническая эффективность бронхорасширяющих ЛС значительно выше, чем при использовании АДИ. Спейсер с лицевой маской используют для ингаляций у детей.
Рис. 20-1. Спейсер
Для лечения больных с тяжелой бронхообструкцией применяют спейсеры большого (>0,75 л) объема. Некоторые ингаляторы выпускают с небольшими спейсерами, основная функция которых заключается в адсорбции крупных частиц аэрозоля.
Порошковые ингаляторы
Первые порошковые ингаляторы (рис. 20-2) появились в начале 1970-х годов. Преимуществом этих средств доставки считают: простоту использования (ингалятор не нуждается в активации в процессе вдоха - ЛС в виде порошка пассивно поступает в бронхи с потоком воздуха), отсутствие эффекта «охлаждения» дыхательных путей (связанное с использованием фреона в АДИ). С другой стороны, для активации большинства ПИ необходима высокая скорость вдоха, при низкой скорости уменьшается доля препарата, поступающего в легкие. Тем не менее клинические исследования у больных с БА свидетельствуют о том, что эффективность препаратов, назначаемых с помощью ПИ, примерно равна их эффективности при использовании АДИ.
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
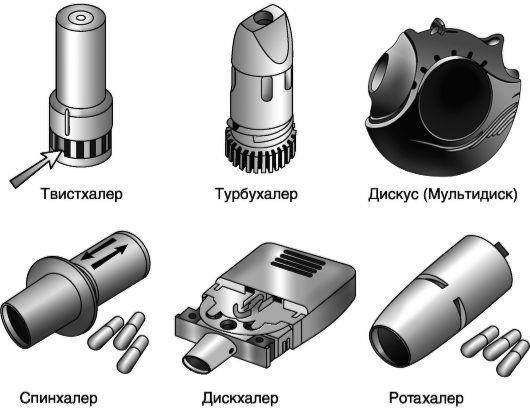
Ряд ПИ представляют собой устройства многоразового использования (спинхалер, ротахалер, аэролайзер), при их применении больные имеют возможность дополнительно приобретать капсулы с препаратом, что снижает стоимость ингаляций, но требует ухода и «перезарядки» ингалятора. Устройства для одноразового применения проще в использовании, но обходятся дороже (дискус, турбухалер).
Эффективность лечения ПИ зависит от условий хранения ЛС (низкая влажность воздуха), из-за этого ПИ часто снабжены поглотителями дополнительной влаги. Из дополнительных конструктивных
Рис. 20-2. Основные виды порошковых ингаляторов
особенностей ПИ следует упомянуть микротурбину (турбухалер), благодаря которой препарат распространяется по спиральной траектории, что увеличивает долю ЛС, поступающего в легкие (20-30% при использовании турбухалера, по сравнению с 11-15% при применении других ПИ).
Небулайзер
Небулайзер представляет собой стационарное устройство для ингаляций. Ограничение, связанное с применением небулайзера, заключается в первую очередь в необходимости источника электроэнергии (ряд моделей небулайзеров способны работать от автомобильного аккумулятора).
Образование аэрозоля в небулайзере происходит непрерывно и во время выдоха больного часть ЛС теряется. Для предотвращения этого некоторые модели небулайзеров снабжены прерывателем - больной сам регулирует образование аэрозоля. Некоторые модели небулайзеров способны согревать аэрозоль.
Существуют небулайзеры, способные выполнять ингаляции ЛС за небольшие (10-12 мин) промежутки времени, и приборы для длительных (1 ч и более) ингаляций.
Основные достоинства небулайзеров:
-независимость качества ингаляций от дыхательного маневра больного и скорости воздушного потока;
-возможность применения у детей, пожилых, лиц с неврологическими проблемами;
-проведение ингаляций не требует контроля со стороны больного и медицинского персонала;
-возможность введения очень больших доз ЛС;
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
- возможность применения различных ЛС через одно ингаляционное устройство.
Вместе с тем небулайзеры нуждаются в уходе и периодической дезинфекции. Среди областей применения небулайзеров следует назвать: ингаляционную терапию у детей (до 5 лет), пожилых, лечение тяжелых приступов БА, доставка в легкие антибиотиков и муколитиков.
Выбор средства доставки
Выбор средства доставки ЛС зависит от способности больного адекватно применять ингалятор. Большинство больных с хроническими заболеваниями легких могут успешно применять наиболее простой и сравнительно дешевый вид ингалятора - АДИ. У детей до 5 лет можно использовать только небулайзер или АДИ со спейсе-ром. Небулайзеры также можно применять у пожилых и лиц с выраженным ограничением воздушного потока.
20.12. ИНФЕКЦИОННЫЕ ЗАБОЛЕВАНИЯ ЛЕГКИХ
И ПЛЕВРЫ Пневмония
Пневмония - острое инфекционное заболевание, характеризующееся очаговым поражением респираторных отделов легких с внутриальвеолярной экссудацией1, выявляемое при объективном
1 При пневмонии воспаление нижних отделов дыхательных путей приводит к повышению проницаемости капилляров и накоплению экссудата (воспалительной жидкости) в конечных отделах дыхательных путей (альвеолах). В обычных условиях в альвеолах происходит газообмен.
и рентгенологическом обследовании и протекающее с выраженными в различной степени лихорадкой и интоксикацией.
Этиология и патогенез пневмоний
Наиболее часто возбудителями внебольничной пневмонии становятся пневмококк (Streptococcus
pneumoniae), который может вызывать как нетяжелые, так и тяжелые пневмонии с высокой летальностью, а также «атипичные» возбудители - Mycoplasma pneumoniae и Chlamydophila pneumoniae. «Атипичные» возбудители чаще встречаются у пациентов молодого и среднего возраста, вызывают нетяжелое течение заболевания, возможны вспышки инфекции в организованных коллективах (воинских подразделениях, школах). Реже пневмонии вызывают Legionella pneumophila (при этом характерно тяжелое течение заболевания с высокой
летальностью), Haemophilus influenzae (обычно у курильщиков и /или на фоне хронического бронхита),
представители семейства Enterobacteriaceae - Klebsiella pneumoniae, Escherichia coli (у пациентов пожилого возраста, с факторами риска - СД, декомпенсацией ХСН), Staphylococcus aureus (у пожилых пациентов, после перенесенного гриппа).
В этиологии нозокомиальной пневмонии основное значение имеют грамотрицательные бактерии
семейства Enterobacteriaceae, Pseudomonas aeruginosa, Acinetobacter spp., S. aureus (в том числе метициллинорези-
стентные штаммы - MRSA).
Симптомокомплекс пневмонии
Для клинической картины пневмонии характерно наличие как общих симптомов: повышение температуры тела, озноб, тахикардия, недомогание, слабость, потливость, потеря аппетита, так и специфических симптомов: боль в грудной клетке, усиливающаяся при глубоком вдохе и кашле; кашель; появление или усиление продукции гнойной мокроты, иногда «ржавой» или с прожилками крови; появление или усиление одышки. При объективном исследовании выявляют признаки инфильтрации легочной ткани1: усиление голосо-
1 Развитие пневмонии приводит к уплотнению легочной ткани и снижению ее воздушности (место воздуха в альвеолах занимает экссудат). Над пораженным участком лучше передается вибрация, возникающая при произношении отдельных слов (усиление голосового дрожания), при постукивании (перкуссия) выслушивается притупление звука, а при выслушивании (аускультация) - ослабление нормального (везикулярного) дыхания. Причина появления крепитации и влажных хрипов заключается в перемещении экссудата в нижних дыхательных путях. Воспаление листков плевры вызывает отложение на их поверхности фибрина, в результате при трении листков плевры друг о друга выслушивается посторонний шум трения.
вого дрожания, притупление перкуторного звука, при аускультации - ослабление везикулярного дыхания, крепитация. Наличие мокроты в бронхах приводит к появлению влажных хрипов. При вовлечении в процесс листков плевры выслушивается шум трения плевры.
Следует подчеркнуть, что по особенностям клинической и рентгенологической картины невозможно достоверно судить о возбудителе, вызвавшем пневмонию, тем более что во многих случаях заболевание вызывают ассоциации возбудителей (например, S. pneumoniae + M. pneumoniae или S. pneumoniae + H. influenzae).
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
Течение и тяжесть заболевания
Тяжесть пневмонии может быть различной и во многом определяется характером возбудителя. Наиболее тяжелое течение (с высокой частотой осложнений и летальных исходов) отмечается у больных с пневмонией,
вызванной Enterobacteriaceae, Pseudomonas aeruginosa, Acinetobacter spp., метициллинрезистентными штаммами S. aureus. С другой стороны, тяжесть течения зависит от своевременного начала антибактериального лечения. По данным клинических исследований, раннее назначение антибактериальных ЛС - наиболее важный фактор, уменьшающий смертность больных. Наконец, более тяжелое течение пневмонии наблюдается у больных с тяжелыми сопутствующими заболеваниями: СД, тяжелой ХСН, почечной и печеночной недостаточностью, а также у лиц, злоупотребляющих алкоголем и наркотиками. Смертность от пневмонии у больных старше 75 лет в 10-15 раз выше, чем в целом по популяции.
Применение антибактериальных препаратов привело к значительному снижению смертности, например, в Италии в 1900-1936 гг. показатели смертности от пневмонии составляли 200-250 случаев на 100 000 населения, а с началом широкого применения антибактериальных средств к 1951-1961 гг. этот показатель уменьшился до 40-70 случаев на 100 000. Однако и сегодня пневмония занимает 6-е место в общем перечне причин смерти и 1-е место в структуре смертности от внутрибольничных инфекций.
От 0,5 до 1,0% больных, поступающих в стационары, заболевают госпитальными (нозокомиальными) пневмониями. В РФ заболеваемость нозокомиальными пневмониями оценивают как 1,1% от общего числа госпитализированных пациентов. Примерно 2/3 случаев госпитальных пневмоний приходятся на долю пациентов отделений интенсивной терапии, а смертность среди этой категории больных колеблется от 50 до 70%.
К осложнениям пневмонии относят парапневмонический плеврит, эмпиему плевры, абсцедирование.
При своевременном начале адекватной эмпирической1 терапии у большинства больных уже на 2-3-е сут отмечаются снижение температуры и уменьшение выраженности симптомов заболевания, но полное выздоровление даже при эффективном лечении наступает спустя 2-3 нед.
Диагноз и методы обследования. Помимо неспецифических изменений в крови (нейтрофильного лейкоцитоза со сдвигом влево, увеличения СОЭ, концентрации С-реактивного белка, гиперглобу-линемии) для пневмонии характерно изменение кислотно-основного равновесия и газового состава крови.
Основным рентгенологическим признаком пневмонии считают инфильтраты в легких. При появлении очагов деструкции участки инфильтрации становятся неоднородными, с участками просветления.
Заподозрить у больного пневмонию можно на основании клинической картины и данных объективного осмотра, но диагноз подтверждается только при наличии рентгенологических изменений.
Этиологическая диагностика2. Для определения этиологии пневмонии используют бактериологическое исследование крови и клинического материала, полученного из дыхательных путей (мокроты, транстрахеального аспирата, жидкости, полученной при бронхоаль-веолярном лаваже). Серологические методы позволяют определять этиологию пневмонии ретроспективно, и обычно их используют только при проведении научных и эпидемиологических исследований.
Наиболее распространенный метод этиологической диагностики - бактериологическое исследование мокроты. Бактериоскопия окрашенных по Грамму мазков мокроты позволяет отличить мокроту хорошего качества, из которой вероятно выделение возбудителя пневмонии (большое количество лейкоцитов, нет или мало клеток плоского эпителия), от образца, контаминированного слюной (мало или нет лейкоцитов, клетки плоского эпителия в большом количестве). Мокрота плохого качества не пригодна для дальнейшего бактериологического исследования.
Клинико-фармакологические подходы к лечению пневмонии
Чаще всего лечение пневмонии остается эмпирическим, из-за того, что от начала лечения до получения данных из лаборатории проходит 2-3 сут, кроме того, примерно в 50% случаев выявить возбудителя
1 Эмпирическая терапия - лечение до выявления возбудителя.
2 Диагностика, направленная на выявление возбудителя заболевания.
не удается. На практике обычно доля выявленных возбудителей не превышает 20-25%. Таким образом, в реальных условиях антибактериальная терапия практически всегда становится эмпирической, по крайней мере, в первые дни болезни.
При амбулаторном лечении и нетяжелых формах заболевания следует отдавать предпочтение антибактериальным ЛС для приема внутрь (амоксициллин, макролиды, фторхинолоны), больные с тяжелым течением пневмонии должны получать антибиотики внутривенно (цефалоспорины третьего поколения в сочетании с макролидами и
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
респираторными фторхинолонами). При улучшении состояния возможен переход с внутривенной формы ЛС на таблетированную (ступенчатая терапия). Общая продолжительность лечения, как правило, составляет 7-10 сут (препарат отменяют через несколько дней после нормализации температуры тела), но при наличии микоплазменной или легионеллезной пневмонии продолжительность лечения составляет 2-3 нед. Более длительного лечения требуют больные, у которых развились осложнения - абсцедирование или плеврит.
Помимо антибактериальных ЛС при лечении пневмонии применяют инфузионную терапию (восполнение дефицита жидкости) и симптоматические средства (НПВС).
Контроль эффективности лечения пневмонии
Универсальных критериев эффективности антибактериальной терапии при пневмонии не существует. Принято считать, что оценку эффективности следует проводить через 48 ч после начала лечения. При этом снижение температуры тела и уменьшение выраженности симптомов заболевания позволяют считать лечение эффективным. Спустя 10-14 сут от начала лечения следует оценить эффективность по данным рентгенологического исследования (уменьшение инфильтрации или восстановление прозрачности легочных полей).
Дополнительно оценить эффективность лечения можно, опираясь на результаты повторного бактериологического исследования, динамику лабораторных показателей.
Абсцесс легких
Абсцесс легких представляет собой ограниченную полость в легочной ткани в результате ее некроза и гнойного расплавления. Наиболее часто абсцессы легких возникают при пневмонии или после аспирации содержимого ротоглотки (в бессознательном
состоянии при алкогольном опьянении, при заболеваниях ЦНС, передозировке седативных ЛС).
Этиология
Заболевание наиболее часто вызывает золотистый стафилококк, грамотрицательные палочки из семейства энтеробактерий или анаэробные бактерии (Bacteroides spp., Fusobacterium spp., Peptostreptococcus spp., Peptococcus spp. и др.), часто отмечают сочетание с энтеробактериями.
Симптомокомплекс
Из-за того, что абсцесс легких обычно формируется на фоне пневмонии, специфических клинических признаков у абсцедиро-вания нет. Характерны отсутствие динамики течения заболевания или ухудшение состояния пациента, несмотря на проводимую антибактериальную терапию, постоянная лихорадка и обильное выделение гнойной мокроты. Признаком анаэробной инфекции считают зловонный запах мокроты. При физикальном1 исследовании обычно определяют только симптомы пневмонии.
Диагноз и методы обследования
Диагноз абсцесса устанавливают на основании рентгенологического исследования или компьютерной томографии легких. При рентгенографии обнаруживают участки просветления на фоне пневмонической инфильтрации (в стадии формирования абсцесса) либо сформировавшуюся полость в легких с уровнем жидкости.
Клинико-фармакологические подходы к лечению абсцесса легких Препаратами выбора при лечении абсцесса легких считают амок-сициллин/клавулановую кислоту, Р-лактамные антибиотики в сочетании с респираторными фторхинолонами.
Эмпиема плевры
Эмпиема плевры (гнойный плеврит, пиоторакс) характеризуется скоплением гноя в плевральной полости. Выпот при эмпиеме содержит большое количество лейкоцитов - >10409/л, причем >75% составляют нейтрофилы. Основными возбудителями эмпиемы плевры на фоне пневмонии (с абсцессом легкого или без него) становятся анаэробы, при гнойном плеврите, развившемся в результате травмы
Общий осмотр больного, перкуссия, аускультация.
или оперативного вмешательства, - грамотрицательные аэробные бактерии или Staphylococcus aureus. Лечение эмпиемы плевры включает в себя дренирование плевральной полости с помощью дренажной трубки и назначение антибактериальных препаратов.
Клинико-фармакологические подходы к лечению эмпиемы плевры
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
Лечение при эмпиеме плевры - хирургическое: удаление выпота из плевральной полости и создание условий для ее дренирования. Выбор ЛС должен основываться на данных микробиологического исследования.
Туберкулез
Туберкулез - хроническая системная бактериальная инфекция, вызываемая Mycobacterium tuberculosis и характеризующаяся образованием специфических гранулем в пораженных тканях и выраженной клеточноопосредованной гиперчувствительностью. Заболевание, как правило, поражает легкие, но в процесс могут вовлекаться и другие органы (лимфатические узлы, кости, суставы, органы мочеполовой системы, оболочки мозга, перикард). При отсутствии эффективного лечения обычно отмечается постепенное хроническое прогрессирование болезни, которое в большинстве случаев приводит к смертельному исходу.
Этиология и патогенез туберкулеза
Возбудитель инфекции передается от человека к человеку аэрогенным путем, другие пути передачи существенного значения не имеют. Обычно туберкулез развивается у ослабленных лиц, у пациентов с нарушениями иммунитета, при длительном контакте с бактерио-выделителем, чаще болезнь поражает молодых людей.
Первоначальное внедрение возбудителя туберкулеза в легкие ранее не инфицированного человека вызывает ответную острую неспецифическую реакцию, которая редко носит выраженный характер и обычно протекает бессимптомно. Для инфицирования достаточно попадания в альвеолы 1-3 клеток M. tuberculosis. Микобактерии захватываются макрофагами и переносятся в регионарные лимфатические узлы. Если распространение микобактерий не ограничивается регионарными лимфоузлами, возбудитель проникает в системный кровоток и возможна диссеминация инфекции.
В участках заражения происходит формирование специфических гранулем1. Микобактерии могут персистировать в гранулемах, но их дальнейшее размножение и распространение ограничены. Затем большинство первичных очагов туберкулеза заживает, часто с последующей кальцификацией гранулем, хотя они остаются потенциальными источниками более поздней реактивации. Сочетание кальцифици-рованного периферического очага в легких и кальцифицированного лимфатического узла в корне легкого иногда видно на рентгенограмме органов грудной клетки и известно как очаг Гона.
У большинства пациентов первичные туберкулезные очаги подвергаются полному заживлению без развития заболевания в дальнейшем. У другой части больных полного заживления первичного очага не происходит. Туберкулез как клинически выраженное заболевание развивается у лиц, которые не в состоянии справиться с первичной инфекцией. У некоторых больных туберкулез развивается в течение нескольких недель с момента внедрения первичной инфекции. У большинства пациентов возбудитель на протяжении многих лет сохраняется в латентном состоянии, до тех пор, пока активное размножение микобактерий не приведет к возникновению болезни. Таким образом, выделяют три стадии туберкулеза:
-первичное инфицирование;
-латентную или скрытую инфекцию;
-рецидивирующий туберкулез.
Первичная туберкулезная инфекция обычно бессимптомна. В нижних и средних долях легких в типичных случаях развивается неспецифический пневмонит. Обычно увеличиваются лимфатические узлы в корнях легких, у детей иногда настолько сильно, что вызывают обструкцию бронхов. Иногда первичная инфекция может непосредственно приводить к развитию клинически выраженного заболевания с симптомами, характерными для реактивации.
Туберкулезная реактивация - хроническое заболевание, клинические проявления которого у пациентов с туберкулезом легких включают в себя общие симптомы (похудение, невысокую лихорадку, обильное потоотделение в ночное время) и симптомы поражения легких (кашель с прогрессирующим увеличением количества мокроты, одышку, кровохарканье).
Наиболее частая локализация туберкулезных очагов в легких - апикальные (верхушечные) задние сегменты верхних долей и верх-
Воспалительное разрастание ткани, имеющее вид узелка или бугорка.
ние сегменты нижних долей легких. Тяжесть заболевания может варьировать от минимальной (небольшие инфильтраты, не вызывающие клинических проявлений болезни) до выраженной (массивное вовлечение легких с образованием каверн1). При отсутствии эффективного лечения туберкулез легких приобретает хроническое и прогрессирующее течение. Периоды длительной стабилизации состояния сменяются периодами прогрессирования с вовлечением в процесс все больших участков легких.
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
По мере прогрессирования туберкулеза патологические очаги в легких подвергаются центральному некрозу с признаками казео-за2. Некротизированная ткань может удаляться через бронхи, приводя к образованию полостей (каверн) на месте бывших узлов. Каверны могут становиться источником массивного кровохарканья. Трансбронхиально обсеменяются другие участки легких с образованием в них инфильтративных очагов.
Диагноз и методы обследования
Важнейший метод исследования при туберкулезе - рентгенография органов грудной клетки. Типичным рентгенологическим признаком активного туберкулеза легких считают множественные узловые инфильтраты в апикальных задних сегментах верхних долей легких и верхних сегментах нижних долей легких. Часто обнаруживают каверны на фоне инфильтративных теней. Иногда выявляют плевральный выпот. Когда туберкулезный процесс становится неактивным или излечивается, на рентгенограммах появляются фиброзные рубцы, пораженные верхние доли легких уменьшаются в объеме. Фиброзные очаги кальцифицируются.
Для диагностики туберкулеза все клинические лабораторные исследования, за исключением бактериологических, малоинформативны.
Бактериологическое исследование - единственный метод, позволяющий достоверно установить диагноз туберкулеза. При туберкулезе легких наиболее информативным считают исследование мокроты. При бактериоскопии мазков мокроты, окрашенных специальными методами (например, по Цилю - Нильсену), можно обнаружить кислотоустойчивые бактерии. Культуральное исследование позволяет
1Каверна - полость распада легочной ткани.
2То есть содержат беловатые, творожистые массы (специфический признак туберкулезной инфекции).
провести специфическую идентификацию кислотоустойчивых бактерий и определить их чувствительность к противотуберкулезным препаратам. M. tuberculosis - медленно растущий микроорганизм, и первичное выделение возбудителя из клинического материала на классических питательных средах требует от 4 до 8 нед.
Надежным способом распознавания первичной туберкулезной инфекции считают постановку внутрикожной туберкулиновой пробы (проба Манту). Туберкулиновая гиперчувствительность проявляется большим размером образующейся папулы и свидетельствует об инфицировании или о заболевании туберкулезом. Однако при нарушениях иммунного статуса у некоторых больных туберкулезом в стадии активного процесса, милиарным туберкулезом и туберкулезным плевритом отмечается парадоксальное отсутствие кожной туберкулиновой реактивности - анергия.
Клинико-фармакологические подходы к лечению туберкулеза
В настоящее время для лечения туберкулеза используют стандартные режимы, рекомендованные ВОЗ, включающие в себя сочетания 2-5 противотуберкулезных препаратов и длительностью от 6 до 9 мес. Пациенты должны принимать препараты под наблюдением медицинского персонала. Эти режимы лечения подтвердили свою высокую эффективность и предупреждают распространение лекарственной устойчивости у M. tuberculosis.
Контроль эффективности и безопасности лечения тебуркулеза проводят на основании клинических и инструментальных данных, среди которых центральное место отводят рентгенологическим исследованиям.
Глава 21. БОЛЕЗНИ ПИЩЕВОДА И ЖЕЛУДКА
21.1. ФАКТОРЫ АГРЕССИИ И ЗАЩИТЫ СЛИЗИСТОЙ ОБОЛОЧКИ ПИЩЕВОДА, ЖЕЛУДКА И ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ
Наличие факторов агрессии не вызывает воспаления и повреждения слизистой оболочки желудка без недостаточности факторов защиты.
Факторы агрессии
Соляная кислота, продуцируемая париетальными клетками слизистой оболочки желудка. Основной этап ее образования - перенос протонов из цитоплазмы в просвет клеточных секреторных канальцев в обмен на ионы калия с помощью фермента Н+/К+-АТФазы (протонной помпы; рис. 21-1). Фермент активируется после воздействия на Н2-, м-холиновые или гастриновые рецепторы соответствующими медиаторами.
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi

Соляная кислота образуется в основном в области дна и тела желудка, там, где она необходима для обработки пищи, поступающей из пищевода. В антральном отделе количество образуемой соляной кислоты минимальное, а кислота, поступающая сюда с пищевым комком, в норме полностью нейтрализуется бикарбонатами (рис. 21-2).
Пепсин - протеолитический фермент, образующийся при активации пепсиногена под действием соляной кислоты.
Гастрин - гормон, образующийся в антральном отделе желудка и в тонкой кишке, стимулирующий образование HCl.
Бактерия Helicobacter pylori - грамотрицательная анаэробная палочка, имеющая на одном конце жгутики. Бактерия персистиру-ет в антральном отделе с наименьшим рН и защищает себя от HCl с помощью «аммиачного облака», которое образуется путем функционирования фермента уреазы. Микроорганизм обнаруживают и в других отделах желудка, если у больного снижена кислотопро-дукция при патологии слизистой оболочки или применении некоторых ЛС. Иногда Helicobacter pylori выявляют в двенадцатиперстной
кишке, но только на участках, где ее эпителий замещен эпителием желудка (желудочная метаплазия). Микроорганизм не повреждает поверхностные клетки слизистой оболочки, но продукты его жизнедеятельности активируют воспаление.
Рис. 21-1. Функционирование протонной помпы париетальной клетки желудка
Желчные кислоты и ферменты поджелудочной железы. Повреждают слизистую оболочку желудка и пищевода, куда поступают при ретроградном забросе содержимого двенадцатиперстной кишки (дуодено-гастральный и гастродуоденальный рефлюкс).
К факторам защиты относят.
Бикарбонаты. Слизистая оболочка пищевода не способна образовывать достаточно значимого количества бикарбонатов. В области тела и дна желудка они образуются в минимальных количествах, достаточных для защиты
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
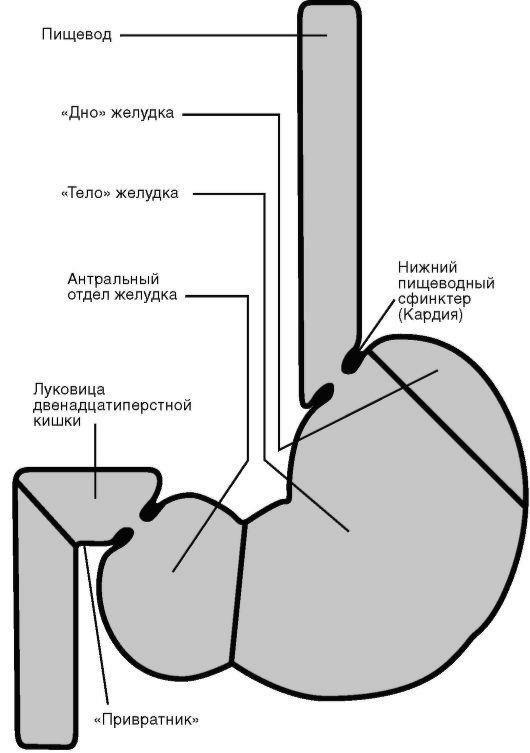
только самой слизистой оболочки. Объем образующихся в антральном отделе желудка бикарбонатов в норме достаточен для нейтрализации всей соляной кислоты, содержащейся в пищевом комке. При декомпенсации ощелачивающей функции антрального отдела желудка соляная кислота частично нейтрализует-
Рис. 21-2. Пищевод, желудок и двенадцатиперстная кишка
ся бикарбонатами, образующимися в поджелудочной железе и поступающими в желудок в результате дуоденогастрального рефлюкса.
Таким образом, при дуоденогастральном рефлюксе в желудок поступают как факторы агрессии, так и факторы защиты слизистых оболочек. Однако ощелачивание пищевого комка бикарбонатами панкреатического происхождения нефизиологично: химические соединения, содержащиеся в рефлюктате, перераздражают
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
