
6 курс / Клиническая фармакология / Кукес. Клиническая фармакология
.pdf
• Эти проводящие пути должны иметь различные электрофизиологические характеристики. Один из этих путей (А) характеризуется
быстрым проведением импульса и более длинным рефрактерным периодом («быстрый»). Второй путь (Б) должен иметь медленную скорость проведения, но короткий рефрактерный период («медленный»).
•Наличие преждевременного инициирующего импульса, вступающего в круг циркуляции в строго определенный временной промежуток. Этот временной промежуток определяется различием в длительности рефрактерных периодов быстрого и медленного путей и обозначается как зона тахикардии.
•Достаточно высокая скорость циркуляции импульса по кругу, поскольку очередной импульс, генерируемый вышележащим водителем ритма, способен блокировать циркуляцию.
•Возможность беспрепятственного распространения циркулирующего импульса за пределы круга для активации остальных отделов сердца.
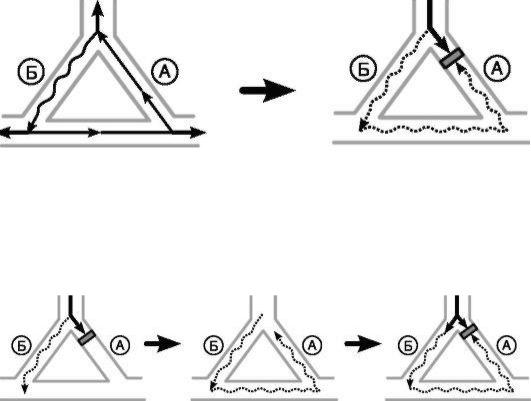
Этапы развития аритмий по механизму re-entry (обозначены на рис. 13-3 буквами): А - очередной синусовый импульс проводится по пути А и Б с разной скоростью, но фронты возбуждения «сталкиваются» на уровне анастомозов и циркуляции импульса по кругу не происходит, Б - преждевременный импульс вступает в круг циркуляции. Путь А уже провел очередной синусовый импульс и находится в состоянии рефрактерности, что приводит к блокаде проведения преждевременного импульса. Путь Б имеет более короткий рефрактерный период и способен провести преждевременный импульс, В - из-за низкой скорости проведения импульс медленно движется по пути Б и анастомозам, Г - к моменту достижения импульсом пути А этот путь выходит из состояния рефрактерности и проводит импульс в ретроградном направлении, Д - импульс вновь повторно входит в путь Б и циркулирует по кругу, Е - циркулирующий по кругу импульс выходит за пределы круга и активирует остальные отделы сердца, становясь водителем ритма.
Петли, определяющие развитие re-entry аритмий, могут быть как врожденными, так и приобретенными. Наджелудочковые reentry тахикардии часто связаны с наличием врожденных дополнительных проводящих путей или продольной диссоциацией АВ-узла на два канала с различными электрофизиологическими свойствами. Желудочковые re-entry аритмии обычно развиваются в результате заболеваний, приводящих к поражению миокарда. Петли reentry в желудочках возникают в тех областях, где нормальная ткань
соседствует с участками фиброзной ткани, появившейся после ИМ или кардиомиопатии.
Триггерные аритмии возникают в результате появления в фазу быстрой реполяризации или в ранний период фазы покоя положительно направленных «выступов» потенциала действия, получивших название ранних или поздних следовых деполяризаций (рис. 13-4).
Рис. 13-4. Ранние (1) и поздние (2) следовые деполяризации
В случаях, когда амплитуда следовых деполяризаций достигает определенной пороговой величины, происходит генерация импульсов путем активации натриевых каналов.
Ранние следовые деполяризации отмечаются при врожденных электрических аномалиях, приводящих к удлинению интервала QT, или в результате воздействия препаратов, в том числе и антиаритмических, которые также удлиняют интервал QT при воздействии на миокард катехоламинов, ишемии, при уменьшении концентрации калия в крови.
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
Поздние следовые деполяризации могут вызывать передозировка сердечными гликозидами, катехоламинами или ишемия.
Клинические проявления и методы диагностики нарушений ритма сердца
Клиническая картина аритмий определяется ЧСС во время эпизода нарушения ритма, его длительностью и состоянием сократительной функции сердца.
Проявления аритмий включают в себя ощущение сердцебиения или перебоев в работе сердца, обморочные или предобморочные состояния, симптомы сердечной недостаточности - одышку, хрипы в легких, снижение АД. У некоторых пациентов эпизоды аритмий протекают практически бессимптомно.
Ведущий метод диагностики аритмий - ЭКГ.
Регистрация ЭКГ с поверхности тела осуществляется с помощью системы электродов, которые формируют электрокардиографические отведения. Рисунок ЭКГ в различных отведениях несколько различается, но в норме содержит определенные компоненты, которые отражают последовательную активацию различных отделов сердца.
•Начальная часть зубца Р отражает генерацию импульса в синусовом узле.
•Зубец Р отражает распространение электрического импульса на предсердия.
•Сегмент PQ (PR) отражает прохождение электрического импульса через АВ-узел.
•Комплекс QRS отражает распространение электрического возбуждения на желудочки.
•Сегмент ST.
•Зубец Т отражает процесс реполяризации желудочков.
•Интервал Т - Р - период электрической диастолы. Существенное значение имеет оценка длительности интервала QT,
который измеряется от начала комплекса QRS до окончания зубца Т.
С помощью ЭКГ в большинстве случаев можно установить локализацию источника аритмии, ЧСС, а в ряде случаев предположить наиболее вероятный механизм развития.
Клинические и ЭКГ-симптомы аритмий представлены в табл. 13-1.
Таблица 13-1. Клинические и ЭКГ-симптомы аритмий
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
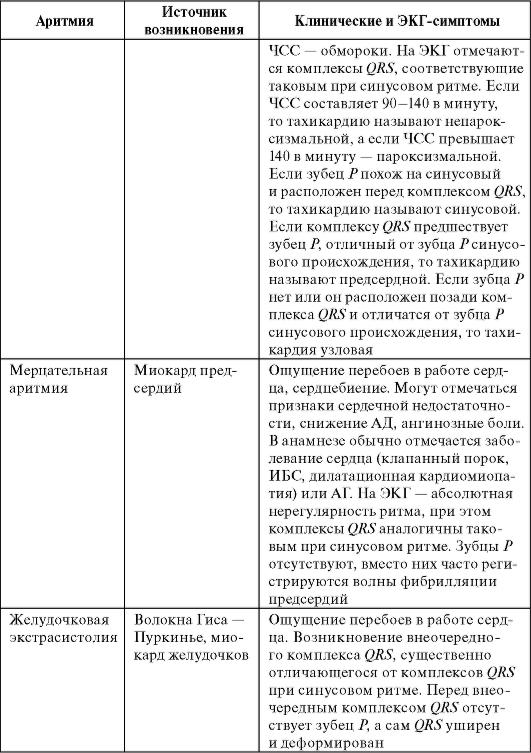
Продолжение табл. 13-1
Окончание табл. 13-1
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi

Для диагностики аритмий можно использовать и другие методы, основанные на регистрации электрической активности сердца. Среди них можно выделить длительное амбулаторное мониторирование ЭКГ по Холтеру, регистрацию ЭКГ во время тестов с физической нагрузкой, инвазивные внутрисердечные исследования, а также методы, позволяющие вызвать суправентрикулярные или желудочковые тахикардии (программируемая стимуляция предсердий или желудочков).
Классификация аритмий
Классификация наиболее распространенных аритмий по механизму развития и локализации представлена в табл.
13-2.
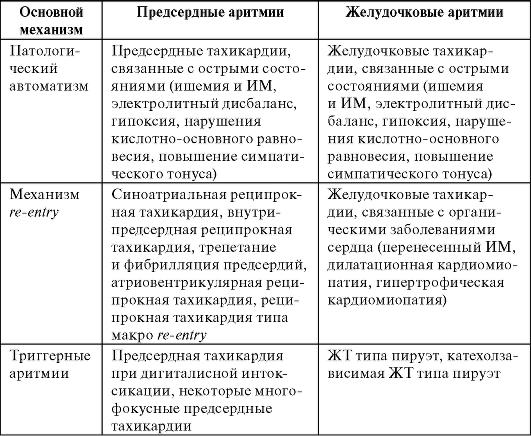
Таблица 13-2. Классификация наиболее распространенных аритмий по механизму развития и локализации
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
Основные цели лечения аритмий
При заболеваниях сердца (в основном при органических поражениях: перенесенном ИМ, дилатационной или гипертрофической кардиомио-патии, поражении сердца при АГ) самая частая причина смерти - внезапная коронарная смерть (ВКС). Основная причина ВКС - желудочковые тахикардии, переходящие в ФЖ с последующей остановкой сердца. Главной задачей лечения этой категории пациентов считают снижение риска ВКС и увеличение продолжительности жизни.
Некоторые аритмии (обычно наджелудочковые), особенно у пациентов без органических заболеваний сердца, не представляют угрозы для жизни. В то же время пароксизмы таких аритмий могут требовать госпитализации, ограничивают физическую активность или вызывают симптомы сердечной недостаточности. В этом случае целью лечения аритмии считают улучшение качества жизни больных.
Методы лечения аритмий могут быть как фармакологическими, так и нефармакологическими. Для фармакологического лечения применяют препараты, обладающие способностью изменять электрофизиологические свойства клеток миокарда и влиять на электрофизиологические нарушения, лежащие в основе развития аритмий. Эти препараты объединены в класс антиаритмических препаратов. Кроме того, при лечении аритмий эффективны препараты, влияющие на состояния, которые запускают аритмии, - ишемию миокарда, высокий симпатический тонус, например БАБ. Для лечения аритмий также могут быть эффективны препараты, которые воздействуют на патологические процессы в миокарде, приводящие к развитию аритмий (патологическое ремоделирование миокарда при инфаркте или кардиомиопатиях), - например, БАБ, ИАПФ, БРА, статины.
Для нефармакологического лечения аритмий в основном используют методы радиочастотной аблации компонентов петли re-entry (в основном при суправентрикулярных аритмиях) и имплантацию дефибриллятора-кардиовертера (для лечения желудочковых аритмий).
Имплантируемый кардиовертер-дефибриллятор (ИКД) - портативное устройство, обычно имплантируемое под грудную мышцу. Трансвенозный электрод при этом расположен в правом желудочке. ИКД способен распознавать желудочковые тахикардии и купировать их нанесением шокового импульса. ИКД чаще всего применяют для лечения желудочковых тахикардий и профилактики ВКС.
13.3. КЛАССИФИКАЦИЯ И МЕХАНИЗМЫ ДЕЙСТВИЯ АНТИАРИТМИЧЕСКИХ ПРЕПАРАТОВ
К антиаритмическим препаратам (ААП) относят ЛС, изменяющие электрические свойства клеток миокарда. Основной механизм действия ААП - воздействие на ионные токи и каналы, участвующие в формировании
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi

потенциала действия. Кроме того, некоторые ААП обладают дополнительной фармакологической активностью, которая может обусловливать дополнительное антиаритмическое действие препарата или развитие НЛР.
Согласно общепринятой классификации, предложенной Vaughan - Williams (1969), выделяют следующие классы ААП.
Класс I. Блокаторы натриевых каналов.
Класс IA. Препараты этого класса блокируют натриевые каналы, что приводит к замедлению скорости деполяризации. Кроме того, эти
ЛС обладают способностью к частичной блокаде калиевых каналов, что приводит к умеренному удлинению реполяризации (рис. 13-5).
Препараты IA класса Препараты Ш класса
Препараты 1С класса Препараты III класса
Рис. 13-5. Влияние антиаритмических препаратов на потенциал действия
Изменения ПД под влиянием препаратов IA класса приводят к замедлению скорости распространения импульса и некоторому увеличению рефрактерного периода. Эти эффекты реализуются как в предсердной, так и в желудочковой ткани, следовательно препараты IA класса имеют потенциальную эффективность как при предсердных, так и при желудочковых аритмиях. Эти ЛС представлены хинидином, прокаинамидом и дизопирамидом®.
Класс IB. Препараты этого класса обладают умеренной способностью блокировать натриевые каналы. Такой эффект при нормальной частоте ритма почти не проявляется, но существенно возрастает при высокой ЧСС или в условиях ишемии. Основной электрофизиологический эффект этой группы препаратов связан со способностью уменьшать продолжительность потенциала действия и рефрактерного периода. Действие препаратов IB класса реализуется преимущественно в миокарде желудочков, из-за чего эти ЛС обычно используют для лечения желудочковых аритмий. Препараты 1В класса представлены лидокаином, мексилетином® и фенотоином.
Класс IC. Препараты этого класса являются активными блокато-рами натриевых каналов, что обеспечивает их выраженное влияние на скорость деполяризации и проведения импульса. Влияние этих препаратов на реполяризацию и рефрактерность незначительно (см.
рис. 13-5). Препараты IC класса оказывают практически одинаковое влияние на предсердную и желудочковую ткани и эффективны как при предсердных, так и при желудочковых аритмиях. Представители этого класса - пропафенон и морацизин.
Класс II. β-Адреноблокаторы. БАБ обладают способностью блокировать действие катехоламинов на скорость спонтанной диастоличе-ской деполяризации водителей ритма СА-узла, что приводит к снижению ЧСС. БАБ замедляют проведение импульса и увеличивают рефрактерный период АВ-узла. БАБ эффективны при аритмиях, возникающих в отделах сердца, находящихся под прямым симпатическим контролем, и наджелудочковых аритмиях. Препараты этого класса также уменьшают частоту генерации импульсов эктопическими водителями ритма. БАБ чаще всего применяют для лечения желудочковых тахикардий. Механизмы эффективности БАБ при ЖТ обусловлены:
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
-антиишемической активностью (ишемия миокарда - важный пусковой механизм, приводящий к развитию ЖТ);
-торможением базовых патологических процессов, лежащих в основе структурно-функциональной перестройки миокарда у пациентов органическими заболеваниями сердца.
Класс III. Блокаторы калиевых каналов. Основное электрофизиологическое свойство препаратов этого класса - блокада калиевых каналов и замедление калиевого тока, что приводит к увеличению продолжительности реполяризации. Эти ЛС незначительно влияют на скорость деполяризации и проведения импульса, но увеличивают рефрактерные периоды в предсердной и желудочковой ткани. Препараты этого класса эффективны как при суправентрикулярных, так и желудочковых аритмиях. Представители: амиодарон и сота-лол.
Класс IV. Блокаторы медленных кальциевых каналов. Препараты этой группы (верапамил и дилтиазем) блокируют медленные кальциевые каналы, определяющие скорость деполяризации СА- и АВ-узлов. БМКК подавляют автоматизм, замедляют проведение и увеличивают их рефрактерность. Эти ЛС особенно эффективны при суправен-трикулярных re-entry аритмиях, когда круг циркуляции импульса включает в себя ткани АВ-узла. Патологические кальциевые токи могут показывать развитие следовых деполяризаций и аритмий, обусловленных триггерным механизмом. Это факт определяет успешное применение БМКК для лечения этих аритмий, в частности триггер-ных желудочковых тахикардий.
13.4. МЕХАНИЗМЫ ДЕЙСТВИЯ АНТИАРИТМИЧЕСКИХ ПРЕПАРАТОВ ПРИ РАЗЛИЧНЫХ ТИПАХ АРИТМИЙ
Обычно нарушения автоматизма развиваются при острых состояниях - ишемии миокарда, нарушении электролитного баланса, высоком симпатическом тонусе, нарушении кислотно-основного равновесия. Эффективность ААП при лечении таких аритмий невысока. Основная задача лечения нарушений автоматизма - устранение и коррекция факторов, вызывающих их развитие.
Для эффективного лечения re-entry аритмий необходимо изменить электрофизиологические свойства путей, по которым циркулирует импульс. При этом ААП позволяют воздействовать как на скорость проведения импульса, так и на длительность рефрактерных периодов путей циркуляции импульса.
Изменять скорость проведения импульса способны препараты IA, IC классов, БМКК и БАБ (в тканях АВ-узла), а изменять длительность рефрактерных периодов способны препараты IB (уменьшение продолжительности), а также IA и III класса (увеличение продолжительности).
Механизм влияния ААП на re-entry аритмии представлен на рис. 13-6-13-9.
Рис. 13-6. Механизм купирования re-entry аритмий антиаритмическими препаратами, уменьшающими скорость деполяризации
Механизм действия препаратов, замедляющих скорость деполяризации (IA, IB, IC классов, БМКК и БАБ), связан с выраженным замедлением скорости проведения импульса по «медленному» (Б) и «быстрому» (А) путям. Существенное снижение скорости циркуляции импульса позволяет вступить в круг импульсу из других источников автоматизма (чаще всего из СА-узла), столкновение импульсов прекращает циркуляцию и купирует re-
entry аритмию.
а б в
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
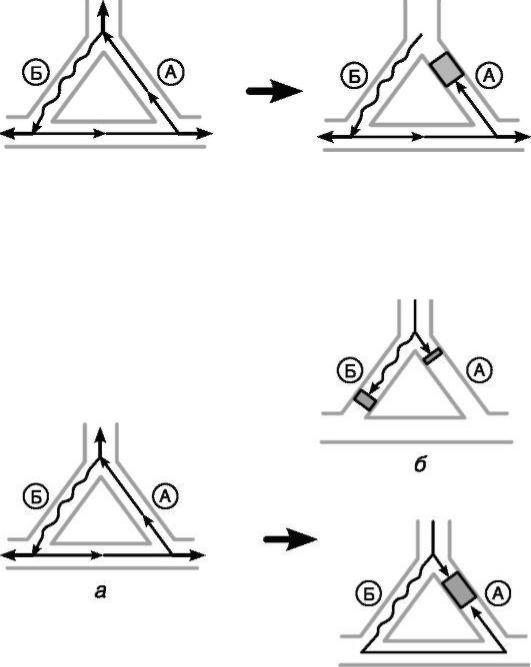
Рис. 13-7. Механизм профилактики re-entry аритмий антиаритмическими препаратами, уменьшающими скорость деполяризации
Снижение скорости проведения импульса в круге re-entry способно предотвратить развитие аритмии: а - внеочередной импульс вступает в круг re-entry. Путь А ранее провел очередной синусовый импульс и находится в состоянии рефрактерности, что приводит к блокаде проведения преждевременного импульса. Путь Б имеет более короткий рефрактерный период и способен провести преждевременный импульс; б - под влиянием ААП импульс медленно движется по анастомозам и вступает в путь А; в - низкая скорость проведения импульса позволяет вступить в круг А очередному синусовому импульсу до того, как циркулирующий импульс вступит в круг Б. Импульсы сталкиваются, что делает невозможным развитие re-entry аритмии.
Рис. 13-8. Механизм купирования re-entry аритмий антиаритмическими препаратами, удлиняющими продолжительность потенциала действия
Механизм действия препаратов, увеличивающих длительность потенциала действия (III и IA классы), связан с их преимущественным влиянием на рефрактерность «быстрого» пути А. Увеличение длительности рефрактерного периода «быстрого» пути А приводит к тому, что циркулирующий по кругу re-entry импульс застает путь А в состоянии рефрактерности и неспособности провести импульс. Это приводит к прекращению циркуляции импульса и купированию аритмии.
в
Рис. 13-9. Механизм профилактики re-entry аритмий антиаритмическими препаратами, удлиняющими продолжительность потенциала действия
Механизм профилактического действия препаратов, удлиняющих продолжительность потенциала действия (IA и III классы), можно объяснить следующим образом. Во-первых, увеличение рефрактерного периода «медленного» пути Б приводит к тому, что длительность рефрактерных периодов «быстрого» (А) и «медленного» (Б) путей становится практически одинаковой. Это приводит к блокаде проведения внеочередного импульса как в быстром, так и в
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
медленном пути, создавая условия, не позволяющие внеочередному импульсу циркулировать по кругу re-entry; (б). Во-вторых, дальнейшее увеличение рефрактерного периода «быстрого» пути (а) может вызвать блокаду ретроградного проведения импульса, что делает невозможным циркуляцию импульса и предотвращает развитие аритмии (в).
Основной момент в лечении триггерных аритмий - устранение факторов, которые приводят к возникновению следовых деполяризаций. К этим факторам относят: препараты, способные удлинять интервал QT (в том числе и антиаритмические), сердечные гли-козиды, а также ситуации, приводящие к выраженной активации симпатоадреналовой системы, в частности интенсивные физические или психоэмоциональные нагрузки.
Кроме того, для лечения триггерных аритмий можно применять БАБ и БМКК. БАБ способны подавлять триггерные аритмии путем
устранения следовых деполяризаций, вызванных катехоламинами. БМКК, замедляя медленные кальциевые токи, могут устранять следовые деполяризации и зависимые от них аритмии.
Основные нежелательные лекарственные реакции, связанные с применением антиаритмических препаратов
Основные НЛР антиаритмических препаратов можно классифицировать следующим образом:
-проаритмические эффекты;
-системные токсические эффекты;
-угнетение функций СА-узла и проведения импульса по проводящей системе сердца (АВ- и внутрижелудочковые блокады);
-угнетение сократимости миокарда.
Проаритмические эффекты ААП имеют большое клиническое значение. Аритмии, вызываемые ААП, могут приводить к ВКС. Развитие проаритмий после приема ААП напрямую связано с их способностью влиять на ионные токи и изменять скорость проведения импульса и /или длительность рефрактерного периода.
Механизмы развития проаритмий, вызванных ААП, включают в себя:
-активацию кругов циркуляции импульса и создание условий для развития новых re-entry аритмий;
-развитие следовых деполяризаций и триггерных аритмий. Способность ААП устранять или предупреждать reentry аритмии
связана с изменением скорости проведения импульса и /или продолжительности рефрактерного периода в отдельных компонентах петли циркуляции импульса. Назначение препаратов, изменяющих скорость проведения импульса и /или продолжительность рефрактерного периода, может менять электрофизиологические свойства путей циркуляции таким образом, что ранее неактивный круг приобретает патологические свойства, что приводит к появлению «новой» re-entry аритмии. Чаще всего появление re-entry аритмий вызывают препараты IA и ГС классов. Проаритмическая тахикардия может иметь меньшую частоту, чем исходная аритмия. Эпизоды проаритмической reentry тахикардии могут приводить к ФЖ и ВКС.
Препараты, увеличивающие продолжительность потенциала действия (IA и III классов), могут вызывать развитие ранних следовых деполяризаций и триггерных желудочковых аритмий. Эти аритмии проявляются как повторяющиеся эпизоды полиморфной ЖТ.
Обычно они протекают бессимптомно, но могут вызывать обмороки
или ВКС.
Большинство ААП подавляют активность синусового узла, вызывают нарушение АВили внутрижелудочковой проводимости. Клинически значимое угнетение функции синусового узла проявляется уменьшением ЧСС (синусовой брадикардией). ААП способны снижать скорость проведения импульса или полностью блокировать его проведение в АВ-узле. АВ-блокада чаще всего развивается при использовании БАБ и БМКК. Препараты IA, IC и реже III классов могут вызывать нарушения проведения импульса в системе Гиса - Пуркинье. Развитие внутрижелудочковой блокады сопряжено с высоким риском появления обморочных состояний и остановки сердца.
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
ААП снижают сократительную функцию миокарда ЛЖ. Таким свойством обладают пропафенон, хинидин, прокаинамид, БМКК. Соответственно необходимо тщательно подходить к выбору ААП при наличии сердечной недостаточности или дисфункции ЛЖ.
ААП могут вызывать НЛР, не связанные с их электрофизиологическим действием. Тем не менее эти эффекты могут быть клинически значимыми и требовать отмены препарата. Токсическое действие проявляется на уровне всех органов и тканей. В качестве примеров можно привести:
-острый пневмонит и хронический фиброзирующий легочный альвеолит при приеме амиодарона;
-угнетение образования лейкоцитов в костном мозге при применении прокаинамида;
-лекарственный гепатит, вызванный приемом хинидина;
-волчаночный синдром, обусловленный приемом прокаинами-да;
-нарушения функции щитовидной железы, вызванные амиода-роном.
Клиническая фармакология отдельных ААП подробно представлена в приложении на компакт-диске.
В таблице 13-3 даны рекомендации по применению ААП при различных аритмиях.
Таблица 13-3. Рекомендации по применению антиаритмических препаратов при различных аритмиях
Еще больше книг только на канале Telegram "Медицинские книги" https://t.me/medknigi
