
3 курс / Патологическая анатомия / Струков_Серов_Патологическая_анатомия
.pdf180 |
Общая патологическая анатомия |
в полостях тела по той же причине может стать основой для образования жидкости воспалительной природы, т.е. перейти в экссудат (например, развитие перитонита на фоне асцита — асцит-перитонит).
Уменьшение содержания тканевой жидкости — обезвоживание (дегидратация), или эксикоз (от лат. siccus — сухой). Оно сопровождается и потерей воды кровью, т.е. ангидремией.
Внешний вид людей при эксикозе характерен: заостренный нос, запавшие глаза, щеки, сморщенная, дряблая кожа, уменьшенная масса тела. При этом кровь становится густой и темной, поверхности серозных оболочек — сухими или покрытыми слизеподобной тягучей массой. Органы уменьшены, капсула их становится морщинистой. Эксикоз встречается при быстрой потере большого объема жидкости, что характерно для холеры, длительной диареи, диспепсии. Иногда обезвоживание наблюдают при коматозных состояниях, например при энцефалите.
Контрольные вопросы и задания
1.Назовите и охарактеризуйте виды нарушения кровообращения, связанные с изменением кровенаполнения.
2.Назовите виды местной артериальной гиперемии в зависимости от причин ее развития.
3.Назовите условия для развития местной венозной гиперемии (полнокровия).
4.Назовите макро- и микроскопические признаки «мускатной печени».
5.Назовите причины и патогенез «бурой индурации легких», опишите
ееморфологию.
6.Что такое «сладж» и «стаз» эритроцитов и их последствия.
7.Назовите патологические процессы, при которых наблюдается плазморрагия.
8.Назовите механизмы нарушений сосудистой стенки, приводящие к кровотечениям и кровоизлияниям.
9.Назовите механизмы и стадии образования тромба.
10.Назовите основные морфологические признаки тромба.
11.Назовите виды тромбов
12.Назовите возможные изменения тромба.
13.Что такое ДВС-синдром, предпосылки его развития и морфологические признаки?
14.Что такое эмболия и ее виды?
15.Охарактеризуйте морфологическую картину шока.
Глава 5
ВОСПАЛЕНИЕ
Воспаление — комплексная местная сосудисто-мезенхимальная реакция на повреждение ткани, направленная на уничтожение агента, вызвавшего это повреждение, и на восстановление поврежденной ткани. Воспаление — реакция, выработанная в ходе филогенеза, которая имеет защитноприспособительный характер.
Еще в конце XIX в. выдающийся биолог И.И. Мечников (1845–1916) считал, что воспаление — приспособительная и выработанная в ходе эволюции реакция организма. Одно из важнейших ее проявлений — фагоцитоз микрофагами и макрофагами патогенных агентов и обеспечение таким образом выздоровления организма. Репаративная функция воспаления для И.И. Мечникова была сокрыта. Подчеркивая защитный характер воспаления, он в то же время полагал, что целительная сила природы — воспалительная реакция — это приспособление, не достигшее еще совершенства. По мнению И.И. Мечникова, доказательство этого — частые болезни, сопровождаемые воспалением, и иногда смерть от них.
Позднее патолог И.В. Давыдовский (1887–1968), рассматривая патологические процессы с точки зрения значения для человека как биологического вида, показал их совершенство и приспособительную роль. Человек обладает всеми приспособительными реакциями вида, кроме того, каждый индивид имеет свои собственные реакции, обусловленные полом, возрастом, реактивностью, другими заболеваниями. При этом видовые реакции преобладают над индивидуальными. И с этих позиций видовые реакции, в том числе и воспаление, — совершенные и целесообразные процессы. И если люди иногда умирают от воспаления, что случается неизмеримо реже, чем выздоровление, то виновно в этом не воспаление как совершенная приспособительная реакция, а индивидуальные особенности больного.
Этиология воспаления
Вызывающие воспаление факторы — биологические, физические (в том числе травматические) и химические, по происхождению они могут быть эндогенными или экзогенными.
Среди биологических факторов наибольшее значение имеют вирусы, бактерии, риккетсии, грибы и животные паразиты. Биологические причины воспаления — циркулирующие в крови антитела и иммунные комплексы, которые состоят из антигена, антител и компонентов комплемента, причем антиген может быть и немикробной природы.

182 |
Общая патологическая анатомия |
|
|
|
|
Рис. 5-1. Схема фаз воспаления
Физические факторы, вызывающие воспаление, — лучевая и электрическая энергия, высокие и низкие температуры, различного рода травмы.
Химические факторы воспаления — различные химические вещества, токсины и яды.
Воспаление определяется не только действием того или иного этиологического фактора, но и особенностью реактивности организма.
Морфология и патогенез воспаления
Воспаление проявляется образованием микроскопического очага или обширного участка повреждения диффузного характера. Иногда воспаление возникает в системе тканей — это системное воспаление: ревматические болезни при системном воспалении соединительной ткани, системные васкулиты, генерализованная воспалительная реакция. Иногда провести грань между локализованным и системным воспалением бывает затруднительно.
Воспаление развивается на территории гистиона и состоит из последовательных фаз: альтерации, экссудации, пролиферации гематогенных, гистиогенных и паренхиматозных клеток (эпителия) (рис. 5-1).
Альтерация
Альтерация, или повреждение ткани, — инициальная фаза воспаления, пусковой механизм, определяющий кинетику воспалительной реакции. Фаза проявляется различного вида дистрофией и некрозом. В эту фазу происходит выброс медиаторов воспаления — биологически активных веществ, обеспечивающих химические и молекулярные связи между процессами, протекающими в воспалительном очаге. В организме существуют медиаторы клеточного (тканевого) и плазменного (гуморального) происхождения. Кроме того, существует система антимедиаторов воспаления, предупреждающих избыточное накопление или прекращающих действие медиаторов.

Глава 5. Воспаление |
183 |
Медиаторы клеточного происхождения связаны с эффекторными клетками, к которым относятся лаброциты (тканевые базофилы), базофильные лейкоциты, которые выбрасывают гистамин, серотонин, медленно реагирующую субстанцию анафилаксии; тромбоциты, продуцирующие, помимо гистамина, серотонина и простагландинов, лизосомные ферменты; полиморфно-ядерные лейкоциты, богатые лейкокинами, лизосомными ферментами, катионными белками и нейтральными протеазами. Медиаторами воспаления продуцируются и клетки иммунных реакций — макрофаги, выбрасывающие свои цитокины (интерлейкины-1, -3, -6), и лимфоциты, тоже продуцирующие цитокины (интерлейкин-2). Роль медиаторов могут играть поврежденные клетки и микроорганизмы.
С медиаторами клеточного происхождения связана активация плазменных медиаторов, что приводит к повышению проницаемости микрососудов: они усиливают фагоцитоз, обладают бактерицидным действием, вызывают вторичную альтерацию (гистолиз), включают иммунные механизмы в воспалительную реакцию, регулируют пролиферацию и дифференцировку клеток на поле воспаления, направленных на возмещение утраченной ткани или замещение очага повреждения соединительной тканью (рис. 5-2). «Дирижером» клеточных взаимодействий на поле воспаления является макрофаг — клетка, продуцирующая более 80 биологически активных веществ.
Медиаторы плазменного происхождения — представители калликреинкининовой (кинины, калликреины), свертывающей, противосвертывающей (XII фактор свертывания крови, или фактор Хагемана, плазмин) и комплементарной (компоненты С3−C5) систем. Медиаторы этих систем
Рис. 5-2. Схема действия медиаторов воспаления клеточного (тканевого) происхождения

184 |
|
|
Общая патологическая анатомия |
||
|
|
|
|
|
|
|
|
|
|
|
|
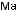














 -1
-1





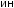 -2
-2
Рис. 5-3. Схема действия медиаторов воспаления плазменного (гуморального) происхождения
повышают проницаемость микрососудов, активируют хемотаксис поли- морфно-ядерных лейкоцитов, фагоцитоз и внутрисосудистую коагуляцию (рис. 5-3).
Медиаторы плазменного и клеточного происхождения взаимосвязаны и работают по принципу аутокаталитической реакции с обратной связью и взаимной поддержкой. Действие медиаторов опосредовано рецепторами на поверхности эффекторных клеток. Из этого следует, что смена одних медиаторов другими во времени обусловливает смену клеточных форм на поле воспаления — от полиморфно-ядерного лейкоцита для фагоцитоза до фибробласта, активируемого цитокинами макрофага, для репарации.
На всех этапах воспаления происходит высвобождение клеточных и гуморальных веществ, предупреждающих избыточное накопление и действие медиаторов, — антимедиаторов, которые синтезируются в макрофагах, тучных клетках, эозинофилах, базофилах, фибробластах. Антимедиаторами являются антиоксиданты (пероксидаза, С-реактивный белок, церулоплазмин), моноаминоксидаза, гистаминаза, глюкокортикоиды, α-антитрипсин. Соотношение медиаторов и антимедиаторов воспаления во многом определяет особенности воспалительного процесса.
Глава 5. Воспаление |
185 |
Экссудация
Экссудация быстро следует за альтерацией и выбросом медиаторов воспаления. Стадии экссудации:
–реакция микроциркуляторного русла с нарушениями реологических свойств крови;
–повышение сосудистой проницаемости на уровне микроциркуляторного русла;
–экссудация составных частей плазмы крови;
–эмиграция клеток крови;
–фагоцитоз;
–образование экссудата и воспалительного клеточного инфильтрата.
Реакция микроциркуляторного русла с нарушениями реологических свойств
крови — один из ярких морфологических признаков воспаления. Изменения микрососудов начинаются с рефлекторного спазма, уменьшения просвета артериол и прекапилляров, которое быстро сменяется расширением всей сосудистой сети зоны воспаления, и прежде всего посткапилляров и венул. Воспалительная гиперемия обусловливает повышение температуры и покраснение воспаленного участка. При начальном спазме ток крови
вартериолах ускоряется, а затем замедляется. В лимфатических сосудах, как и в кровеносных, вначале лимфоток ускоряется, а затем замедляется. Лимфатические сосуды переполнены лимфой и лейкоцитами.
Вбессосудистых тканях (роговице, клапанах сердца), питание которых
внорме осуществляется диффузией питательных веществ, в начале воспаления преобладает альтерация, а затем очень быстро происходит врастание сосудов из соседних областей и включение их в воспаление.
Изменения реологических свойств крови состоят в нарушении распределения в кровяном потоке лейкоцитов и эритроцитов при замедленном токе крови в расширенных венулах и посткапиллярах. Полиморфно-ядерные лейкоциты (нейтрофилы) выходят из осевого тока, собираются в краевой зоне и располагаются вдоль стенки сосуда. Краевое расположение нейтрофилов сменяется их краевым стоянием с последующей миграцией за пределы сосуда.
Изменения гемодинамики и сосудистого тонуса в очаге воспаления приводят к стазу в посткапиллярах и венулах, который сменяется тромбозом. Те же изменения происходят и в лимфатических сосудах. Таким образом, при продолжающемся притоке крови в очаг воспаления отток крови, а также лимфы нарушается. При блокаде отводящих кровеносных и лимфатических сосудов очаг воспаления исполняет роль барьера, предупреждающего распространение и генерализацию процесса.
Повышение сосудистой проницаемости на уровне микроциркуляторного русла — одно из существенных признаков воспаления. Вся гамма тканевых изменений, своеобразие форм воспаления в значительной мере определяются состоянием сосудистой проницаемости, глубиной ее повреждения. Большая роль в повышении проницаемости сосудов принадлежит эндотелиальным клеткам, продуцирующим простагландины, фактор активации тромбоцитов, оксид азота и ряд других цитокинов. Это приводит
186 |
Общая патологическая анатомия |
к усилению микропиноцитоза и повышению сосудистой проницаемости. Одновременно происходят повреждение и слущивание эндотелия. При этом оголяется базальная мембрана, содержащая коллаген IV типа, обладающий хемотаксисом к тромбоцитам, что способствует образованию микротромбов. Все эти реакции обеспечивают экссудацию в ткани и полости жидкой части плазмы, эмиграцию клеток крови, образование экссудата и воспалительного клеточного инфильтрата.
Экссудация составных частей плазмы крови — это проявление сосудистой реакции, развивающейся в пределах микроциркуляторного русла. Она выражается в выходе за пределы сосуда жидких составных частей крови: воды, белков, электролитов.
Эмиграция клеток крови, т.е. выход их из тока крови через стенку сосудов, осуществляют хемотаксические медиаторы. Эмиграции предшествует краевое стояние нейтрофилов. Они прилипают к стенке сосуда (главным образом в посткапиллярах и венулах), затем образуют отростки (псевдоподии), которые проникают между эндотелиальными клетками, — это межэндотелиальная эмиграция (рис. 5-4). Базальную мембрану нейтрофилы преодолевают вероятнее всего на основе феномена тиксотропии (обратимого изометрического уменьшения вязкости коллоидов), т.е. перехода геля мембраны в золь при прикосновении клетки к мембране. В околососудистой ткани нейтрофилы продолжают движение с помощью псевдоподий. Этот механизм характерен для эмиграции и всех других клеток крови. Процесс эмиграции лейкоцитов носит название лейкодиапедез, эритроцитов — эритродиапедез.
Фагоцитоз (от греч. phagos — пожирать и kytos — вместилище) — поглощение и переваривание клетками (фагоцитами) различных тел живой (бактерии) и неживой (инородные тела) природы. Фагоциты — разнообразные клетки, но при воспалении наибольшее значение приобретают нейтрофилы и макрофаги.
Фагоцитоз обеспечивается рядом биохимических реакций. При фагоцитозе уменьшается содержание гликогена в цитоплазме фагоцита, что связано с усиленным анаэробным гликогенолизом, необходимым для выработки энергии для фагоцитоза. Вещества, блокирующие гликогенолиз, подавляют и фагоцитоз.
Фагоцитируемый объект (бактерия), окруженный инвагинированной цитомембраной (фагоцитоз характеризуется потерей цитомембраны фагоцита), образует фагосому. При слиянии ее с лизосомой образуется фаголизосома (вторичная лизосома), в которой с помощью гидролитических ферментов происходит внутриклеточное переваривание — завершенный фагоцитоз (рис. 5-5), в котором большую роль играют антибактериальные катионные белки лизосом нейтрофилов. Они убивают микроорганизмы, которые затем перевариваются. Если микроорганизмы не перевариваются фагоцитами, чаще макрофагами, и размножаются в их цитоплазме, возникает незавершенный фагоцитоз, или эндоцитобиоз. Он обусловлен многими причинами, в частности тем, что лизосомы макрофагов могут содержать недостаточное количество антибактериальных катионных белков или вообще лишены их. Таким образом, фагоцитоз — не всегда защитная реакция

Глава 5. Воспаление |
187 |
а |
|
б |
|
|
|
Рис. 5-4. Эмиграция лейкоцитов через стенку сосуда при воспалении: а — один из нейтрофилов (H1) тесно прилежит к эндотелию (Эн), другой (Н2) имеет хорошо очерченное ядро (Я) и пронизывает эндотелий. Большая половина этого лейкоцита расположена в подэндотелиальном слое. На эндотелии в этом участке видны псевдоподии третьего лейкоцита (Н3). Пр — просвет сосуда, × 9000; б — нейтрофилы (СЛ) с хорошо контурированными ядрами (Я) расположены между эндотелием и базальной мембраной (БМ); стыки эндотелиальных клеток (СЭК) и коллагеновые волокна (КлВ) за базальной мембраной, ×20 000 (по Флори и Гранту)
организма, иногда он создает предпосылки для диссеминации микробов. Если болезнь характеризуется нестерильным иммунитетом, эндоцитобиоз обеспечивает сохранение возбудителей в организме, препятствуя их генерализации. И в этом случае эндоцитобиоз носит приспособительный характер.
Образование экссудата и воспалительного клеточного инфильтрата завершает процессы экссудации. Выпот жидкой части крови, эмиграция лейкоцитов, диапедез эритроцитов ведут к появлению в пораженной ткани или полости воспалительной жидкости — экссудата. Накопление экссудата в ткани ведет к увеличению ее объема, сдавлению нервных окон-

188 |
Общая патологическая анатомия |
|
чаний и появлению боли, которую при |
|
воспалении связывают с действием плаз- |
|
менных медиаторов воспаления (бради- |
|
кинин), к нарушению функции ткани |
|
или органа. |
|
Обычно белки экссудата составля- |
|
ют более 2% его объема. В зависимо- |
|
сти от степени проницаемости стенки |
|
сосуда в ткань могут проникать разные |
|
белки. При небольшом повышении про- |
|
ницаемости сосудистого барьера через |
|
него проникают в основном альбумины |
|
и глобулины. При высокой степени про- |
|
ницаемости наряду с ними выходят |
|
и крупномолекулярные белки, в част- |
|
ности фибриноген. В одних случаях |
|
в экссудате преобладают нейтрофилы, |
|
в других — лимфоциты, моноциты и гис- |
|
тиоциты, в-третьих — эритроциты. |
|
Скопление в тканях клеток экссуда- |
|
та, а не жидкой его части, называется |
|
воспалительным клеточным инфильтратом, |
|
в котором преобладают как гематоген- |
Рис. 5-5. Фагоцитоз. Макрофаг с фа- |
ные, так и гистиогенные элементы. |
гоцитированными обломками лей- |
|
коцита (СЛ) и липидными вклю- |
Пролиферация |
чениями (Л). Электронограмма, |
Пролиферация (размножение) кле- |
×20 000 |
ток — завершающая фаза воспаления, |
направленная на восстановление поврежденной ткани. Возрастает количество мезенхимальных камбиальных клеток, В- и Т-лимфоцитов, моноцитов. При
размножении клеток в очаге воспаления наблюдают клеточную дифференцировку и трансформацию (рис. 5-6): камбиальные мезенхимальные клетки трансформируются в фибробласты; В-лимфоциты дают начало образованию плазматических клеток. Т-лимфоциты дифференцируются в различные формы — Т-хелперы, Т-супрессоры. Моноциты дают начало гистиоцитам и макрофагам. Макрофаги — источник образования эпителиоидных и гигантских клеток (клеток инородных тел и Пирогова–Лангханса).
На различных этапах пролиферации фибробластов образуются продукты их деятельности — белок коллаген и гликозаминогликаны, аргирофильные
иколлагеновые волокна, межклеточное вещество соединительной ткани.
Впроцессе пролиферации при воспалении участвует и эпителий, что особенно выражено в коже и слизистых оболочках желудка и кишечника. При этом пролиферирующий эпителий может образовывать полипозные разрастания. Пролиферация клеток на поле воспаления способствует возмещению утраченных тканей и клеток — репарации. При этом дифферен-

Глава 5. Воспаление |
189 |
Стволовые Стволовые
Хелперы Киллеры  Супрессоры
Супрессоры 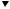
Рис. 5-6. Схема дифференцировки и трансформации клеток при воспалении
цировка пролиферирующих эпителиальных структур возможна лишь при созревании и дифференцировке соединительной ткани.
Воспаление со всеми его компонентами появляется только на поздних этапах внутриутробного развития. У плода, новорожденного и ребенка воспаление имеет ряд особенностей. Первая особенность воспаления — преобладание альтеративного и продуктивного компонентов, так как они филогенетически более древние. Вторая особенность воспаления, связанная с возрастом, — склонность местного процесса к распространению и генерализации в связи с анатомической и функциональной незрелостью органов иммуногенеза и барьерных тканей.
Регуляцию воспаления осуществляют гормональные, нервные и иммунные факторы. Одни гормоны: соматотропный гормон (СТГ) гипофиза, дезоксикортикостерон, альдостерон — усиливают воспалительную реакцию (провоспалительные гормоны). Другие: глюкокортикоиды и адренокортикотропный гормон гипофиза — напротив, уменьшают ее (противовоспалительные гормоны). Холинергические вещества, стимулируя выброс медиаторов воспаления, действуют подобно провоспалительным гормонам, а адренергические, угнетая медиаторную активность, ведут себя подобно противовоспалительным гормонам. На выраженность воспалительной реакции, темпы ее развития и характер влияет состояние иммунитета. Особенно бурно воспаление протекает в условиях антигенной стимуляции (сенсибилизации) — иммунное, или аллергическое, воспаление.
Исход воспаления различен в зависимости от его этиологии и характера течения, состояния организма и структуры воспаленного органа. Продукты тканевого распада подвергаются ферментативному расщеплению и фагоцитарной резорбции, происходит рассасывание продуктов распада. Благодаря клеточной пролиферации очаг воспаления постепенно замещается клетками соединительной ткани. Если очаг воспаления небольшой, может наступить полное восстановление ткани. При значительном дефекте ткани на месте очага образуется рубец.
