
920
.pdfthe fertilizers containing Cd, increase the content of Cd in the agricultural soils. The effects of Cd on photosynthetic activities are a subject of intensive investigations, and chlorophyll fluorescence estimation could bean accurate tool to the precise determination of the physiological state of plants. The maximal quantum yield of photosystem II (PSII) (Fv/Fm) is one of the most important parameters of chlorophyll fluorescenceestimation.The quantum yield of PSII is an indication of dissociation of light-harvesting pigment systems of PSII. The disturbance in quantum yield of PSII could indicate a decline in the photosynthetic efficiency which may affect electron transport, thylakoid number per granum, transpiration rate and stomatal conductance [3, 4]. Chlorophyll fluorescence has great potential as a tool to monitor the interaction between soil pollutant and plants[5-7].
Several organic and inorganic soil amendments are applied to contaminated soil for improving its physical, chemical, and biological characteristics. The biochar is widely used as a soil amendment; however, the diatomite is also attracted scientific attention andproved to be a very promising and effective adsorbent in HMs-contaminated soils[8].
To reveal the effects of Cd stress and role of biochar and diatomite on the chlorophyll fluorescence of barley, the experiment was conducted on Cd polluted soil.
Materials and Methods. The upper (0- to 20-cm) layer of Haplic Chernozem was used for the model experiment. Soilwas sampled from a reserved virgin plot in the Persianovskaya steppe in the Rostov region(south of the European part of Russia). The soil had the following properties (g kg–1): Corg 0.37;CaCO3 0.04; physical clay 6.36; clay 2.81; pHH2O 7.6; exchangeable bases (cmolc kg–1): Ca2+31.0, Mg2+ 6.0, Na+ 0.06. Soil samples were analyzed by the commonly used Standard methodfor the Russian Federation (Vorob’eva, 2006).
The sampled soilswere sieved by2 mm size of sieve.The 2 kg well mixed soils were filled in plastic pots with a closed drainage system for model experiment. The experimental design included the control (original uncontaminated soil) and treatments with the addition of Cd 10 mg kg–1 in triplicate. Soil incubated at room temperature in normal mode of lighting for one month. After one month of incubation, biochar (2.5%) and diatomite (2.5%) were applied. Then, the 15 seeds were sown per pot at 2 cm depth.
Plants were dark-adapted in the laboratory room with dark curtains and no artificial light source for 20 min before chlorophyll fluorescence measurements. During the measurement, the room temperature was the same as the growth environment of plants. The maximal quantum yield of PSII was measured using pulse amplitude modulated (PAM) fluorometer (Diving PAM, Waltz, Germany). Photosynthetic photon flux density (PPFD) of red measuring light was 0.15 mmol photons m–2 s–1 and PPFD of white saturating flash was 1800 mmol photons m–2 s–1. Fifteen readings were recorded by selecting fresh leaves and all the leaves were measured under the same condition.
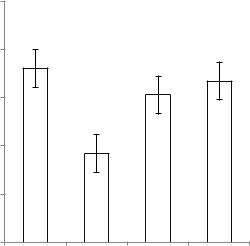
Results and discussion. The results showed that Cd suppressed maximal quantum yields of PSII of barley, while, the addition of biochar and diatomite improved the photosynthetic performance than the Cd stressed barley. The maximal quantum yields of PSII decreased by 11.28% in barley grown in Cd-polluted soil with compared to control whereas; this decrease was less in biochar (3.6%) and diatomite (1.67%) appliedtreatments (Figure 1). Biochar and diatomite amendments in polluted soil alleviate the soil Cd toxicity.
260
Maximal quantum yield of PS II (Fv/F
0,85
0,8
0,75
0,7
0,65
0,6
Control |
Cd |
Cd+ 2.5% |
Cd + 2.5% |
|
|
biochar |
diatomite |
Treatment
Figure 1.Assessment of maximal quantum yield of photosystem II (Fv/Fm) of photosynthetic performance of barley in Cd polluted with amendments
The reduction in barley growth and biomass could be a reason for the inhibition of photosynthesis [9, 10]. The decline in photosynthesis efficiency also affects electron transport, transpiration rate and stomatal conductance [3, 4, 6]. The application of 2.5% pine wood biochar alleviated Cd toxicity for barley grown in highly multi-metals polluted soil [11]. The improvement in barley growth may be due to increases in water retention by application of the biochar and diatomite[12, 13]. Another study showed that the application of 5% rice straw biochar decreased the bioavailability of Cd, and improved microbial counts and soil enzyme activities [14]. The studies indicate the application of diatomite improve the growth and photosynthetic pigments, helping plants to overcome from various biotic and abiotic stresses, especially metal-stress [8, 13, 15].
Conclusion. Chlorophyll fluorescence has proven to be a non-destructive, quick, and accurate tool to the precise determination of the physiological state of barley grown in Cd-polluted soil. The results indicated biochar and diatomite application to Cd-polluted soil improved the photosynthetic activities of barley. Thus, this work suggests biochar, as well as diatomite, have the potential to be used as a useful amendment to alleviate plant stress and remediate Cd-contaminated soil.
Acknowledgement: This research was supported by the Grant of President of Russian Federation, projects no. МК-2818.2019.5 andMK-2973.2019.4, Grant of the President to support Leading scientific schools No. NSh-3464.2018.11,RFBR (No. 19- 29-05265мк).
References
1.Prasad MNV: Cadmium toxicity and tolerance in vascular plants. Environmental and Experimental Botany 1995, 35(4). P. 525-545.
2.Sanità di Toppi L, Gabbrielli R: Response to cadmium in higher plants. Environmental and Experimental Botany 1999, 41(2):105-130.
3.Da Costa MVJ, Sharma PK: Effect of copper oxide nanoparticles on growth, morphology, photosynthesis, and antioxidant response in Oryza sativa. Photosynthetica 2015, 54(1):110-119.
4.Perreault F, Samadani M, Dewez D: Effect of soluble copper released from copper oxide nanoparticles solubilisation on growth and photosynthetic processes of Lemna gibba L. Nanotoxicology 2014, 8(4):374-382.
261
5.Moustakas M, Malea P, Haritonidou K, Sperdouli I: Copper bioaccumulation, photosystem II functioning, and oxidative stress in the seagrass Cymodocea nodosa exposed to copper oxide nanoparticles. Environ Sci Pollut Res Int 2017, 24(19):16007-16018.
6.Rajput V, Minkina T, Fedorenko A, Sushkova S, Mandzhieva S, Lysenko V, Duplii N, Fedorenko G, Dvadnenko K, Ghazaryan K: Toxicity of copper oxide nanoparticles on spring barley ( Hordeum sativum distichum). Science of The Total Environment 2018, 645:1103-1113.
7.Lysenko VS, Varduny TV, Kosenko PO, Kosenko YV, Chugueva OI, Semin LV, Gorlachev IA, Tarasov EK, Guskova OS: Video registration as a method for studying kinetic parameters of chlorophyll fluorescence in Ficus benjamina leaves. Russian Journal of Plant Physiology 2014, 61(3):419-425.
8.Zhao Y, Tian G, Duan X, Liang X, Meng J, Liang J: Environmental Applications of Diatomite Minerals in Removing Heavy Metals from Water. Industrial & Engineering Chemistry Research 2019, 58(27):11638-11652.
9.Shanmugaraj BM, Malla A, Ramalingam S: Chapter 1 - Cadmium Stress and Toxicity in Plants: An Overview. In: Cadmium Toxicity and Tolerance in Plants. Edited by Hasanuzzaman M, Prasad MNV, Fujita M: Academic Press; 2019: 1-17.
10.Dong J, Wu F-B, Zhang G-P: Effect of cadmium on growth and photosynthesis of tomato seedlings.
Journal of Zhejiang University Science B 2005, 6(10):974-980.
11.Gorovtsov A, Rajput V, Tatiana M, Saglara M, Svetlana S, Igor K, Grigoryeva TV, Vasily C, Iraida A, Vladislav Z et al: The role of biochar-microbe interaction in alleviating heavy metal toxicity in Hordeum vulgare L. grown in highly polluted soils. Applied Geochemistry 2019, 104:93-101.
12.Günal E, Erdem H, Çelik İ: Effects of three different biochars amendment on water retention of silty loam and loamy soils. Agricultural Water Management 2018, 208:232-244.
13.Abdalla M: Beneficial effects of diatomite on the growth, the biochemical contents and polymorphic DNA in Lupinus albus plants grown under water stress. Agriculture and Biology Journal of North America 2011, 2:207-220.
14.Li L, Jia Z, Ma H, Bao W, Li X, Tan H, Xu F, Xu H, Li Y: The effect of two different biochars on remediation of Cd-contaminated soil and Cd uptake by Lolium perenne. Environmental Geochemistry and Health 2019.
15.Bello OS, Adegoke KA, Oyewole RO: Insights into the Adsorption of Heavy Metals from Wastewater using Diatomaceous Earth. SeparationScienceandTechnology2014, 49(12):1787-1806.
Т. Минкина, В. Раяпут, В. Чаплыгин, В. Лысенко, И. Сазонов, А. Барбашев, С. Шушкова, Д. Брен, А. Яковленко Южный федеральный университет, Россия
e-mail: tminkina@mail.ru
РОЛЬ БИОХАРА И ДИАТОМИТА В ФОТОСИНТЕТИЧЕСКОЙ АКТИВНОСТИ ЯЧМЕНЯ В ЗАГРЯЗНЕННЫХ КАДМИЕМ ПОЧВАХ
Аннотация: Кадмий является токсичным тяжелым металлом, который наносит прямой вред растениям и людям в нескольких формах. Флуоресценция хлорофилла имеет большой потенциал в качестве инструмента для мониторинга взаимодействия загрязнителя почвы и растений. Эксперимент проводился с целью наблюдения за фотосинтетической активностью ячменя и роли препаратов на почве загрязненной Cd. Биочар является широко используемым препаратом при восстановлении почв, загрязненных тяжелыми металлами из-за его сорбционных свойств. В последнее время диатомит также оказался эффективным адсорбентом для загрязнения почвы. Результаты показали, что токсичность Cd снижала максимальный квантовый выход фотосистемы II (Fv / Fm) на 11,28% по сравнению с контролем (незагрязненная почва), в то время как меньшее снижение было обнаружено при обработке биочаром (3,6%) и диатомитом (1,7%). Препараты на биочар и диатомит в загрязненной почве позволили снизить токсичность Cd и ускорить рост ячменя.
Ключевые слова: Флуоресценция хлорофилла, Тяжелые металлы, Фотосистема II, Физиология, Почва.
262
УДК 631.41
Т.М. Минкина, Д.Г. Невидомская, Ю.С. Подковырина, М.В. Бурачевская, Т.В. Бауэр, В.А. Чаплыгин, С.С. Манджиева Южный федеральный университет, Ростов-на-Дону, Россия
e-mail: tminkina@mail.ru
АНАЛИЗ МОЛЕКУЛЯРНО-СТРУКТУРНОГО СОСТОЯНИЯ МЕДИ В ЗАГРЯЗНЕННОМ ЧЕРНОЗЕМЕ ОБЫКНОВЕННОМ ПРИ ПОСТУПЛЕНИИ МЕТАЛЛА В ФОРМЕ ЛЕГКО-
И ТРУДНОРАСТВОРИМЫХ СОЕДИНЕНИЙ
Аннотация. Проведен анализ молекулярно-структурного состояния меди в загрязненном черноземе обыкновенном при поступлении металла в форме оксида и нитрата. Исследования проводились методом ближней тонкой структуры края рентгеновского поглощения – XANES. Установлена более полная трансформации Cu(NO3)2 в черноземе обыкновенном по сравнению с CuO в течение годичной инкубации металла в почве.
Ключевые слова: медь, чернозем обыкновенный, загрязнение, легко- и труднорастворимые соединения, XANES.
Рентгеновская спектроскопия поглощения является в настоящее время одним из наиболее перспективных методов неразрушающей диагностики локальной атомной и электронной структур материалов без дальнего порядка в расположении атомов. Развитие методов прямого изучения локальной структуры и механизмов закрепления металла в активных твердофазных компонентах почвы стало возможно благодаря использованию анализа тонкой структуры спектра рентгеновского поглощения на базе синхротронного излучения [3]. Важность получения данной информации состоит в том, что до сих пор обсуждаются на уровне гипотез механизмы трансформации металлов в почве при поступлении их в форме различных соединений [4].
Цель работы состояла в изучении пространственно-структурных особенностей меди в черноземе обыкновенном при поступлении металла в форме легко- и труднорастворимых соединений.
Для реализации поставленной цели был проведен специальный эксперимент, в котором чернозем обыкновенный карбонатный был загрязнен высокими дозами Cu(NO3)2 (2000 мг/кг) и CuO (2000 мг/кг и 10000 мг/кг), внесенных раздельно. Инкубация почвы с соединениями Сu проводилась в течение года. Анализ молеку- лярно-структурный состояния меди в почве проводилось методом ближней тонкой структуры края рентгеновского поглощения проводились на спектрометре Rigaku R-XAS Lopper. При измерении спектров рентгеновского поглощения использовался Ge (440) монохроматор, обеспечивающий энергетическое разрешение 0.4 эВ для К-края Cu. Энергетическая калибровка осуществлялась на медной фольге. Спектры XANES K-края меди были сняты в энергетическом диапазоне от 8930 эВ до 9250 эВ [2].
Теоретическое моделирование спектров К-края поглощения меди в CuO и Cu(NO3)2 было проведено методом конечных разностей и методом полного многократного рассеяния, которые реализуются в программных комплексах FDMNES
263
2010 и Feff, соответственно [1]. Расчет потенциала проводился с учетом и без muf- fin-tin приближения. Согласие экспериментальных и теоретических спектров было достигнуто в расчетах, проведенных в полном потенциале (без учета muffin-tin эффектов).
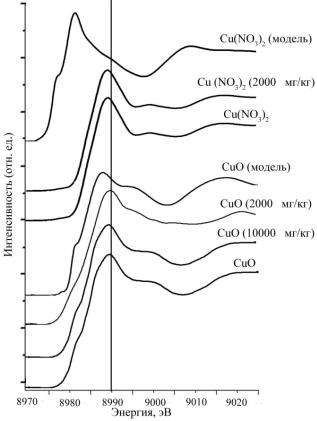
Сравнительный анализ спектров чистого соединения CuO со спектрами почвенных образцов показал, что вне зависимости от дозы загрязнения и вида загрязнения (CuO и Cu(NO3)2), состояние меди не изменяется (Рисунок 1). Экспериментальные XANES спектры имеют сходный вид с пиком в серединной части края спектра (~ 8985-8990 эВ).
Эффективность расщепления исходного спектра оценивается по двум критериям. Суммарное содержание металла в модели должно приближаться к 100%, а «остаток», обусловленный ошибкой модели, должен стремиться к 0. Как видно из рисунка, почвенный спектр занимает промежуточное положение между спектрами модельного и экспериментального образцов исследуемых соединений металлов. Амплитуда и частота волны экспериментальных спектров воспроизведены в виде нитрата Сu, в случае загрязнения почв данной солью металла, или в виде оксида Сu, в случае загрязнения им почвы. Согласие модельного и экспериментального спектров высокое.
Рисунок 1. Экспериментальные и модельные спектры и рентгеновского поглощения XANES для чистых Cu содержащих соединений
и загрязненных ими почвенных образцов
Сходный характер в величине интенсивности предкраевого пика в спектрах почвенных образцов, насыщенных CuO и Cu(NO3)2 указывает, что поглощенная медь имеет ярко выраженную асимметрию первой атомной оболочки, такую же,
264
как в спектрах чистых соединений меди. Форма, размер и особенности в краевой и вблизи краевой областей спектров почвенных образцов, насыщенных CuO и Cu(NO3)2, имеют четкие различия, что, в первую очередь, зависит от локальной атомной структуры окружающей центральный атом меди. Во-вторых, позволяет предположить, что сорбированные комплексы Cu XANES спектров CuO и Cu(NO3)2 образуют различные фазы локальной атомной структуры.
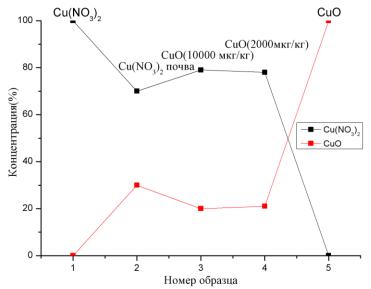
Для оценки вклада содержания меди проведена аппроксимация экспериментальных спектров с применением анализа принципиальных компонент (Рисунок 2), реализованным в программном комплексе FitIt [1]. Используя данный метод возможно уточнение структуры одной из смешанных компонент и определение процентного содержания компонентов для всех экспериментальных спектров. Анализ основных компонент позволил разложить серию экспериментальных почвенных спектров на суперпозиции нескольких экспериментальных спектров «чистых» эталонных компонентов и определить число данных чистых спектров, смешанных в серии экспериментов и их концентрации.
За эталоны приняты спектры чистых соединений нитрата и оксида меди. Исходя из полученных данных процент содержания оксида и нитрата меди в почвенных спектрах достигает более 70% относительно эталонных спектров, где их содержание составляет 100% (Таблица).
Рисунок 2. Аппроксимация экспериментальных спектров нитрата и оксида Cu относительно чистых медьсодержащих спектров
Таблица
Результаты анализа принципиальных компонент по аппроксимации экспериментальных спектров нитрата и оксида меди
Компонент |
Cu(NO3)2 |
CuO |
Cu(NO3)2 |
100% |
0 |
Cu(NO3)2 почва |
70% |
30% |
CuO (10000 мкг/кг) |
79% |
20% |
CuO(2000 мкг/кг) |
78% |
21% |
CuO |
0 |
100% |
Данный анализ показал, что при сопоставлении экспериментальных почвенных спектров нитратов меди с аппроксимированным модельным наблюдается хорошая воспроизводимость данных спектров, что указывает на большой вклад меди
265
из нитратов, ассоциированных в составе почвенных компонентов с образованием Cu-содержащих фаз. Исходя из аналогичного соотношения спектров оксидов можно предположить незначительное участие меди в образовании содержащих ее почвенных фаз.
Таким образом, хорошее соответствие между модельными спектрами и экспериментальными XANES спектрами показывает, что теоретическое моделирование центров поглощения, участвующих в образовании связей, можно успешно использовать для изучения пространственной структуры. Принимая во внимание, что вид спектров почвенных образцов, насыщенных CuO, имеют большую сходимость со спектрами чистого соединения по сравнению со спектрами Cu(NO3)2, а также учитывая различия в произведении растворимости данных соединений, очевидно, что поступление металла в почву в форме легкорастворимого соединения будет способствовать более полной трансформации ионов меди с образованием разнообразных соединений.
Исследование выполнено при финансовой поддержке Российского научного фонда № 19-74-00085.
Литература
1.Смоленцев Г.Ю., Солдатов А.В. Рентгеновская спектроскопия – анализ наноразмерной структуры вещества. Ростов-на-Дону: Мини-Тайп. 2006. 88 с.
2.Bianconi A. XANES spectroscopy. In X-ray absorption: principles, applications and techniques of EXAFS, SEXAFS and XANES / Edited by R. Prins and D.C. Koningsberger New York: John Wiley& Sons. 1988. 573 p.
3.Gräfe M., Donner E., Collins R.N., Lombi E. Speciation of metal(loid)s in environmental samples by X- ray absorption spectroscopy: A critical review // Analytica Chimica Acta. 2014. V. 822. P. 1-22.
4.Minkina T.M., Bauer T.V., Batukaev A.A. et al. Transformation of technogenic Cu and Zn compounds in chernozem // Environmental Engineering and Management Journal. 2015. V. 14. No. 2. P. 481-486.
T.M. Minkina, D.G. Nevidomskaya, Yu.S. Podkovyrina, М.V. Burachevskaya, T.V. Bauer, V.A. Chaplygin, S.S. Mandzhieva
Southern Federal University, Rostov-on-Don, Russia
ANALYSIS OF THE MOLECULAR-STRUCTURAL STATE OF COPPER IN ORDINARY CHERNOZEM CONTAMINATED WITH EASILY AND HARDLY SOLUBLE METAL COMPOUNDS
Abstract. The molecular structural state of copper in ordinary chernozem contaminated with oxide and nitrate metal form was analyzed. The studies were carried out by the method of near fine structure of the x-ray absorption edge – XANES. More complete transformation of Cu(NO3)2 in ordinary chernozem was established in comparison with CuO during the annual incubation of metal in soil.
Keywords: copper, ordinary chernozem, contamination, easily and hardly soluble compounds, XANES.
The study was supported by the Russian Science Foundation No. 19-74-00085 References
1.Smolentsev G.Yu., Soldatov A.V. X-ray spectroscopy – analysis of the nanoscale structure of a substance. Rostov-on-Don: Mini-Type, 2006, 88 p.
2.Bianconi A. XANES spectroscopy. In X-ray absorption: principles, applications and techniques of EXAFS, SEXAFS and XANES / Edited by R. Prins and D.C. Koningsberger New York: John Wiley& Sons. 1988. 573 p.
3.Gräfe M., Donner E., Collins R.N., Lombi E. Speciation of metal(loid)s in environmental samples by X- ray absorption spectroscopy: A critical review // Analytica Chimica Acta. 2014. V. 822. P. 1-22.
4.Minkina T.M., Bauer T.V., Batukaev A.A. et al. Transformation of technogenic Cu and Zn compounds in chernozem // Environmental Engineering and Management Journal. 2015. V. 14. No. 2. P. 481-486.
266
УДК 631.4
Т.М. Минкина, Д.Г. Невидомская, В.А. Чаплыгин, С.С. Манджиева, Ю.А. Литвинов Южный федеральный университет, Ростов-на-Дону, Россия
e-mail: tminkina@mail.ru
ОСОБЕННОСТИ РАСПРЕДЕЛЕНИЯ ТЯЖЕЛЫХ МЕТАЛЛОВ В РАСТИТЕЛЬНОСТИ РАЙОНА ПРОМЫШЛЕННЫХ ОТСТОЙНИКОВ СТОЧНЫХ ВОД
Аннотация. На примере импактной зоны промышленных отстойников сточных вод и шламонакопителей (г. Каменска-Шахтинского Ростовской области) показано влияние долгосрочного химического загрязнения высокими уровнями тяжелых металлов на дикорастущие растенияв техногенных мезофильных сукцессиях.
Ключевые слова: тяжелые металлы, импактная зона, растительность ,загрязнение.
Для растений высокий уровень загрязнения среды обитания является стрессовым фактором, вызывающим интегральный ответ, направленный на выживание биосистем за счет формирования защитных механизмов [4, 7]. Растения, обитающие в условиях длительного воздействия химического загрязнения, не имея возможности «уйти» от влияния стресса, фактически вынуждены приспосабливаться к нему, мобилизуя свои внутренние защитные ресурсы. Целью исследования было изучить и выявить особенности накопления некоторых тяжелых металлов (ТМ) растениями – эдификаторами техногенных мезофильных сообществ.
Каменский район расположен в пределах Среднедонской подпровинции Понтической провинции Евразиатской степной области [2]. До начала работы промышленных предприятий г. Каменска-Шахтинского на месте хранилищ промстоков были пойменные луга и живописные озера. Однако техногенные трансформации, обусловленные деятельностью промышленных предприятий и химических заводов, образующих кластер промзоны г. Каменска-Шахтинского, способствовали тому, что в пойме реки Северского Донца доминирующей стала техногенная мезофильная сукцессия района озера Атаманское. Данное озеро с начала 60-х годов использовалось в качестве резервуара для промстоков сброс которых осуществлялся до середины 90-х годов XX века [6]. Растительность данного района представлена монодоминантными тростниковыми группировками, состоящими из тростника южного (Phragmitesaustralis Cav.) и растений кондоминантов, среди которых встречаются: коровяк обыкновенный (Verbascumthapsus L.), полынь австрийская (Artemisiaaustriaca), тысячелистник благородный (Achilléanóbilis), цикорий обык-
новенный (Cichóriumíntybus), пижма обыкновенная (Tanacétumvulgáre).
Почвы района исследования представляют собой техногенно-трансформи- рованные отложения, которые согласно классификации и диагностики почв России [5] относятся к хемоземам.
Стандартные укосы растений проводили в естественных местообитаниях. С каждой площадки мониторинга формировали среднюю пробу из растений, принадлежащих к одному виду. Объединенная проба растений состояла из 8-10 точечных проб. Пробоподготовку растительного материала осуществляли методом сухого
267
озоления [3] с последующей кислотной экстракцией ТМ из золы 20% HCl. Определение металлов в растениях проводилось на атомно-адсорбционном спектрофотометре. Полученные показатели сравнивались с максимально допустимыми уровнями ТМ, принятыми для кормовых трав [1].
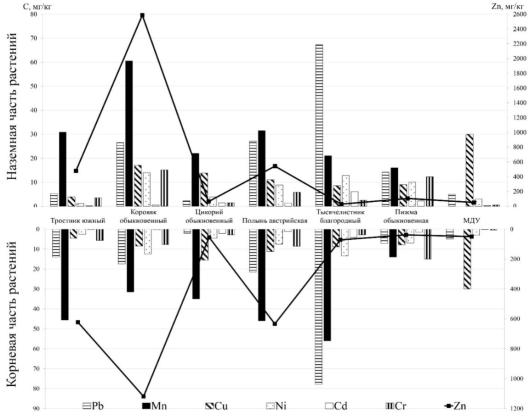
По величине абсолютного содержания в растениях исследуемой территории ТМ располагаются в следующем порядке: Zn>Mn>Pb> Cu ≥ Cr>Ni>Cd.Во всех растительных образцах площадок мониторинга, прилегающих к озеру Атаманскому, установлены превышения МДУ для Zn и Cr. На некоторых площадках превышения МДУ также диагностируется для Pb, Сd иNi. Особенно высокие концентрации Znотмечаются на площадках мониторинга, которые приурочены к «очагам загрязнения» промстоков.
Рисунок. Среднее содержание Pb, Zn, Cu, Ni, Cd, Cr и Mn в надземной
и корневой частях разных видов растений, произрастающих на площадках мониторинга района озера Атаманского промзоны г. Каменска-Шахтинского Ростовской области, мг/кг
Биогеохимическая ситуация, складывающаяся в импактной зоне района озера Атаманского, показывает, что в данных естественных условиях растительные сообщества адаптировались к избыточным концентрациям металлов в почвах. Следует отметить, что изменения в составе луговых ассоциаций не могут быть объяснены только прямым действием веществ-загрязнителей на чувствительные растения. Здесь вступают в силу законы межвидовой конкуренции за факторы роста и жизненное пространство. В структуре сообществ повышается значение видов растений с большей экологической амплитудой: тростник южный (семейства Мятли-
268
ковые), коровяк обыкновенный (семейства Норичниковые), на позиции кондоминантов выходят виды, менее приспособленные к новым, худшим условиям обитания. Это растения из семейства сложноцветных (Астровые) – полынь австрийская, тысячелистник благородный; цикорий обыкновенный, пижма обыкновенная и пр.
Различия в содержании Zn в растениях коровяка обыкновенного, произрастающих на фоновых незагрязненных и загрязненных почвах, составляют для корневой части растений до 66 раз, а для надземной части до 200 раз.
Не вызывает сомнений, что основной фактор загрязнения растений – это долгосрочная аккумуляция ТМ в почве. Показано, что основными аккумуляторами доминирующего поллютанта – Zn выступают растения тростника и коровяка в силу их морфолого-анатомического и физиологического строения. Выявленные превышения МДУ по абсолютным значениям составили для коровяка:Zn до 96 раз, Pb до 12 раз, Ni до 48 раз, Cr до37 раз, Cd до 4 раз. Причем, аккумуляция ТМ у растений коровяка, преимущественно, отмечается в надземной части (Рисунок). В растениях тростника выявлены превышения по Zn до 22 раза, Pb до 5 раз, Cr до 18 раз, наибольшие содержания металлов депонируются в подземной части, поскольку широко разветвленные в почве корневища тростниковых зарослей, известны своей высокой аккумулирующей активностью [10]. На рисунке представлены средние содержания Pb, Zn, Cu, Ni, Cd, Cr и Mn в надземной и корневой частях исследуемых видов дикорастущих растений.
Особенности аккумуляции ТМ растениями можно представить рядами накопления металлов согласно среднему абсолютному содержанию в частях растений разных видов:
Надземная часть:
Коровяк обыкновенный: Zn>Mn>Pb> Cu ≥ Cr>Ni>Cd;
Тростник южный: Zn>Mn>Pb> Cu ≥ Cr>Ni>Cd;
Полынь горькая: Zn>Mn>Pb> Cu ≥ Ni>Cr ≥ Cd; Тысячелистник благородный: Pb>Zn>Mn> Cu ≥ Ni>Cr ≥ Cd; Пижма обыкновенная: Zn>Mn>Pb> Cr ≥ Ni> Cu ≥ Cd; Цикорий обыкновенный: Zn>Mn>Cr>Ni ≥ Pb> Cu≥ Cd; Корневая часть:
Коровяк обыкновенный: Zn>Mn>Pb>Ni ≥ Cu>Cr>Cd;
Тростник южный: Zn>Mn>Pb> Cr ≥ Cu>Ni>Cd;
Полынь горькая: Zn>Mn>Pb> Cu ≥ Cr>Ni ≥ Cd; Тысячелистник благородный: Pb>Zn>Mn>Ni ≥ Cu>Cd ≥ Cr; Пижма обыкновенная: Zn>Cr>Mn> Cu ≥ Pb> Cr ≥ Cd; Цикорий обыкновенный: Zn>Mn>Cu>Ni ≥ Cr>Pb ≥ Cd.
На основании приведенных рядов установлено, что основную роль в накоплении ТМ разными видами растений при очень высоком уровне загрязнения почв играет техногенный фактор.
Анализ данных позволил установить, что видами-аккумуляторамиZn являются коровяк и тростник [8, 9]. Выявлено, что коровяк из рассматриваемых растений накапливает в своей надземной массе наибольшее количество Mn, Pb иNi, а тысячелистник –Pb.
Таким образом, по величине абсолютного содержания в растениях ТМ располагаются в следующем порядке: Zn>Mn>Pb> Cu ≥ Cr>Ni>Cd. Во всех растительных образцах площадок мониторинга, прилегающих к озеру Атаманскому, установлены превышения МДУ для Zn и Cr. Определены виды-аккумуляторы Zn –
269
