
Urologia_-_Komyakov_Urologia_2012
.pdfнеосложненном течении ДГПЖ составляет до 80 %. В зависимости от сроков медикаментозного лечения ДГПЖ задачи делятся на:
1)краткосрочные - уменьшение СНМП и профилактика острой задержки мочеиспускания;
2)долгосрочные - улучшение уродинамики, предотвращение хирургических вмешательств, осложнений и прогрессирования заболевания;
3)общие - сохранение и улучшение качества жизни, минимизация побочных эффектов лечения.
Лекарственная терапия должна быть направлена на все компоненты инфравезикальной обструкции:
■ уменьшение размеров предстательной железы (статический компонент обструкции); ■ расслабление гладкомышечных элементов, ее капсулы, шейки мочевого пузыря и
задней уретры (динамический компонент); ■ устранение ишемии детрузора (трофический) и снятие отека простаты
(воспалительный компонент).
Идеального препарата для лечения ДГПЖ нет, поэтому подбирать терапию надо строго индивидуально с учетом ее эффективности и безопасности. В настоящее время предложено большое количество лекарственных средств для лечения ДГПЖ:
1)α-адреноблокаторы (α-АБ): селективные (α1) - празозин, альфузозин, доксазозин, теразозин и др.; суперселективные (α1А) - тамсулозин;
2)ингибиторы 5-α-редуктазы: синтетические - финастерид, дутастерид; растительные -
экстракты Serenoa repens, Pygeum africanum и др.;
3)тканевые препараты - простаты экстракт (раверон, простатилен);
4)полиеновые антибиотики - леворин, ипертрофан;
5)гормоны: аналоги лютеинезирующего рилизинг-гормона - гозерелин (золадекс), бусерелин; антиандрогены - флутамид, бикалутамид (касодекс), ципротерон (андрокур); гестагены - депостат; андрогены, эстрогены, антиэстрогены, ингибиторы ароматазы, антагонисты пролактина;
6)фитопрепараты - экстракты пальмы сабал, уртирон, масло семян тыквы и др.;
7)гомеопатические средства - афала.
Среди большого арсенала лекарственных препаратов только α1-адреноблокаторы и ингибиторы 5-α-редуктазы являются основными средствами медикаментозного лечения ДГПЖ. Их эффективность доказана международными исследованиями и многолетней клинической практикой. Применение α-адреноблокаторов приводит к расслаблению гладкомышечных элементов шейки мочевого пузыря и простаты, устранению гипоксии и улучшению энергетического метаболизма в детрузоре. Они представляют собой препараты первой линии лечения больных ДГПЖ при наличии СНМП (IPSS > 8-35), так как: 1) обеспечивают быстрое симптоматическое улучшение (по шкале IPSS) уже на 1-2-й неделе лечения независимо от размеров простаты; 2) эффективны в отношении обструктивных и ирритативных симптомов; 3) не влияют на уровень ПСА; 4) удобны в применении (прием 1 или 2 раза в сутки). Желаемого результата при использовании всех α-адреноблокаторов, за исключением тамсулозина, можно добиться за счет увеличения дозы и кратности приема препарата.
В клинической практике используют селективные α-адреноблокаторы (теразозин, доксазозин, альфузозин и др.) и суперселективные α1А-адренобло-каторы (тамсулозин).
Все селективные α-адреноблокаторы имеют примерно одинаковую клиническую
эффективность и частоту побочных реакций (10-16 %) в виде недомогания, слабости, головокружения, головной боли, ортостатической гипотензии (2-5 %), тахикардии и тахиаритмии. Наименьшими побочными явлениями обладает тамсулозин.
α1-Адреноблокаторы устраняют динамический компонент инфравезикальной обструкции, но не влияют на прогрессирование ДГПЖ. Замедляют рост предстательной железы ингибиторы 5-α-редуктазы II типа - финастерид и дутастерид. Аналогичным
механизмом действия, но со значительно меньшей эффективностью обладают растительные препараты - экстракты Serenoa repens, Pygeum africanum и др. При длительной, не менее 6-12 мес, терапии ингибиторами 5-α-редуктазы риск прогрессирования ДГПЖ снижается почти на 70 %, так как уменьшаются объем простаты, выраженность СНМП (IPSS), уровень ПСА, вероятность острой задержки мочеиспускания
ириск оперативного вмешательства. Среди редких нежелательных явлений терапии следует отметить эректильную дисфункцию, снижение либидо, уменьшение объема эякулята и гинекомастию. Прием ингибиторов 5-α-редуктазы снижает кровоток в простате
иуменьшает гематурию, связанную с самим заболеванием и хирургическими вмешательствами на простате.
Пациентам с ДГПЖ, имеющим СНМП (IPSS >8-35), и с установленным риском прогрессирования заболевания (объем простаты более 30 см, уровень ПСА от 1,5 до 10 нг/мл) показана наиболее эффективная комбинированная терапия α- адреноблокаторами и ингибиторами 5-α редуктазы, так как она обеспечивает
быстрое симптоматическое улучшение и уменьшение объема предстательной железы.
Остальные лекарственные средства относятся к препаратам второго ряда и применяются в лечении больных ДГПЖ как вспомогательные средства для уменьшения
выраженности симптомов или в комплексной терапии в сочетании с α1- адреноблокаторами и/или ингибиторами 5-α-редуктазы.
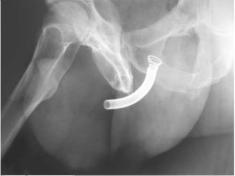
Малоинвазивные методы лечения: установка постоянных, временных (съемных) или рассасывающихся стентов (эндопротезов) в простатическом отделе уретры под эндовидеорентгенологическим контролем (рис. 11.35), термальные методы - используются при абсолютных противопоказаниях к хирургическим вмешательствам.
Уретральные стенты препятствуют сдавливанию просвета мочеиспускательного канала гиперплазированной тканью простаты, но имеют высокий риск осложнений, связанный с инкрустацией солями, инфекцией и болевым синдромом.
Рис. 11.35. Обзорная рентгенограмма. Спиралевидный металлический эндопротез, установленный больному с ДГПЖ в простатический отдел уретры
Многочисленные термальные методы основаны на физическом воздействии на гиперплазированную ткань высоких и низких температур от тепловых, радиочастотных (электромагнитных), лазерных и ультразвуковых источников, установленных в уретре или прямой кишке на уровне простаты. В зависимости от вида и фокуса излучения по мере повышения температуры от 42-45 до 120 °C в ткани гиперплазированной простаты возникают морфологические изменения, характеризующиеся нарушением микроциркуляции, разрушением о -адренорецепторов, подавлением клеточной пролиферации, дистрофией и образованием очагов некроза с их последующим склерозированием.
К неэндоскопическим методам электромагнитного воздействия относятся трансректальная (40-42 °C) и трансуретральная гипертермия (40-45 °C), трансуретральная термотерапия (45-70 °C), термодеструкция или термоаблация (70-82 °C).
Трансуретральная радиочастотная термотерапия (TUMT) и термодеструкция (TUNA) приводят к образованию очагов коагуляционного некроза в глубине простаты. В отличие от вышеперечисленных методов высокоинтенсивный фокусированный ультразвук (HIFU) с помощью специального трансректального зонда и компьютерной программы наведения позволяет создать локальное повышение температуры до 80-120 °C. В результате деструкция возникает только в заданных точках простаты, не затрагивая окружающие органы и ткани.
Наименее безопасной считается интерстициальная лазерная коагуляция, которая заключается в непосредственном введении в ткань простаты остроконечных световодов, нагревающих ее до 66-100 °C.
Хирургическое лечение. Показаниями к оперативному лечению ДГПЖ являются:
■отсутствие эффекта от длительной медикаментозной терапии с нарастанием обструктивных и ирритативных симптомов, отрицательно влияющих на повседневную активность пациента;
■увеличение количества остаточной мочи (более 100 мл);
■повторяющиеся острые задержки мочеиспускания;
■рецидивирующая инфекция мочевыводящих путей;
■камни мочевого пузыря;
■неоднократная макрогематурия, рефрактерная к терапии ингибиторами 5-а- редуктазы;
■гидроуретеронефроз и хроническая почечная недостаточность.
Оперативное вмешательство не следует выполнять на ранних стадиях ДГПЖ, когда преобладают ирритативные симптомы, так как оно не приносит облегчения больному.
Выделяют паллиативные и радикальный методы оперативного лечения ДГПЖ.
При паллиативных методах предстательная железа не удаляется (эпицистостомия - троакарная или открытая) или удаляется только ее часть (ТУР предстательной железы и ее модификации - электроинцизия, электровапоризация, роторезекция и лазерная вапоризация).
Радикальный метод - аденомэктомия (простатэктомия), которая может быть выполнена как эндоскопически (трансуретрально) - трансуретральная аденомэктомия с электроэнуклеацией гиперплазированной предстательной железы единым блоком или удалением всей аденоматозной ткани путем трансуретральных срезов, так и открытым способом (чреспузырным или позадилонным доступом).
Данные оперативные вмешательства выполняют как в экстренном, так и в плановом порядке. Показаниями к экстренной операции служат острая задержка мочеиспускания, в том числе с наличием ложного хода уретры после неудачной катетеризации мочевого пузыря, и профузная макрогематурия. Она может быть выполнена паллиативно или радикально. Выбор объема экстренной операции зависит от длительности задержки мочеиспускания, наличия и обострения воспалительных заболеваний мочеполовых органов, функционального состояния мочевых путей и почек и выраженности сопутствующей патологии.
Степень увеличения гиперплазированной простаты не служит показанием к хирургическому лечению, но является определяющим фактором при выборе между эндоскопическим и открытым методами операции. Аденомэктомия - единственный радикальный метод лечения ДГПЖ.
Эпицистостомия (надлобковое дренирование мочевого пузыря) заключается в установке в мочевой пузырь через его переднюю стенку дренажной трубки (катетеров Пеццера, Фолея). Она может быть выполнена открытым способом - путем высокого сечения мочевого пузыря или в результате пункции его троакаром, по которому в полость мочевого пузыря устанавливают дренажную трубку, после чего троакар удаляют (рис.
11.36).

Рис. 11.36. Троакарная эпицистостомия
Последний способ предпочтителен. Эпицистостомию выполняют при острой и хронической задержке мочеиспускания как временную меру для улучшения функции мочевых путей и почек и купирования обострения мочевой инфекции. У ослабленных больных с высоким риском хирургических вмешательств надлобковый дренаж может оставаться пожизненно.
После надлобкового дренирования мочевого пузыря необходимо проводить мониторинг объема циркулирующей жидкости, АД, концентрации электролитов в связи с возможным развитием угрожающих жизни нарушений водно-электролитного и кислотноосновного баланса. Иногда эпицистостомия в результате декомпрессии мочевого пузыря может спровоцировать кровотечение из расширенных вен его стенки.
Трансуретральная электрорезекция предстательной железы - один из основных методов лечения ДГПЖ. Данным методом можно резецировать или удалить предстательную железу любых размеров, однако ее оптимальный объем не более 80 см3, так как ТУР большей по объему гиперплазированной ткани удлиняет время вмешательства, сопровождается большей кровопотерей и может привести к ТУРсиндрому. Техника операции заключается в послойном срезании кусочков простаты с эвакуацией их через тубус резектоскопа (см. 4.9, рис. 5-10 на цв. вклейке). Модификациями классической ТУР являются электроинцизия простаты (рассечение ее долей), электровапоризация (выпаривание тканей предстательной железы) и роторезекция.
В тех случаях, когда в процессе ТУР удаляют всю ткань гиперплазированной предстательной железы, она носит радикальный характер, и операцию называют трансуретральной аденомэктомией (рис. 11.37).
Рис. 11.37. Трансуретральная электрорезекция ДГПЖ в полном объеме (аденомэктомия)
Трансуретральную аденомэктомию можно выполнить, используя другую технику операции, которая заключается в биполярной электроэнуклеации простаты единым блоком (TUEB). Оказавшуюся в мочевом пузыре вылущенную железу размельчают специальным прибором (марцеллятором) и удаляют через тубус резектоскопа. Противопоказание к выполнению трансуретральных эндоскопических операций - невозможность помещения больного в кресло из-за анкилоза тазобедренных суставов.
Осложнениями трансуретрального эндоскопического лечения ДГПЖ являются кровотечения, развитие ТУР-синдрома, инфекция мочевых путей, а в отдаленном периоде - сужения мочеиспускательного канала, шейки мочевого пузыря, недержание мочи и ретроградная эякуляция. ТУР синдром (водная интоксикация организма) происходит в результате попадания гипоосмолярной ирригационной жидкости через резецированные стенки вен в системный кровоток. Возникающие при этом нарушения осмолярности крови и ее электролитного состава (гипонатриемия, гипокалиемия) сопровождаются резким ухудшением состояния больного с нарушением сердечной деятельности, падением артериального давления, гемолизом крови, развитием острой почечной и печеночной недостаточности.
Открытую аденомэктомию (простатэктомию) выполняют на протяжении уже более 100 лет. Смысл операции заключается в удалении (бимануальном вылущивании) гипертрофированной предстательной железы (аденомы) из ее хирургической капсулы. С этой целью использовали различные доступы. В настоящее время применяют только два - позадилонный и чреспузырный. Оба начинаются с нижнесрединного внебрюшинного разреза. При позадилонном доступе мочевой пузырь не вскрывают, а гиперплазированную предстательную железу удаляют после вскрытия передней поверхности хирургической капсулы аденомы.
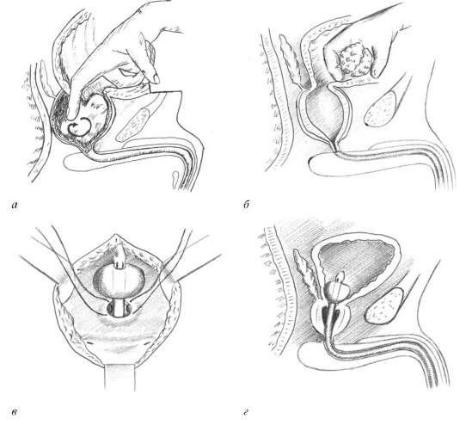
Рис. 11.38. Этапы чреспузырной аденомэктомии: а - энуклеация аденоматозной ткани единым блоком; б - извлечение аденомы через надлобковую рану мочевого пузыря; в
- гемостатические швы изнутри мочевого пузыря на ложе аденомы; г - дренирование мочевого пузыря по уретре трехходовым катетером Фолея
Наибольшее распространение получил чреспузырный доступ. После вскрытия мочевого пузыря и его ревизии капсулу аденомы вскрывают электроножом или тупо пальцем. Аденоматозную ткань вылущивают по частям или единым блоком и удаляют (рис. 11.38, а, б). По уретре в мочевой пузырь устанавливают катетер Фолея, на края ложа удаленной аденомы накладывают гемостатические швы (рис. 11.38, в). Мочевой пузырь ушивают наглухо, а дренирование его осуществляют за счет введенного по мочеиспускательному каналу трехходового катетера Фолея (рис. 11.38, г). Преимуществами чреспузырной аденомэктомии являются хороший осмотр предстательной железы и мочевого пузыря, при необходимости возможность удаления камней, опухолей, дивертикулов, визуальный контроль за всеми этапами удаления аденомы, ревизия раны и выполнение тщательного гемостаза путем ушивания стенок ложа и кровоточащих сосудов.
Операцию заканчивают дренированием мочевого пузыря путем эпицистостомии и/или установления по уретре трехходового катетера Фолея. Предпочтителен последний вид дренирования.
Основными осложнениями чреспузырной аденомэктомии являются ранние и поздние кровотечения, тромбоэмболия легочной артерии, инфекционно-воспалительные процессы, а в отдаленном периоде - рубцовая деформация ложа удаленной аденомы, недержание мочи, цистит и камнеобразование. Характерное осложнение позадилонной аденомэктомии - остеит лонных костей.
Прогноз благоприятный при правильно выбранном и своевременном лечении. В редких случаях после аденомэктомии может возникнуть рецидив заболевания, который обусловлен неполным удалением гиперплазированной ткани. При отсутствии лечения прогноз неблагоприятный и связан с прогрессированием заболевания, развитием гидроуретеронефроза, хронического пиелонефрита и терминальной хронической почечной недостаточности.
11.6.2. Рак предстательной железы
Эпидемиология. Рак предстательной железы (РПЖ) - одно из самых частых онкологических заболеваний у мужчин. В структуре онкологической заболеваемости среди мужского населения в мире он занимает третье место, в США - первое, в Западной Европе - второе и в России - четвертое, уступая только раку легкого, желудка и кожи. Отличительные особенности РПЖ - существенные географические и этнические различия. По сравнению с азиатскими странами (Китай, Япония), РПЖ в США встречается в 100 раз чаще, превышая 100 случаев на 100 000 населения. Частота заболевания у этнических китайцев (японцев), эмигрировавших в США, увеличивается, но не достигает показателей коренного населения. Наиболее часто РПЖ встречается у представителей черной расы, но самая высокая заболеваемость наблюдается в популяции афроамериканцев (116/100 000), что почти в 2 раза выше, чем среди белых американцев. Если в мире ежегодный прирост РПЖ составляет 3 % в год, то в России 6-8 %, и по темпу прироста он занимает первое место среди всех злокачественных новообразований у мужчин. До 60 % больных с впервые выявленным РПЖ имеют III и IV стадии заболевания.
Этиология и патогенез. Возникновение и рост РПЖ связаны с дисбалансом половых гормонов в процессе старения мужского организма. Андрогенная стимуляция служит одним из пусковых механизмов в развитии заболевания. Подтверждением тому является отсутствие случаев заболеваемости РПЖ у кастрированных мужчин (евнухов). В развитии опухоли основную роль играет тестостерон, который в клетках предстательной железы под воздействием фермента 5-а-редуктазы превращается в значительно более функционально активный андроген дегидротестостерон.

К основным факторам риска РПЖ относятся возраст, генетическая предрасположенность и особенности питания. Постоянное присутствие в рационе витамина Е и селена снижает риск развития РПЖ, и, наоборот, он увеличивается при избыточном потреблении жирной, копченой, жареной мясной пищи и молока, но не зависит от курения и злоупотребления алкоголем. Установлено, что 9-10 % РПЖ обусловлены генетическими причинами, однако ген, связанный с развитием РПЖ, пока не обнаружен. Вероятность заболевания увеличивается в 2-3 раза, если у родственников первой линии (отец, родной брат) РПЖ был диагностирован в молодом возрасте (до 50 лет), и в 7-8 раз, если были больны два и более кровных родственников.
Возможно, РПЖ переходит в клинические формы в результате прогрессии латентных опухолей под воздействием эндо- и экзогенных факторов. Это подтверждается тем, что среди этнических китайцев, проживающих в США, заболеваемость манифестированным РПЖ в 7 раз, а у японцев в 3 раза выше, чем соответственно в Китае и Японии.
Предстательная железа состоит из пяти зон: центральной, периферической,
переходной, периуретральной и передней фибромускулярной стромы (рис. 11.39).
Рис. 11.39. Зональная анатомия предстательной железы по J. McNeal: А - центральная; В - фибромускулярная; С - переходная; D - периферическая; Е -
парауретральная зона. 1 - семявыделительный проток; 2 - простатическая часть мочеиспускательного канала
Центральная и периферическая зоны - наиболее крупные участки простаты - вместе составляют около 95 % железистой ткани предстательной железы. Центральная зона окружает семявыносящие протоки на их пути от основания простаты к семенному бугорку. Она занимает 15-20 % объема железы, однако РПЖ в ней встречается не более чем в 5-10 % случаев. Периферическая зона - пальпируемая часть железы через
прямую кишку. Она окружает центральную зону, включает основную часть железистой ткани, и в ней берут начало около 70-80 % аденокарцином простаты.
Переходная зона - парные участки предстательной железы, которые располагаются по бокам от простатической уретры на уровне семенного бугорка, - занимают оставшиеся 5 % железы. Самой частой патологией этой зоны является ДГПЖ, которая может приводить к значительному ее увеличению, иногда превышающему по объему остальные участки простаты. В этой зоне рак развивается реже, чем ДГПЖ, и частота его составляет около 20 %. Периуретральные железы располагаются между простатической уретрой и проксимальным гладкомышечным сфинктером мочевого пузыря. Фибромускулярная строма занимает переднюю поверхность простаты и состоит преимущественно из мышечной ткани. Аденокарциномы в двух последних зонах не развиваются.
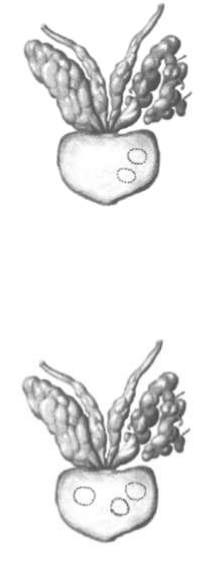
РПЖ и ее доброкачественная гиперплазия развиваются из разных отделов предстательной железы, представляют собой разные по сути и локализации заболевания одного органа, поэтому удаление доброкачественной гиперплазии (аденомэктомия) не является профилактикой РПЖ. В патогенезе РПЖ важную роль играют так называемые переходные состояния: простатическая интраэпителиальная гиперплазия и атипичная пролиферация желез. Они характеризуются дисплазией разной степени выраженности, нарушением структуры эпителия и считаются предраковыми заболеваниями.
Простатическая интраэпителиальная неоплазия (ПИН) представляет собой пролиферацию секреторного эпителия простатических протоков и ацинусов (в пределах эпителиального слоя), при этом происходящие цитологические изменения неотличимы от таковых при карциноме. Различают ПИН 1-й, 2-й и 3-й степени. Клиническое значение имеет только ПИН высокой, 2-й и 3-й степени, так как у этой категории пациентов при повторной биопсии в 30-90 % случаев выявляется РПЖ.
Классификация. Для стадирования РПЖ используется клинико-морфологическая классификация TNM (2010):
Т - первичная опухоль:
Тх - первичная опухоль не может быть оценена; Т0 - нет данных о первичной опухоли;
Т1- опухоль не определяется клинически посредством пальцевого ректального исследования или методами получения диагностического изображения;
Т1а - случайно выявленная опухоль (при ТУР предстательной железы), занимающая менее 5 % резецированной ткани;
Т1b - случайно выявленная опухоль (при ТУР предстательной железы), занимающая более 5 % резецированной ткани;

Т1с - опухоль, обнаруженная при помощи игольчатой биопсии в связи с высоким уровнем ПСА;
Т2 - опухоль ограничена предстательной железой1;
_________
1Опухоль, которая была обнаружена в одной или обеих долях при проведении игольчатой биопсии, но которая не определяется посредством пальцевого ректального обследования или методами получения диагностического изображения, классифицируется как Т1с.
_______
Т2а - опухоль занимает не более половины одной доли; T2b - опухоль занимает более половины одной доли;
Т2с - опухоль локализуется в обеих долях;
Т3 - опухоль прорастает за пределы капсулы предстательной железы1;
________________
1 Инвазия в верхушку предстательной железы или в капсулу (но не за ее пределы) предстательной железы классифицируется не как Т3, а как Т2.
___________

Т3а - экстракапсулярное распространение опухоли;
Т3b - экстракапсулярное распространение опухоли с инвазией семенных пузырьков;
Т4 - опухоль неподвижна или распространяется в отличные от семенных пузырьков прилежащие структуры: шейку мочевого пузыря, наружный сфинктер, прямую кишку, мышцу поднимающую анус и/или стенку таза.
N - регионарные лимфоузлы2:
Nx - регионарные лимфоузлы не могут быть оценены; N0 - нет метастаза в регионарные лимфоузлы;
N1 - метастаз в регионарные лимфоузлы.
________________
2 Регионарные лимфоузлы - это узлы малого таза, которые по существу являются тазовыми узлами, расположенными ниже разветвления общих подвздошных артерий. Латеральность не влияет на N- классификацию.
___________
М - отдаленные метастазы3:
Mx - отдаленные метастазы не могут быть оценены; M0 - нет отдаленных метастазов;
M1 - обнаружены отдаленные метастазы;
M1a - метастазы в отдалённый лимфоузел /отдаленные лимфоузлы; M1b - метастазы в кость/кости;
M1c - метастазы другой локализации/других локализаций.
________________
3 При классификации следует использовать высшую категорию, если метастазирован более чем один участок.
___________
Широкое распространение в клинической урологии для определения степени агрессивности РПЖ получила шкала Глисона. Она представляет собой количественную оценку степени злокачественности опухоли и складывается из суммы баллов двух наиболее распространенных по частоте встречаемости ее гистологических градаций (от 1 до 5 баллов). Показатели шкалы Глисона варьируют в интервале от 2 до 10 баллов. Чем
больше баллов по шкале Глисона, тем опухоль менее дифференцирована и, значит, более агрессивна.
Впрактической деятельности нашла применение клинико-морфологическая характеристика РПЖ (табл. 11.3).
Взависимости от особенностей клинического течения различают латентный
(бессимптомный) и клинически значимый РПЖ. Латентный РПЖ (Т1-2а, G< 6, объем опухоли менее 0,5 см3) характеризуется малой вероятностью прогрессирования и развития осложнений и чаще всего обнаруживается только при аутопсии. Практически 85-90 % больных остаются клинически здоровыми до конца жизни, и, как правило, им не требуется медицинского вмешательства. Пятилетняя выживаемость в этой группе составляет 100,0 % независимо от того, получали они лечение или нет. Клинически
