
lecture2ах
.pdf
Розрахунок рН розчинів слабких протолітів
Протоліз слабких основ : |
= |
K b |
|
Cосн |
|||
|
|
Протоліз слабких протолітів посилюється при розбавленні. Це приводить до зміни рН розчину.
[H3O+] = |
[H3O+] = |
|
K a Cкисл |
звідки рН = |
pK a pC |
|
2 |
||
|
[OH–] = [OH–] = 
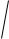 KbCосн
KbCосн
рН = pКw – рОН = 14 – |
pKb pCосн |
|
2
Скисл > 102 Kа , |
Сосн > 102 Kb |

.
Розчини багатопротонних протолітів,
амфолітів і сумішей протолітів
рKа1 |
< рKа2 – 3 |
|
(для кислот) |
|
|
|
|
|
|||
рKb1 |
< рKb2 – 3 |
|
(для основ) |
|
|
|
|
|
|||
[H3O+] = |
|
|
|
|
|
|
1 |
|
|
|
|
K a |
|
K a |
|
|
pH |
pK a |
pK a |
|
|||
|
|
|
2 |
|
|||||||
|
|
|
1 |
|
2 |
|
|
1 |
|
2 |
|
|
|
|
|
|
|
|
|
||||
|
n |
|
n |
|
С кисл i |
|
|
рН = – lg |
рН = 14 + lg |
Сосн i |
|
i |
1 |
i |
1 |
NH + |
NH |
4 |
3 |
pH |
рН = рKа |
= 0,5 |
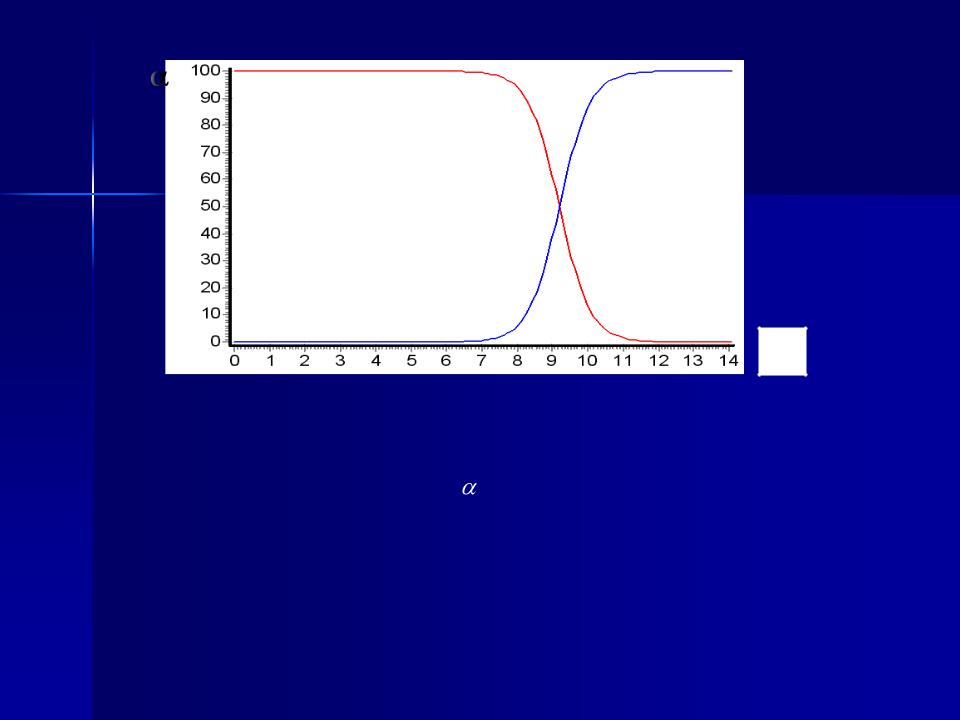
, %
рН
Стан пірофосфатної кислоти в водном у розчині:
1 – H4R; 2 – H3R– ; 3 – H2R2– ; 4 – HR3–; 5 – R4–

Буферні розчини
[H |
O+] = Kа |
НА |
|
|
рН = рKа + lg |
|
А |
|
|||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||
3 |
|
|
А |
|
|
|
|
НА |
|
||
|
|
|
|
|
|
|
|
||||
|
[HA] ≈ Cкисл |
|
|
[A] ≈ Cосн |
|
|
|
|
|||
рН = рKа + lg |
|
Сосн |
|
|
0,1 ≤ |
Сосн |
|
≤ 10 |
|||
|
|
|
Скисл |
||||||||
|
|
|
|
|
|
|
|||||
|
|
|
Скисл |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||
рН = 14 – (рKа + lg |
|
Сосн |
) |
|
|
|
|
||||
|
Скисл |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|

Кількісні характеристики гідролізу
Сіль, утворена
слабкою |
слабкою |
слабкою |
кислотою та |
основою та |
кислотою та |
сильною |
сильною |
слабкою |
основою |
кислотою |
основою |
Кгідр
h
[H3O+]
pH
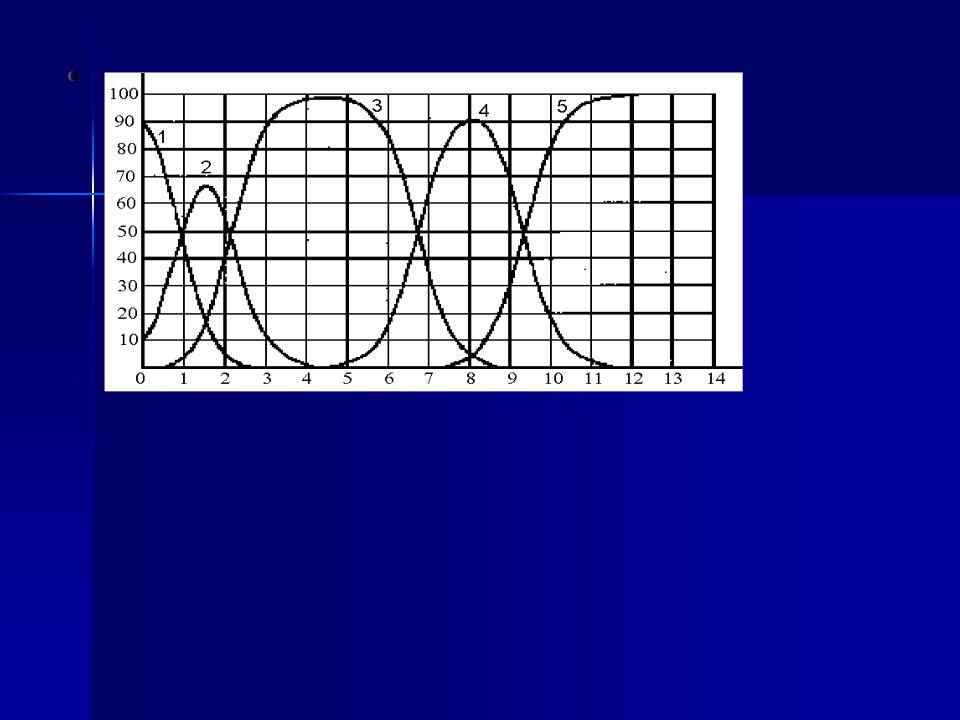
Розв’язування типових задач
Задача 1. Визначте pH і pαH+ розчину, одержаного при розчиненні 10мл 70%-го розчину сульфатної кислоти густиною 1,61г/мл в 250мл води.
Розв’язування. Маса 10мл розчину H2SO4 дорівнює
m |
p |
V |
10 1,61 16,1 |
. |
|
|
г |
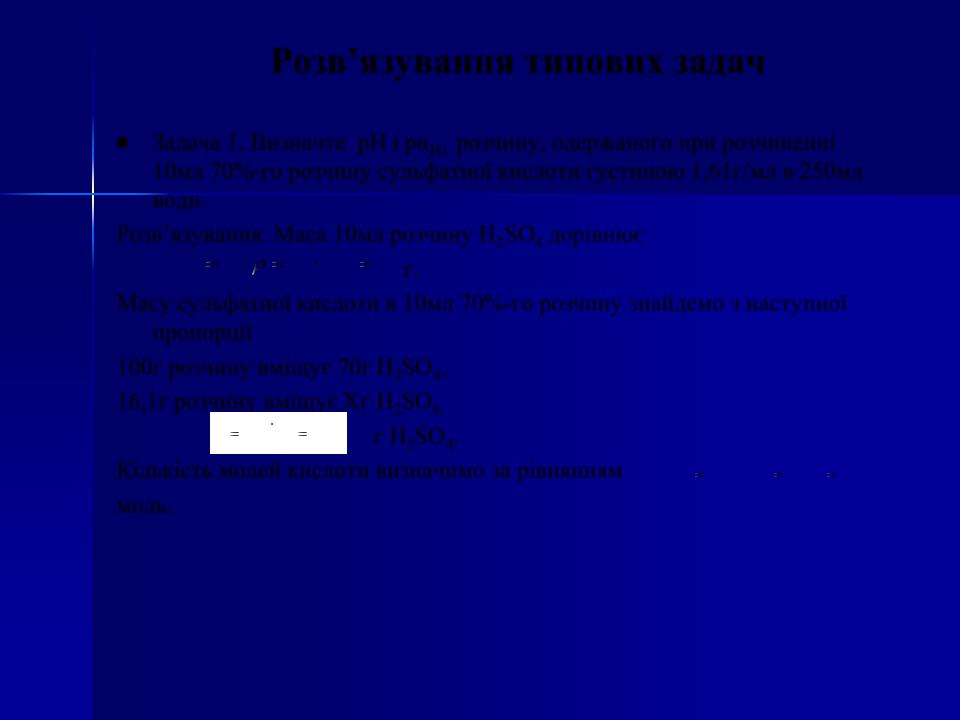
Масу сульфатної кислоти в 10мл 70%-го розчину знайдемо з наступної пропорції
100г розчину вміщує 70г H2SO4,
16,1г розчину вміщує Хг H2SO4,
X |
16,1 |
70 |
11,27 |
г H2SO4. |
|
|
|
|
|
|
|
|
|
|
100 |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кількість молей кислоти визначимо за рівнянням |
n |
|
|
mH SO |
|
|
11,27 |
0,115 |
||||||
H SO |
|
2 |
4 |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
M H SO |
|
98 |
|
|||
моль. |
|
|
|
|
|
|
2 |
4 |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
2 |
|
4 |
|
|
|
|
