
lecture2ах
.pdf
Основні положення протолітичної теорії
Швидка передача протонів через водний розчин
Протонизаряджені частинки надзвичайно малі за розміром, мають сильне електричне поле. Тому ізольований протон Н+ у розчині не існує. Як і інші розчинені частинки, він сольватується розчинником з утворенням іону H3O+ у воді. Перенесення протона від кислот до основ йде не тільки при прямому зіткненні відповідних частинок, але і за складним «естафетним» механізмом, в якому беруть участь молекули розчинника.

Протолітичні властивості розчинників
Апротонні - не містять рухомих протонів, малополярні (з дуже низькою величиною діелектричної проникності ) і не здатні до участі в протолітичних реакціях. вуглеводні і їх галогенпохідні, наприклад, С6Н6, СCl4, а також CS2 і інші;
протогенні (кислотні)- легко віддають протони, але здатні і до їх приєднання (безводні СН3СООH, НСООH і інші речовини);
протофільні (основні)- легко приєднують протони, але здатні і до їх
віддачі (етилендіамін H2N(СН2)2NH2 і інші аміни, аміди, гідразин, рідкий аміак);
амфіпротнні, в рівній мірі здатні приєднувати і віддавати протони (спирти).
протоноакцепторні, здатні тільки до приєднання протонів (піридин С5Н5N);
диполярні апротонні (ДАР) – більш полярні ( > 15), ніж інші апротонні розчинники. Їх кислотно-основні властивості слабо
виражені. Приклади: ацетон (СН3)2СО, диметилформамід (СН3)2NСНО, диметилсульфоксид (СН3)2SО, ацетонітрил СН3СN.

Автопротоліз
автопротоліз – перенесення протонів від одних молекул розчинника HL до інших:
HL + HL H2L+ + L–.
H2L+ + L–.
ліоній (H2L+) і ліат (L–).
КHL = a (H2L+) a (L–) ≈ [H2L+] [L–].
Кw = [H3O+][OH–].
С. Серенсен водневий показник (рН).
Для водного середовища
рН = – lg а H3O+. a H3O+ ≈ [H3O+],
Для довільного протолітичного розчинника визначають рН розчину за узагальненою формулою:
рН = – lg [H2L+].
pH = – lg [H+], рК = – lgK, рКHL = –lg КHL.

Шкала рН у воді (а)
і в довільному протолітичному розчиннику (б)
|
|
кисле середовище |
лужне середовище |
||
(а) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
7 |
14 |
|||
|
|
нейтральне середовище |
|||
кисле середовище лужне середовище
(б)
0 |
рКHL/2 |
рКHL |
|
нейтральне середовище |
|

Розрахунок рН розчинів сильних протолітів
Введемо наступні допущення:
у розчині міститься тільки одна речовина, здатна до протолізу;
частинка такої речовини приєднує або віддає тільки один протон;
протоліз йде необоротно і кількісно (на 100 %);
впливом іонної сили розчину можна нехтувати;
концентрація протоліту достатньо висока у порівнянні з концентрацією продуктів автопротолізу. Цій умові відповідають водні розчини, якщо
С > 10–5 М.

Розрахунок рН розчинів сильних протолітів
[H3O+] = Скисл,
рН = –lg Скисл = рСкисл.
Водний розчин сильної основи (NаОН або СН3ОNа)
[OH–] = Сосн
|
O+] = |
Kw |
|
K w |
|
10 |
–14 |
|
[H |
|
= |
|
= |
|
|
, |
|
|
|
|
|
|||||
3 |
[OH ] |
|
Cосн |
|
|
Cосн |
||
|
|
|
|
|||||
рН = 14 – рСосн.
Неводний розчин
рН = рКHL – рСосн.
(< 10–5 М)
Чому дорівнює рН водного розчину HCl з с (НСІ)= 10–9 М?

Константи рівноваги протолітичних реакцій
Протоліз слабкої однопротонної кислоти HА у водному розчині: HА + H2O  А + H3O+;
А + H3O+;
Kа = |
[A] [H3О ] |
|
[HA] |
||
|
константа кислотності характеризує зв'язану пару НА/А.
Величина Ка тим вища, а рКа тим менша, чим сильніше протолізується кислота.
Найсильніша кислота – іон гідроксонію Ка = 1 і рКа = 0. Протоліз слабкої однопротонної основи А
А + H2O  НА + OH–.
НА + OH–.
константа основності Kb:
K = НА ОН |
|
b |
А |
|
|
Чим сильніша основа, тим вище її Kb і нижче рKb. Найсильніша основа– це гідроксид-іон - Kb = 1 і рKb = 0.

Kа Kb = Кw рKа + рKb = 14.
для довільного розчинника одержуємо: Kа Kb = КHL рKа + рKb = рКHL.
рKа характеристика протолітичної пари в цілому: чим вища рKа, тим слабкіша кислота і тим сильніше зв'язана основа (мал.):
Дуже слабкі основи |
Слабкі основи |
Дуже сильні основи |
0 |
Ac– |
NH3 |
14 |
|
|
|
pKa |
Дуже сильні кислоти |
HAc |
+ |
Дуже слабкі кислоти |
|
NH4 |
|
|
|
Слабкі кислоти |
|
|
Сила кислот і основ у водному розчині залежно від величини рKа спряжених протолітичних пар

Реакції нейтралізації
HA + B  A + HB.
A + HB.
Розчинник в цій реакції безпосередньо не бере участь.
A HB
Крівн = |
HA B |
|
для водного розчину
К = |
A |
|
[H |
O+]; |
К = |
B[H |
O+]. |
||||
|
|
||||||||||
a1 |
|
HA |
|
3 |
|
a2 |
HB |
3 |
|
||
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
Ка |
1 |
|
A HB |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кa |
2 |
|
HA B |
|
= Крівн. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
lg Крівн = pKa2 – pKa1.
Таким чином, величина константи рівноваги реакції між основою і кислотою (реакції нейтралізації) визначається різницею рКа протолітичних пар, до яких належать ці речовини.

Розрахунок рН розчинів слабких протолітів
Протоліз слабкої кислоти НА, продукт реакції – А: |
= |
H3О |
= |
А |
||||||
Cкисл |
|
|
||||||||
C |
кисл |
|||||||||
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
||
Протоліз слабкої основи: = |
ОН |
= |
НА |
|
|
|
|
|
||
|
|
|
|
|
|
|
||||
|
Сосн |
|
|
|
|
|
||||
Со сн |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
||||
Закон розбавлення Оствальда.
Скисл = [НА] + [А]
Kа = |
А H3О |
= |
|
2Cкисл2 |
= |
2 C кисл |
|
|
2 |
Cкисл |
|
||||
НА |
|||||||
|
|
Cкисл |
1 |
||||
Для дуже слабкого протолиту ( . <<1) Kа = 2 |
Cкисл |
|
У таких випадках ступінь протолізу приблизно рівний:
K a
= 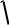 Cкисл
Cкисл
