
Volume1
.pdf
88 |
Часть 1. Введение в мир клетки |
|
Рис. 2.19. Реакция между двумя моносахаридами, |
|
врезультатекоторойобразуетсядисахарид.Этареак- |
|
ция относится к так называемым реакциям конденса- |
|
ции,вкоторыхдвемолекулысоединяютсяврезультате |
|
потеримолекулыводы.Обратнуюреакцию(вкоторой |
|
вода присоединяется) называют гидролизом. Обра- |
|
тите внимание, что реагирующий углерод, с которым |
|
образуется новая связь (на моносахариде слева), — |
|
это углерод, связанный с двумя атомами кислорода |
|
в результате формирования сахарного кольца (см. |
|
рис. 2.18). Как указано на рисунке, такая ковалентная |
|
связь между двумя молекулами сахаров известна как |
|
гликозиднаясвязь(см.такжерис.2.20). |
состоящий из двух единиц глюкозы, может |
существовать в одиннадцати различных раз- |
новидностях (рис. 2.20), тогда как три раз- |
ные гексозы (C6H12O6) могут соединяться |
в различных сочетаниях и образовывать |
несколько тысяч трисахаридов. По этой |
причине определение взаимного простран- |
ственного расположения сахаров в полисахариде является намного более сложной |
задачей, чем определение последовательности нуклеотидов в молекуле ДНК, где |
каждая единица соединена со следующей одним и тем же способом. |
Важнейшим источником энергии для клеток служит моносахарид глюкоза. |
В последовательном ряду реакций она расщепляется на более мелкие молекулы, |
высвобождая энергию, которую клетка может использовать для выполнения по- |
лезной работы, что мы обсудим позже. В качестве энергетических хранилищ клетки |
используют простые полисахариды, состоящие только из глюкозных звеньев, — |
преимущественно гликоген у животных и крахмал у растений. |
Круг функций сахаров отнюдь не ограничен выработкой и накоплением |
энергии. Помимо этого, они могут быть использованы, например, для построения |
механических опор и подложек. Так, наиболее распространенное на Земле органи- |
ческое вещество — целлюлоза клеточных стенок растений — представляет собой |
полисахарид глюкозы. Поскольку межглюкозные связи в целлюлозе так или иначе |
отличаются от таковых в крахмале и гликогене, люди не способны переваривать |
целлюлозу и использовать составляющую ее глюкозу. Другое необычайно рас- |
пространенное органическое вещество — хитин наружных скелетов насекомых |
и клеточных стенок грибов — также является «неудобоваримым» полисахаридом: |
в данном случае это линейный полимер производного глюкозы, называемого |
N-ацетилглюкозамином (см. приложение 2.4). Другие полисахариды служат основ- |
ными компонентами слизи, хрящей и различных секретов. |
Меньшие по размеру олигосахариды могут быть ковалентно связаны с белками, |
образуя гликопротеины, и с липидами с образованием гликолипидов, причем как |
первые, так и вторые входят в состав клеточных мембран. Как описано в главе 10, по- |
верхности большинства клеток облечены и убраны гликопротеинами и гликолипидами, |
унизывающими клеточную мембрану. Боковые цепи сахаров в этих молекулах часто |
избирательно опознаются другими клетками. И различия между людьми, основанные |
Глава 2. Химия клетки и биосинтез 89
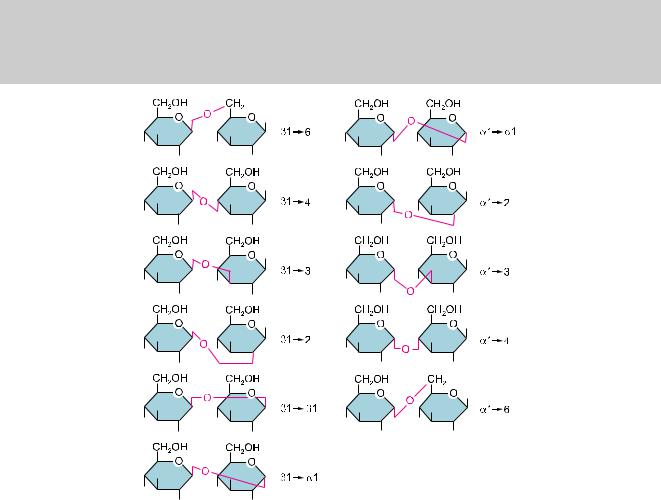
Рис. 2.20. Одиннадцать дисахаридов, состоящих из двух мономеров D-глюкозы. Отличаясь лишь типомсвязимеждудвумязвеньямиглюкозы,этидисахаридыхимическиразличны.Таккаколигосахариды, связанные с белками и липидами, могут иметь шесть и более различных сахаров, соединенных как в линейном порядке, так и в разветвленном положении посредством гликозидных связей, таких, как показаны здесь, число различных типов олигосахаридов, которые могут использоваться клеткой, чрезвычайновелико.Объяснениеразличиймеждуα-иβ-связямидановприложении2.4(стр.178–179). Короткие черные линии, которые выглядят как «тупиковые», указывают положения групп –ОН. (Красные линии показывают лишь ориентации дисахаридных связей и «углы» не подразумевают наличия дополнительныхатомов.)
на особенностях строения сахаров на поверхности клеток, легли в основу классификации четырех основных групп крови человека, названных A, B, AB и O.
2.1.12. Жирные кислоты – компоненты клеточных мембран, а также источники энергии
Молекула жирной кислоты, такой как пальмитиновая кислота, имеет две химически различные области (рис. 2.21). Одна из них — длинная углеводородная цепь, которая является гидрофобной и не очень активна химически. Вторая — карбоксильная группа (–COOH), которая проявляет кислотные свойства (карбоновой кислоты): она ионизируется в растворе (–СОО–), чрезвычайно гидрофильна и химически активна. В клетке почти все молекулы жирных кислот своими карбоксильными группами ковалентно связаны с другими молекулами.

90 Часть 1. Введение в мир клетки
Рис. 2.21. Жирная кислота. Жирная кислота состоит из гидрофобной углеводородной цепи, к которой присоединена гидрофильная карбоксильная группа. Здесь показана пальмитиновая кислота. Различные жирныекислотыимеютразныеуглеводородныехвосты. а) Структурная формула. Карбоксильная группа показанавионизированнойформе.б)Шаростержневаямодель.в)Полусферическая(объемная)модель.
Углеводородный хвост пальмитиновой
кислоты насыщен: он не имеет двойных свя-
зей между атомами углерода и содержит максимально возможное число атомов водорода. Стеариновая кислота — еще один
представитель обычных жирных кислот
в животном жире — также насыщенна. Не-
которые другие жирные кислоты, такие как олеиновая кислота, имеют ненасыщенные хвосты с одной и более двойными связями,
рассредоточенными по длине. Двойные связи
создают в молекулах перегибы, нарушающие
их способность формировать плотную упаковку. Именно этим и объясняется различие между твердым маргарином (насыщенным)
и жидкими растительными маслами (поли-


 ненасыщенными). Множество различных жирных кислот, присутствующих в клетках, различаются длиной своих углеводородных цепей, а также числом и положением
ненасыщенными). Множество различных жирных кислот, присутствующих в клетках, различаются длиной своих углеводородных цепей, а также числом и положением
углерод-углеродных двойных связей (см. приложение 2.5, стр. 180–181).
Жирные кислоты запасаются в цитоплазме многих клеток в форме капелек из молекул триацилглицерина (часто называют триглицеридами), которые состоят из трех цепей жирных кислот, присоединенных к молекуле глицерина (см. приложение 2.5); из таких молекул и состоят животные жиры, присутствующие
вмясе, масле и сливках, и растительные масла — такие как кукурузное и оливковое. Когда клетке требуется энергия, цепи жирных кислот высвобождаются из триацилглицеринов и расщепляются до двууглеродных структурных единиц. Эти двууглеродные звенья тождественны субъединицам, получаемым при расщеплении глюкозы, и они вступают в те же протекающие с выделением энергии реакции, что будут описаны позже в этой главе. Триглицериды служат концентрированным запасом пищи в клетках, потому что они могут быть расщеплены с получением приблизительно в шесть раз большего количества полезной энергии, чем можно получить из того же количества (по массе) глюкозы.
Жирные кислоты и их производные типа триацилглицеринов являют нам примеры липидов. В число липидов входит получившая расплывчатое определение группа биологических молекул, которые нерастворимы в воде, но растворимы
вжире и органических растворителях типа бензола8. Они, как правило, содержат
8 В таком определении вместо четкой химической характеристики класса говорится о физических свойствах липидов. На сегодня принято следующее определение липидов: «Липиды – это

Глава 2. Химия клетки и биосинтез 91
либо длинные углеводородные цепи, как в жирных кислотах и терпенах, либо многочисленные связанные кольца-циклы , как в стероидах.
Наиболее важная функция жирных кислот в клетках состоит в построении клеточных мембран. Эти тонкие покровы (оболочки) окружают все клетки и ограждают их внутренние органеллы. Они состоят в основном из фосфолипидов, которые представляют собой маленькие молекулы, которые, подобно триацилглицеринам, построены главным образом из жирных кислот и глицерина. Однако в фосфолипидах к глицерину присоединены две цепи жирных кислот, а не три, как в триацилглицеринах. «Третий» участок на глицерине занимает гидрофильная фосфатная группа, которая, в свою очередь, присоединена к маленькому гидрофильному соединению, такому как холин (см. приложение 2.5). Поэтому каждая молекула фосфолипида состоит из гидрофобного хвоста двух цепей жирных кислот и гидрофильной фосфатной головки. Это придает фосфолипидам характерные физические и химические свойства, отличающие их от более гидрофобных триацилглицеринов. Такие молекулы как фосфолипиды, имеющие и гидрофобные и гидрофильные области,
называют амфифильными.
Присущее фосфолипидам свойство образовывать мембраны обусловлено их амфифильной природой. Фосфолипиды растекаются по поверхности воды и образуют одинарный слой фосфолипидных молекул, в котором гидрофобные хвосты обращены к воздуху, а гидрофильные головки погружены в воду. Два таких молекулярных слоя могут легко объединиться в воде по принципу хвост-к-хвосту и образовать фосфолипидный «сэндвич», или липидный бислой. Такой бислой является структурной основой всех клеточных мембран (рис. 2.22).
Рис. 2.22. Структура фосфолипида и ориентация в мембранах. В водной среде гидрофобные хвосты фосфолипидов собираются вместе, чтобы исключить воду. Здесь они сформировали двойной слой таким образом, что гидрофильная головка каждого фосфолипида обращена к воде. Двойные липидные слои—основаклеточныхмембран,очеммыподробнопоговоримвглаве10.
найденные в природе жирные кислоты, их производные и продукты метаболических превращений с преимущественным сохранением углеродного скелета.» В такой формулировке встает вопрос о принадлежности терпенов и стероидов к липидам. — Прим. ред.

92 Часть 1. Введение в мир клетки
2.1.13. Аминокислоты — субъединицы белков
Аминокислоты образуют класс разнообразных молекул с одним определяющим свойством: все они обладают карбоксильной группой и аминогруппой, которые присоединены к одному атому углерода, названному α-углеродом (рис. 2.23). Их химическое разнообразие обусловлено боковой цепью, которая также присоединена к α-углероду. Огромное значение аминокислот в клетке связано с их ролью в построении белков, которые являются полимерами аминокислот, соединяющихся по принципу голова- к-хвосту в длинную цепь, которая затем сворачивается в трехмерную структуру, уникальную для белка каждого типа. Ковалентные связи между двумя смежными аминокислотами в белковой цепи образуют амид (см. приложение 2.1) и зовутся пептидными связями; цепь аминокислот известна также под названием полипептид (рис. 2.24). Независимо от специфических аминокислот, из которых состоит полипептид, он имеет аминогруппу (NH2) на одном конце (его N-конец) и карбоксильную группу (COOH) на другом конце (его C-конец). Это придает ему определенную направленность — структурную (в отличие от электрической) полярность.
Рис. 2.23. Аминокислота аланин. а) В клетке, где значение pH близко к 7, свободная аминокислота существуетвионизированнойформе;нокогдаонавстраиваетсявполипептиднуюцепь,зарядынаамино- и карбоксильной группах исчезают. б) Шаростержневая модель и в) полусферическая (объемная)
модельмолекулыаланина(H—белый;C—черный;O—красный;N—синий).
Каждая из 20-ти аминокислот, обычно входящих в белки, имеет уникальную для своего типа боковую цепь, присоединенную к атому α углерода (см. приложение 3.1, стр. 194–195). Все организмы, будь то бактерии, археи, растения или животные, имеют белки, построенные из одних и тех же 20-ти аминокислот. Каким образом этот точно установленный набор из 20-ти элементов был избран, является одной из необъяснимых тайн эволюции жизни; нет никакой очевидной с точки зрения химии причины, по которой другие аминокислоты не могли бы сослужить такую же службу. Но как только данный выбор утвердился, он уже не мог быть изменен —слишком многое от него зависело.
Подобно сахарам, все аминокислоты, кроме глицина, существуют в виде оптических изомеров: в D- и L-форме (см. приложение 3.1). Но в составе белков непреложно встречаются только L-формы (хотя D-аминокислоты входят в состав стенок бактериальных клеток и некоторых антибиотиков). Первопричина такого

Глава 2. Химия клетки и биосинтез 93
Рис. 2.24. Небольшая часть белковой молекулы. Четыре показанныеаминокислотысоединеныдругсдругомтремя пептиднымисвязями,однаизкоторыхвыделенажелтым. Однаизаминокислототтененасерым.Боковыецепиаминокислот показаны красным. Два конца полипептидной цепи химически различны. Один конец, N-конец, оканчивается аминогруппой,адругой,C-конец,—карбоксильнойгруппой. Последовательность всегда читается со стороны N-конца; следовательно, в данном примере представлена последо-
вательностьPhe-Ser-Glu-Lys.
исключительного использования L-аминокислот
в построении белков — еще одна необъяснимая загадка эволюции. Химическая универсальность этих 20-ти
аминокислот существенна для функции белков.
Пять из этих 20-ти аминокислот имеют боковые цепи, которые способны образовывать ионы
в нейтральном водном растворе и, таким образом, могут нести заряд (рис. 2.25). Другие незаряжены; некоторые полярны и гидрофильны, а некоторые неполярны и гидрофобны. Как мы покажем в главе 3, свойства боковых цепей аминокислот лежат в основе разнообразных и сложных функций белков.
2.1.14. Нуклеотиды — субъединицы ДНК и РНК
Нуклеотид — молекула, состоящая из содержащего азот циклического соединения, связанного с сахаром-пентозой, который, в свою очередь, несет одну или несколько фосфатных групп (приложение 2.6, стр. 182–183). Пятиуглеродный сахар может быть представлен либо рибозой, либо дезоксирибозой. Нуклеотиды, содержащие рибозу, известны как рибонуклеотиды, а те, что содержат дезоксирибозу, — как дезоксирибонуклеотиды. Содержащие азот циклические соединения обычно упоминаются как основания по историческим причинам: в кислых условиях каждое из них может связывать H+ (протон) и таким образом повышать концентрацию ионов ОН– в водном растворе. Между различными основаниями существует сильное «семейственное сходство». Цитозин (C), тимин (T) и урацил (U) называют пиримидинами, потому что все они суть производные шестичленного пиримидинового кольца; гуанин (G) и аденин (A) — соединения пурина, и в их молекулах присутствует второе, пятичленное, кольцо, примыкающее к шестичленному. Каждый нуклеотид получил название по имени основания, которое он содержит (см. приложение 2.6).
Нуклеотиды могут выступать в роли краткосрочных носителей химической энергии. И в первую очередь это рибонуклеотид аденозинтрифосфат, или ATP (adenosine triphosphate) (рис. 2.26), который переносит энергию в сотнях различных внутриклеточных реакций. АТР образуется в результате реакций, которые подпитываются энергией, высвобождаемой в ходе окислительного расщепления молекул питательных веществ. Входящие в состав молекулы ATP три фосфата связаны последовательно в ряд двумя фосфоангидридными связями, при разрыве которых высвобождается большое количество полезной энергии. Концевая фосфатная группа особенно часто отщепляется путем гидролиза, при этом зачастую

94 Часть 1. Введение в мир клетки
Рис.2.25.ЗарядбоковыхцепейаминокислотзависитотpH.Показанопятьразличныхбоковыхцепей,
которыемогутнестизаряд.КарбоновыекислотымогутлегкопотерятьH+ вводномраствореиобразовать отрицательно заряженный ион, который обозначают суффиксом «ат», как например, в названиях аспартат или глутамат. Схожая ситуация имеет место у аминов, которые в водном растворе могут принять H+ и образовать положительно заряженный ион (который не имеет специального названия). Этиреакциибыстрообратимы,иколичествадвухвозможныхформ—заряженнойинезаряженной— зависят от pH раствора. При высоком pH карбоновые кислоты имеют тенденцию быть заряженными ,
аамины — незаряженными. Принизком pH происходит обратное: карбоновыекислоты незаряжены,
ааминызаряжены.ЗначениеpH,прикоторомровнополовинаостатковкарбоновыхкислотилиаминов заряжена,известнокакpKбоковойцепиаминокислоты(обозначеножелтойполосой).
ВклеткеpHблизкок7,такчтопочтивсекарбоновыекислотыиаминызаряжены.
фосфат переносится на другие молекулы и высвобождается энергия, которая идет на энергопотребляющие реакции биосинтеза (рис. 2.27). Другие нуклеотидные производные служат носителями для переноса других химических групп, как будет описано позже.
Однако самая наиважнейшая роль нуклеотидов в клетке — это хранение и извлечение биологической информации. Нуклеотиды служат как бы строительными

Глава 2. Химия клетки и биосинтез 95
Рис. 2.26. Химическая структура аденозинтрифосфата (ATP). а) Структурная формула. б) Полусфери-
ческая (объемная) модель. В модели б цвета атомов следующие: C — черный; N — синий; H — белый;
O—красный;P — желтый.
Рис. 2.27. Молекула ATP служит переносчиком (и носителем) энергии в клетках. «Энергопотребляю-
щая» реакция образования ATP из ADP (аденозиндифосфата) и неорганического фосфата сопряжена с «энерговыделяющим» окислением пищевых продуктов (в клетках животных, грибов и некоторых бактерий)илиспоглощениемсветовойэнергии(вклеткахрастенийинекоторыхбактерий).Гидролизже ATPобратнонаADPинеорганическийфосфат,всвоюочередь,обеспечиваетэнергиеймногиереакции, протекающиевклетке.
блоками для построения нуклеиновых кислот — длинных полимеров, в которых нуклеотидные субъединицы ковалентно связаны друг с другом фoсфодиэфирными связями, образующимися между фосфатной группой одного нуклеотида и гидроксильной группой cахара следующего нуклеотида (рис. 2.28). Цепи нуклеиновых кислот синтезируются из богатых энергией нуклеозидтрифосфатов путем реакции конденсации, в ходе которой при образовании фосфодиэфирной связи высвобождается неорганический пирофосфат.

96 Часть 1. Введение в мир клетки
Рис. 2.28. Малая часть одной из цепей молекулы дезоксирибонуклеиновой кислоты (ДНК). Показаны четыре нуклеотида. Одна из фосфодиэфирных связей, соединяющихсоседниеостаткинуклеотидов,выделена желтым, а один из нуклеотидов затушеван серым. Нуклеотиды соединены друг с другом фосфодиэфирными связями между определенными углеродными атомамирибозы,известнымикак5'-и3'-атомы.Поэтой причинеодинконецполинуклеотиднойцепи,5'-конец, всегда имеет свободную фосфатную группу, а другой, 3' конец,—свободнуюгидроксильнуюгруппу.Линей- ная последовательность нуклеотидов в полинуклеотидной цепи обычно записывается в краткой форме однобуквенным кодом и всегда читается с 5'-конца. В данном примере представлена последовательность
G–A–T–C.
Существует два главных типа нуклеи- |
новых кислот, отличающихся сахаром в са- |
харофосфатном остове. Те, что построены |
на основе сахара рибозы, известны как рибо- |
нуклеиновые кислоты, или РНК, и обычно |
содержат основания A, G, C и U. Те, что син- |
тезируются на основе дезоксирибозы (в кото- |
рой гидроксильная группа в позиции 2' угле- |
родного кольца рибозы заменена водородом), |
известны как дезоксирибонуклеиновые кис- |
лоты, или ДНК, и содержат основания A, G, |
C и T (T химически подобен U, входящему |
в состав РНК, и отличается лишь наличием |
дополнительной метильной группы в пири- |
мидиновом кольце; см. приложение 2.6). |
РНК обычно встречается в клетках в виде |
одинарной полинуклеотидной цепи, но ДНК |
практически всегда представлена двухцепо- |
чечной молекулой — двойная спираль ДНК |
состоит из двух полинуклеотидных цепей, |
направленных антипараллельно друг другу |
и удерживаемых вместе водородными свя- |
зями, образованными между основаниями |
двух цепей. |
Линейная последовательность нуклео- |
тидов в ДНК или РНК кодирует генети- |
ческую информацию клетки. Способность оснований в различных молекулах |
нуклеиновых кислот узнавать друг друга и образовывать пары посредством |
водородных связей (так называемое спаривание оснований): G с C и А с T или |
с U — лежит в основе всей наследственности и эволюции, что мы подробнее по- |
ясним в главе 4. |

Глава 2. Химия клетки и биосинтез 97
2.1.15. В химии клеток господствуют макромолекулы с удивительными свойствами
Повесумакромолекулысоставляютнаибольшуючастьсредиуглерод-содержащих молекул в живой клетке (рис. 2.29 и таблица 2.3). Они служат основными строительными блоками, из которых построена клетка, а также являются компонентами, которые обусловливают наиболее характерные свойства живых существ. Макромолекулы клеток представляют собой полимеры, которые построены из ковалентно связанных маленьких органических молекул (называемых мономерами) в длинные цепи (рис. 2.30). И тем не менее они обладают примечательными свойствами, которые невозможно было бы предсказать по их простым составляющим.
Рис. 2.29. Клетки изобилуют макромолекулами. Приблизительный состав бактериальной клетки показанввесовомсоотношении;животнаяклеткаимеетпохожийсостав(см.табл.2.3).
Белки особенно многочисленны и многофункциональны. Они исполняют тысячи различных функций в клетках. Многие белки «служат» ферментами, то есть катализаторами, которые управляют множеством необходимых для жизнедеятельности клетки реакций образования и разрыва ковалентных связей. Ферменты катализируют все реакции, посредством которых клетки извлекают энергию из молекул пищи. Например, фермент фотосинтезирующих организмов, названный рибулозобифосфаткарбоксилазой, помогает превращать CO2 в сахара, производя таким образом львиную долю органической материи, необходимой для жизни на Земле. Другие белки используются для построения структурных компонентов клетки, таких как тубулин (белок, который самособирается в длинные микротрубочки клетки) или гистоны (белки, которые упаковывают ДНК в хромосомах). Некоторые белки работают молекулярными двигателями по производству силы и движения – как
